
Wetenschap
Kan iemand helpen met deze chemische vergelijking K4FEC6N6 plus KMNO4 H2SO4 KHSO4 FE2S3?
Hier is de uitsplitsing en uitleg:
1. Het identificeren van de reactanten en producten:
* reactanten:
* Kalium ferricyanide (k₄fe (cn) ₆)
* Kalium permanganaat (kmno₄)
* Zwavelzuur (h₂so₄)
* Producten:
* Kalium bisulfate (khso₄)
* IJzer (iii) sulfide (fe₂s₃)
2. De vergelijking in evenwicht brengen:
De volledige gebalanceerde chemische vergelijking is complex en omvat meerdere stappen en nevenreacties. Hier is een vereenvoudigde weergave van de hoofdreactie:
3K₄FE (CN) ₆ + 8kmno₄ + 24h₂so₄ → 12khso₄ + Fe₂s₃ + 18co₂ + 8mnso₄ + 18no₂ + 12h₂o
Verklaring van het evenwichtsproces:
* ijzer (Fe): 3 mol k₄fe (CN) ₆ aan de reactantzijde vereisen 2 mol Fe₂s₃ aan de productzijde om de ijzeratomen in evenwicht te brengen.
* Mangaan (Mn): 8 mol kmno₄ aan de reactant -zijde vereisen 8 mol mnso₄ aan de productzijde om de mangaanatomen in evenwicht te brengen.
* kalium (k): De kaliumatomen balanceren automatisch met de vorming van KHSO₄ en MNSO₄ aan de productzijde.
* zwavel (s): 24 mol h₂so₄ aan de reactant -zijde draagt bij aan de vorming van 12 mol khso₄ en 1 mol Fe₂s₃ aan de productzijde, waarbij de zwavelatomen in evenwicht komen.
* koolstof (c): 18 mol Co₂ worden geproduceerd aan de productzijde om de 18 koolstofatomen van de 3 mol K₄FE (CN) ₆ aan de reactantzijde in evenwicht te brengen.
* stikstof (n): 18 mol No₂ worden geproduceerd aan de productzijde om de 18 stikstofatomen van de 3 mol k₄fe (CN) ₆ aan de reactantzijde in evenwicht te brengen.
* zuurstof (O): De zuurstofatomen worden in evenwicht gebracht door de vorming van co₂, no₂, h₂o en so₄²⁻ ionen in de producten.
* waterstof (h): 24 mol h₂so₄ aan de reactant -zijde draagt bij aan de vorming van 12 mol khso₄ en 12 mol h₂o aan de productzijde, waarbij de waterstofatomen balanceren.
belangrijke opmerkingen:
* Deze reactie is zeer complex en kan verschillende andere producten produceren naast die vermeld. Het gaat om redoxreacties, neerslag en gasevolutie.
* De vereenvoudigde vergelijking vertegenwoordigt niet alle mogelijke producten of de stoichiometrie nauwkeurig.
* Het is belangrijk om de juiste laboratoriumtechnieken en veiligheidsmaatregelen te gebruiken bij het hanteren van chemicaliën.
Als u meer informatie of opheldering nodig hebt, kunt u het vragen!
 Welke groep bevat acht valentie-elektronen?
Welke groep bevat acht valentie-elektronen?  Wat is een evenwichtige vergelijking voor magnesiumbromide en hydlocloorzuur die hydrobrome chloride produceren?
Wat is een evenwichtige vergelijking voor magnesiumbromide en hydlocloorzuur die hydrobrome chloride produceren?  Welke massa waterstofchloride wordt gevormd als 1 mol reageert met chloor?
Welke massa waterstofchloride wordt gevormd als 1 mol reageert met chloor?  Het verschil tussen convectie en advectie Heat Transfers
Het verschil tussen convectie en advectie Heat Transfers Verschillen tussen polyethyleen en polyurethaan
Verschillen tussen polyethyleen en polyurethaan
 Superbug-gen gevonden op een van de meest afgelegen plekken op aarde
Superbug-gen gevonden op een van de meest afgelegen plekken op aarde Wetenschappers schatten de ijsdikte en subglaciale terreinen in de Yulong-sneeuwberg
Wetenschappers schatten de ijsdikte en subglaciale terreinen in de Yulong-sneeuwberg NASA volgt hittegolf boven het zuidwesten van de VS
NASA volgt hittegolf boven het zuidwesten van de VS Het vervangen van plastic door alternatieven is in de meeste gevallen slechter voor de uitstoot van broeikasgassen, zo blijkt uit onderzoek
Het vervangen van plastic door alternatieven is in de meeste gevallen slechter voor de uitstoot van broeikasgassen, zo blijkt uit onderzoek  Wat is het klimaat in Ontraion?
Wat is het klimaat in Ontraion?
Hoofdlijnen
- Xist markeert de plek:hoe een RNA-molecuul het X-chromosoom tot zwijgen brengt
- Welke koolhydraten vormt de celwallof planten?
- Kunnen honden snel woorden leren?
- De hongerige insecten die de mestcrisis in Oeganda bestrijden
- Wat is een definitie van basis?
- Orka's leren elkaar hoe ze vis kunnen stelen uit menselijke visserij
- Onderzoek laat zien hoe ribosomen hun blokkades opheffen
- Hoe een moleculaire schakelaar de groei van plantenorganen vormgeeft
- Veranderingen in diervoeder kunnen 1 miljard mensen van voedsel voorzien
- Team ontwikkelt afscheider die gasovergang voor waterelektrolyse vermindert

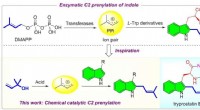
- Bio-geïnspireerde door zuur gekatalyseerde C2-prenylatie van indoolderivaten
- Monstervoorbereiding in forensische toxicologische analyse kan enorme gevolgen hebben

- Produceren van F-18-radiofarmaca voor PET-beeldvorming
- Een draagbaar meetapparaat om optimale rijpheid in tomaten te detecteren

 Wat wordt gas als het zijn condensatiepunt bereikt?
Wat wordt gas als het zijn condensatiepunt bereikt?  Vlakke graslanden die in hoogte toenemen?
Vlakke graslanden die in hoogte toenemen?  Houd je van Vos? MSNBC? Het kan zijn dat je opgesloten zit in een ‘partijdige echokamer’, zo blijkt uit onderzoek
Houd je van Vos? MSNBC? Het kan zijn dat je opgesloten zit in een ‘partijdige echokamer’, zo blijkt uit onderzoek  Op ras gebaseerd politiegeweld heeft gevolgen voor de rijkdom van zwarte gezinnen, zo blijkt uit onderzoek
Op ras gebaseerd politiegeweld heeft gevolgen voor de rijkdom van zwarte gezinnen, zo blijkt uit onderzoek  Welke terreinen bestudeert elk van de vijf takken van de aardwetenschappen?
Welke terreinen bestudeert elk van de vijf takken van de aardwetenschappen?  Nieuwe hydrogel verwijdert microplastics uit water
Nieuwe hydrogel verwijdert microplastics uit water  'Aleppo-momenten':wat zorgt ervoor dat onze hersenen bevriezen onder druk?
'Aleppo-momenten':wat zorgt ervoor dat onze hersenen bevriezen onder druk?  Magnetische velden gevonden in een jet van een babyster
Magnetische velden gevonden in een jet van een babyster
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

