
Wetenschap
Waarom hebben kleinere sterk geladen ionen een grotere affiniteit voor een ionenuitwisselingskolom dan groter met lading?
1. Elektrostatische interacties:
* Laaddichtheid: Kleinere ionen hebben een hogere ladingsdichtheid omdat hun lading in een kleiner volume is geconcentreerd. Dit leidt tot sterkere elektrostatische interacties met de tegengesteld geladen groepen op de ionenuitwisselingshars.
* Hydratatie: Kleinere ionen zijn sterker gehydrateerd, wat betekent dat ze meer watermoleculen aantrekken. Deze hydratatieschaal kan interacties met de hars belemmeren. Sterk geladen ionen overwinnen dit effect echter omdat de sterke elektrostatische interacties domineren.
2. Grootte en toegankelijkheid:
* Toegankelijkheid: Kleinere ionen kunnen gemakkelijker in de poriën van de hars passen, waardoor de kans op interactie met de uitwisselingssites wordt vergroot. Grotere ionen kunnen moeite hebben om toegang te krijgen tot deze sites vanwege sterische hindering.
3. Ionenuitwisselingscapaciteit:
* affiniteit versus capaciteit: Hoewel kleinere, sterk geladen ionen een hogere affiniteit hebben voor de hars, is de totale ionenuitwisselingscapaciteit (de totale hoeveelheid ionen die kan worden uitgewisseld) afhankelijk van het aantal uitwisselingsplaatsen en de grootte van de harsdeeltjes.
Samenvattend:
Kleinere sterk geladen ionen hebben een grotere affiniteit voor ionenuitwisselingskolommen omdat:
* Ze vertonen sterkere elektrostatische interacties vanwege hun hogere ladingsdichtheid.
* Ze zijn meer toegankelijk voor de uitwisselingssites in de hars vanwege hun kleinere maat.
Opmerking: De specifieke affiniteit van een ion voor een ionenuitwisselingskolom kan ook worden beïnvloed door andere factoren zoals pH, temperatuur en het type hars dat wordt gebruikt.
 De atomen in een watermolecuul worden bij elkaar gehouden door covalente bindingen. Dit betekent dat de gebonden atomen?
De atomen in een watermolecuul worden bij elkaar gehouden door covalente bindingen. Dit betekent dat de gebonden atomen?  Hoe breekt de ozon uit?
Hoe breekt de ozon uit?  Verbetering van de efficiëntie van de ionentransmissie van massaspectrometers
Verbetering van de efficiëntie van de ionentransmissie van massaspectrometers Wat voor soort azijn lost snoep op?
Wat voor soort azijn lost snoep op?  Wetenschappers ontdekken groenere route naar veelgebruikt industrieel materiaal
Wetenschappers ontdekken groenere route naar veelgebruikt industrieel materiaal
 Verkenning Indische Oceaan maakt historische onderzeese uitzending
Verkenning Indische Oceaan maakt historische onderzeese uitzending Enorme reddingspoging na dodelijke stormtonnen in heel Frankrijk, Italië
Enorme reddingspoging na dodelijke stormtonnen in heel Frankrijk, Italië Dit is hoe vervuiling door perfluorstoffen wordt verspreid in Spanje
Dit is hoe vervuiling door perfluorstoffen wordt verspreid in Spanje Door zware regenval doen rivieren zwellen, waardoor in een groot deel van Thailand overstromingen ontstaan
Door zware regenval doen rivieren zwellen, waardoor in een groot deel van Thailand overstromingen ontstaan Afrikaanse landen hebben meer luchtkwaliteitsgegevens nodig - en door deze te delen, worden de voordelen ervan ontgrendeld
Afrikaanse landen hebben meer luchtkwaliteitsgegevens nodig - en door deze te delen, worden de voordelen ervan ontgrendeld
Hoofdlijnen
- Wetenschappers identificeren sleutelfactoren die microben helpen gedijen in ruwe omgevingen
- Welke dieren hebben witte sclera?
- Plantensporen worden rechtstreeks geproduceerd door?
- Sociale hersenen:delen insectengemeenschappen de hersenkracht?
- Familiebanden Snapper leveren nieuw bewijs op over mariene reservaten
- Bioloog volgt de ogen van spinnen om te leren hoe kleine hersenen informatie verwerken
- Wat is de wetenschappelijke naam voor root haarcel?
- Celstructuur van Nostoc
- Welke ecologische omstandigheden kunnen volgens u leiden tot de snelle diversificatie van sommige lijnen?
- Biologische voedingsmiddelen verifiëren
- Team ontdekt controle over celsignalering met behulp van een kobalt (III)-nitrosylcomplex

- Wetenschappers ontwikkelen milieuvriendelijke, vorstbestendige coatings

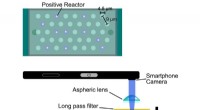
- Smartphone-virusscanner:met nieuw draagbaar apparaat kunnen smartphones biologische virussen tellen
- NREL onderzoekt coatings die nodig zijn voor het concentreren van zonne-energie

 Verhoogt of verlaagt de regen de pollentelling?
Verhoogt of verlaagt de regen de pollentelling?  Aan het begin van de zeventiende eeuw beheerste Spanje het territorium op welke continenten?
Aan het begin van de zeventiende eeuw beheerste Spanje het territorium op welke continenten?  Hoe zien we wat
Hoe zien we wat  Fakkels onderweg:testkit voor nanodeeltjes laat zien hoe nanodeeltjes van verschillende grootte zich in tumorweefsel verspreiden
Fakkels onderweg:testkit voor nanodeeltjes laat zien hoe nanodeeltjes van verschillende grootte zich in tumorweefsel verspreiden  Moslims worden in Canada vaak gediscrimineerd
Moslims worden in Canada vaak gediscrimineerd Welk apparaat zet zonne-energie om in elektrische energie?
Welk apparaat zet zonne-energie om in elektrische energie?  Wetenschappers ontdekken waarom vliegen zo moeilijk te meppen zijn
Wetenschappers ontdekken waarom vliegen zo moeilijk te meppen zijn  Wat is de snelheid van de duisternis als duisternis afwezig is, denk je dat duisternis.
Wat is de snelheid van de duisternis als duisternis afwezig is, denk je dat duisternis.
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

