
Wetenschap
Wat wordt gevormd als zwavel reageert met een metaal?
Hier is een uitsplitsing:
* metalen zijn elementen die de neiging hebben elektronen te verliezen en positief geladen ionen (kationen) vormen.
* zwavel is een niet -metaal dat de neiging heeft elektronen te winnen en negatief geladen ionen (anionen) vormt.
Wanneer een metaal en zwavel reageren, verliest het metaal elektronen aan de zwavel, waardoor een metaalkation en een sulfide -anion wordt gevormd. Deze ionen combineren vervolgens om een ionische verbinding te vormen die een sulfide wordt genoemd, .
Voorbeeld:
IJzer (Fe) reageert met zwavel (s) om ijzer te vormen (II) sulfide (FES):
FE + S → FES
Opmerking:
* Het specifieke type gevormde sulfide hangt af van het betrokken metaal en de reactieomstandigheden.
* Sommige sulfiden zijn oplosbaar in water, terwijl anderen dat niet zijn.
* Sulfiden hebben verschillende toepassingen, zoals in pigmenten, meststoffen en batterijen.
 Onderzoek identificeert het belangrijkste ingrediënt voor betaalbare brandstofcelkatalysatoren
Onderzoek identificeert het belangrijkste ingrediënt voor betaalbare brandstofcelkatalysatoren  Onderzoekers lokaliseren de grootste celreceptor van het lichaam
Onderzoekers lokaliseren de grootste celreceptor van het lichaam Welke variabelen beïnvloeden de pH-waarden?
Welke variabelen beïnvloeden de pH-waarden?  Ontwerpen van biologische beweging op nanometerschaal
Ontwerpen van biologische beweging op nanometerschaal Zelfassemblage in meerdere stappen opent de deur naar nieuwe herconfigureerbare materialen
Zelfassemblage in meerdere stappen opent de deur naar nieuwe herconfigureerbare materialen
 Arctische stormen:hoe wetenschappers de voorspellingen van gevaarlijke polaire dieptepunten verbeteren
Arctische stormen:hoe wetenschappers de voorspellingen van gevaarlijke polaire dieptepunten verbeteren Opinie:De ware schade van invasieve uitheemse soorten is zojuist onthuld in een baanbrekend rapport – hier is hoe we moeten handelen
Opinie:De ware schade van invasieve uitheemse soorten is zojuist onthuld in een baanbrekend rapport – hier is hoe we moeten handelen  Dodelijke instorting van de dam in Brazilië roept angst op voor milieuproblemen
Dodelijke instorting van de dam in Brazilië roept angst op voor milieuproblemen Wetgevers in Maryland keuren wetsvoorstel goed om de eerste staat in het land te worden die schuimvoedselcontainers verbiedt
Wetgevers in Maryland keuren wetsvoorstel goed om de eerste staat in het land te worden die schuimvoedselcontainers verbiedt Langdurige houtkapstudie toont de effecten op chimpansees en gorilla's in de Republiek Congo aan
Langdurige houtkapstudie toont de effecten op chimpansees en gorilla's in de Republiek Congo aan
Hoofdlijnen
- Hoe grootschalige eencellige genomica een aanvulling vormt op metagenomica-onderzoeken
- Van welk type weefsel is de baarmoeder gemaakt?
- Wat is de aard van onderzoek voor een paper?
- Wat zou er gebeuren als een cel geen ribosomen had?
Cellen zijn de kleinste functionele eenheden van alle levende wezens. In de cellen bevinden zich gespecialiseerde structuren, organellen genaamd, die ze helpen bepaalde functies uit te voeren. Rib
- Wat is een definitie van basis?
- Hoe laat transductie uw lichaam toe om zijn zintuigen te ervaren?
- Zeester zien:de ontbrekende schakel in de oogevolutie?
- Waarom leggen sommige vogelsoorten slechts één ei?
- Hoe noem je planten met dikke vlezige weefsels?
- Watermoleculen uit elkaar halen om schone brandstof te genereren:onderzoek naar een veelbelovend materiaal

- Nieuwe strategie zet evolutie van microscopische structuren in een stroomversnelling
- Stazakken van hernieuwbare grondstoffen en nanocellulose

- Chemische doorbraken openen nieuwe deuren voor medicijnontwikkelaars en kankeronderzoekers

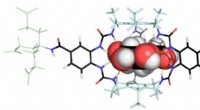
- Glucosebindend molecuul zou de behandeling van diabetes kunnen transformeren
 welke straalmachine?
welke straalmachine?  Wat is de maximale hoeveelheid elektronen die een atoom kan doneren en waarom?
Wat is de maximale hoeveelheid elektronen die een atoom kan doneren en waarom?  Welke twee metalen worden gebruikt om een legering te vormen?
Welke twee metalen worden gebruikt om een legering te vormen?  Major Landforms in de regio Southwest
Major Landforms in de regio Southwest Satelliet ziet tropische cycloon Vayu gecentreerd voor de kust van India
Satelliet ziet tropische cycloon Vayu gecentreerd voor de kust van India Welk percentage aardoppervlak is permafrost?
Welk percentage aardoppervlak is permafrost?  Eilanden op Titan kunnen eigenlijk bellenstromen zijn
Eilanden op Titan kunnen eigenlijk bellenstromen zijn Neolithische mens:de eerste houthakker?
Neolithische mens:de eerste houthakker?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

