
Wetenschap
Wat zijn de verschillen tussen het activeren en deactiveren van groepen in elektrofillische aromatische substitutie?
Activerende en deactiveren van groepen in elektrofiele aromatische substitutie
elektrofiele aromatische substitutie (EAS) is een fundamentele reactie in de organische chemie waarbij een elektrofiel een waterstofatoom op een aromatische ring vervangt. De reactiviteit van de aromatische ring wordt aanzienlijk beïnvloed door de al aanwezige substituenten. Deze substituenten zijn gecategoriseerd als activeren of deactivering Groepen op basis van hun effect op de snelheid van de reactie.
Groepen activeren Verhoog de elektronendichtheid van de aromatische ring, waardoor het gevoeliger is voor aanvallen door elektrofielen. Het zijn meestal elektronen-donerende groepen, die verder kunnen worden geclassificeerd:
* Sterke activerende groepen: Deze groepen zijn krachtige elektronendonoren en verhogen de snelheid van EA's aanzienlijk. Ze hebben meestal eenzame paar elektronen die rechtstreeks aan de ring kunnen doneren. Voorbeelden zijn:
* alkylgroepen (r-)
* -oH (hydroxylgroep)
* -nh2 (aminogroep)
* -or (alkoxygroep)
* -nr2 (dialkylamino-groep)
* Zwakke activerende groepen: Deze groepen zijn minder elektronen-donerend dan sterke activeringsgroepen, maar verhogen nog steeds de snelheid van EAS. Ze hebben meestal een dubbele binding of een PI -systeem dat kan deelnemen aan resonantie met de aromatische ring. Voorbeelden zijn:
* -CH =CH2 (vinylgroep)
* -c6h5 (fenylgroep)
deactiverende groepen Verminder de elektronendichtheid van de aromatische ring, waardoor deze minder reactief is in de richting van elektrofielen. Het zijn meestal elektronen-withending groepen, die kunnen worden geclassificeerd als:
* Sterke deactiverende groepen: Deze groepen zijn krachtige elektronenontbikkers en verlagen de snelheid van EA's aanzienlijk. Ze hebben een sterk elektronen-withending effect door resonantie en/of inductief effect. Voorbeelden zijn:
* -NO2 (Nitro Group)
* -So3H (sulfonzuurgroep)
* -cn (cyano-groep)
* -cooh (carbonzuurgroep)
* -cor (carbonylgroep)
* Zwakke deactiverende groepen: Deze groepen hebben een matig elektron-met-brandend effect en verminderen de snelheid van EA's in mindere mate dan sterke deactiverende groepen. Voorbeelden zijn:
* -x (halogenen:f, cl, br, i)
Belangrijkste verschillen:
| Feature | Groepen activeren | Deactiverende groepen |
| --- | --- | --- |
| elektronendichtheid | Verhoog de elektronendichtheid | De elektronendichtheid verlagen |
| Effect op EAS -snelheid | Verhoog de reactiesnelheid | De reactiesnelheid verlagen |
| elektronendonatie/intrekking | Elektronen-doneren | Elektronen-met-drawing |
| resonantie -effecten | Stabiliseercarbocatie -tussenproduct | Destabiliseercarbocatie -tussenproduct |
| Positie van substitutie | Ortho/para regie | Meta -regie |
belangrijke opmerkingen:
* ortho/para regie: Activerende groepen zijn over het algemeen ortho/para -richtingen. Dit betekent dat ze de inkomende elektrofiel naar de posities ortho en para naar zichzelf richten.
* meta -regie: Deactiverende groepen zijn over het algemeen meta -regie. Dit betekent dat ze de inkomende elektrofiel naar de positie -meta naar zichzelf sturen.
* halogenen (zwakke deactiveren): Halogenen zijn een speciaal geval. Hoewel ze elektron-met-drawing en deactiverend zijn, zijn ze nog steeds ortho/para-regie vanwege hun enige paren die deelnemen aan resonantie.
Inzicht in de effecten van het activeren en deactiveren van groepen is cruciaal voor het voorspellen van de reactiviteit en regioselectiviteit van elektrofiele aromatische substitutiereacties. Het helpt bij het effectief ontwerpen en synthetiseren van de gewenste producten.
Hoofdlijnen
- Wat is het primaire verschil in manier van nerveuze en endocriene systemen communiceren met hun doelcellen?
- Wie heeft echt DNA ontdekt?
- Wat is het Baader-Meinhof-fenomeen?
- Hoe heet een eenvoudig brein?
- Waarom is bioleaching en fytomining belangrijk?
- Welk orgel regelt alle andere lichaamssystemen?
- Hoe maanlicht de voortplanting van dieren afstemt
- Waar krijg je bacteriën?
- Wilde genen bij gedomesticeerde soorten:hoe we onze gewassen een boost kunnen geven met behulp van hun verre verwanten
- Nieuwe techniek om de ductiliteit van keramische materialen voor raketten te verbeteren, motoren

- Chemische verbindingen in voedingsmiddelen kunnen een belangrijk SARS-CoV-2-enzym remmen

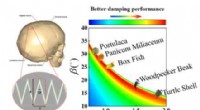
- De relatie tussen delicate hechtdraadstructuur en dempende prestaties van biomaterialen
- Gebruik van zonlicht om de toekomst te voeden via covalente organische raamwerken

- Gelijktijdige meting van biofysische eigenschappen en positie van afzonderlijke cellen in een microdevice

 Welke organel wordt aangetroffen in bloedcellen, geen menselijke cellen?
Welke organel wordt aangetroffen in bloedcellen, geen menselijke cellen?  Bosbranden, barbecueverboden:hittegolf verschroeit Europa
Bosbranden, barbecueverboden:hittegolf verschroeit Europa Wetenschap en wetenschappers hoog aangeschreven over de hele wereld:enquête
Wetenschap en wetenschappers hoog aangeschreven over de hele wereld:enquête Scheidingswanden:hoe immuuncellen weefsel binnendringen
Scheidingswanden:hoe immuuncellen weefsel binnendringen  Waarom u zich zorgen zou moeten maken over het Chinese optreden tegen VPN's
Waarom u zich zorgen zou moeten maken over het Chinese optreden tegen VPN's  Dit is waarom je internet binnenkort misschien door een drone wordt bezorgd
Dit is waarom je internet binnenkort misschien door een drone wordt bezorgd Zijn er naast de 8 bekende planeten nog andere planeten?
Zijn er naast de 8 bekende planeten nog andere planeten?  ESA vliegende ladingen op houten satelliet
ESA vliegende ladingen op houten satelliet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


