
Wetenschap
Hoe kun je zien of een aminozuur polair was?
1. Zoek naar elektronegatieve atomen:
* zuurstof (O) en stikstof (N) zijn zeer elektronegatieve atomen. Als de zijketen deze atomen bevat, zal deze waarschijnlijk polair zijn.
* zwavel (s) Kan ook bijdragen aan polariteit, hoewel in mindere mate.
2. Overweeg de aanwezigheid van functionele groepen:
* Hydroxylgroepen (-oH): Deze groepen zijn zeer polair en zullen het aminozuur polair maken.
* carboxylgroepen (-cooh): Deze groepen zijn ook polair en dragen bij aan de algehele polariteit van het aminozuur.
* amide-groepen (-conh2): Deze groepen zijn polair vanwege de elektronegatieve stikstof- en zuurstofatomen.
3. Onderzoek de structuur:
* opgeladen zijketens: Aminozuren met positieve of negatief geladen zijketens zijn altijd polair.
* Ongeladen maar polaire zijketens: Deze zijketens kunnen waterstofbruggen vormen met watermoleculen. Voorbeelden zijn serine, threonine, tyrosine, asparagine en glutamine.
Voorbeelden:
* Polaire aminozuren: Serine (OH), Threonine (OH), Asparagine (conh2), glutamine (conh2), lysine (NH3+), arginine (NH2+), histidine (NH+), aspartaat (COO-), glutamaat (COO-)
* Niet-polaire aminozuren: Alanine (CH3), Valine (CH (CH3) 2), leucine (CH2CH (CH3) 2), isoleucine (CH (CH3) CH2CH3), glycine (H), proline (cyclische structuur), fenylalanine (aromatische ring), tryptofan (aromatische ring), methionine (SCH3), cyste (SHION), cyste (sh) (sh) (sh) (sh) (sh) (sh) (sh).
Belangrijke opmerking: Het is cruciaal om te onthouden dat sommige aminozuren zowel polaire als niet-polaire componenten hebben. De algehele polariteit van het aminozuur hangt af van de dominante invloed van zijn zijketen. Cysteïne (SH) wordt bijvoorbeeld als niet-polair beschouwd vanwege het zwavelatoom, maar het kan disulfidebruggen vormen en met water interageren, wat bijdraagt aan sommige polaire eigenschappen.
Laat het me weten als je meer specifieke voorbeelden wilt of nog vragen hebt!
 Voedsel is belangrijk:gezonde voeding vergroot de economische en fysieke haalbaarheid van de doelstelling van 1,5°C
Voedsel is belangrijk:gezonde voeding vergroot de economische en fysieke haalbaarheid van de doelstelling van 1,5°C  Hoe evolutie de wetenschap ten goede kan veranderen
Hoe evolutie de wetenschap ten goede kan veranderen  Wat is een voorbeeld van concurrentie in ecologie?
Wat is een voorbeeld van concurrentie in ecologie?  Canada telt schade na Fiona; Cuba en Florida zetten zich schrap voor storm Ian
Canada telt schade na Fiona; Cuba en Florida zetten zich schrap voor storm Ian Wespen vliegen 's nachts
Wespen vliegen 's nachts
Hoofdlijnen
- Hoe gistformaties ontstonden
- Hoe een filmmaker, een stapel oude schelpen en een stel amateurs de oesterriffen van Australië terugbrengen
- Wat gebeurt er vlak voordat de transcriptie begint?
- Waar bestaan algemene sense -organen uit?
- Hoe bidsprinkhaankreeften de wereld begrijpen
- Het gebruik van pinguïns om de gezondheid van de oceaan te monitoren is mogelijk niet effectief
- Waarom is uw DNA 75 procent vergelijkbaar met die van een fruitvlieg?
- Een nieuw begrip van hoe cellen zichzelf verdedigen tegen bacteriële porievormende toxines
- De kleinste krachten opsporen:hoe T-cellen indringers detecteren
- Chemici ontwikkelen contaminantendetectietechniek voor heparine

- Techniek om functionele materialen te maken op basis van polymeren van metaalclusters
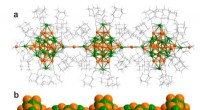
- Energie op aanvraag:leren van katalysatoren uit de natuur
- Team ontwikkelt machine met als doel een einde te maken aan textielverspilling

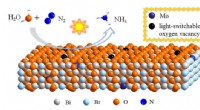
- Verbeterde fotosynthese van ammoniak in de omgeving met behulp van nanosheets met lichtschakelbare zuurstofvacatures
 Wat betekent CERN voor de toekomst van het universum?
Wat betekent CERN voor de toekomst van het universum?  Hoeveel gram melkzuur zit er in een 0,5M oplossing van zuur?
Hoeveel gram melkzuur zit er in een 0,5M oplossing van zuur?  Een niet-invasieve procedure maakt het mogelijk om archeologische informatie te verkrijgen zonder opgravingen
Een niet-invasieve procedure maakt het mogelijk om archeologische informatie te verkrijgen zonder opgravingen Kinderen betrekken bij het verduurzamen van scholen verspreidt de boodschap buiten het klaslokaal
Kinderen betrekken bij het verduurzamen van scholen verspreidt de boodschap buiten het klaslokaal Een arts die gespecialiseerd is in het diagnosticeren en behandelen van vormen van stralende energie staat bekend als?
Een arts die gespecialiseerd is in het diagnosticeren en behandelen van vormen van stralende energie staat bekend als?  Toegankelijke stages ondersteunen gelijkheid en diversiteit in techniek
Toegankelijke stages ondersteunen gelijkheid en diversiteit in techniek Wat is het macromolecuul van sprite?
Wat is het macromolecuul van sprite?  Vulkanen fungeerden als een veiligheidsklep voor het langetermijnklimaat van de aarde
Vulkanen fungeerden als een veiligheidsklep voor het langetermijnklimaat van de aarde
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

