
Wetenschap
Waarom neemt de massa magnesiumsulfaat af wanneer wordt verwarmd?
* gehydrateerd magnesiumsulfaat: Magnesiumsulfaat bestaat meestal als een hydraat, wat betekent dat er watermoleculen aan zijn kristalstructuur zijn bevestigd. Dit wordt vaak weergegeven als mgso₄ · xh₂o, waarbij "x" het aantal watermoleculen per formule -eenheid vertegenwoordigt.
* Uitdroging: Wanneer verwarmd, worden de watermoleculen in het gehydrateerde magnesiumsulfaat afgedreven als waterdamp. Dit proces wordt uitdroging genoemd .
* watervrij magnesiumsulfaat: Nadat het water is verwijderd, is de resterende vaste stof watervrij magnesiumsulfaat (MgSO₄). Aangezien watervrij magnesiumsulfaat een lager molecuulgewicht heeft dan de gehydrateerde vorm, lijkt het erop dat de massa is afgenomen. De afgegeven waterdamp gaat echter gewoon verloren door de atmosfeer, dus de totale massa blijft constant.
Samenvattend:
* De schijnbare Afname van de massa is te wijten aan het verlies van watermoleculen tijdens uitdroging.
* De werkelijke De massa blijft constant; De waterdamp ontsnapt eenvoudigweg in het milieu.
Belangrijke opmerking: Als de verwarming bij zeer hoge temperaturen wordt voortgezet, kan het watervrij magnesiumsulfaat verder ontleden, wat mogelijk leidt tot een afname van de massa. Dit is echter een apart proces dat optreedt bij veel hogere temperaturen dan typische uitdroging.
 Onderzoekers onderzoeken de oppervlakte-extractie van platinakatalysatoren in alkalische media
Onderzoekers onderzoeken de oppervlakte-extractie van platinakatalysatoren in alkalische media  Wat zijn fysisch-chemische eigenschappen die de basen gemeen hebben?
Wat zijn fysisch-chemische eigenschappen die de basen gemeen hebben?  Eenvoudige en snelle pH-experimenten met Litmus
Eenvoudige en snelle pH-experimenten met Litmus Waar gebruikte vroege Scientistis het proces van elektrolyse voor?
Waar gebruikte vroege Scientistis het proces van elektrolyse voor?  Berekening van de molaire warmtecapaciteit
Berekening van de molaire warmtecapaciteit
 Synchronisatie van ijskernen met behulp van vulkanische aslagen
Synchronisatie van ijskernen met behulp van vulkanische aslagen Studies in Bangladesh beschrijven hoe e-waste recycling werknemers blootstelt aan chemicaliën
Studies in Bangladesh beschrijven hoe e-waste recycling werknemers blootstelt aan chemicaliën Biochar kan niet-duurzaam veenmos in de glastuinbouw vervangen
Biochar kan niet-duurzaam veenmos in de glastuinbouw vervangen Wereld gewaarschuwd:verander nu of breng voedsel en klimaat in gevaar
Wereld gewaarschuwd:verander nu of breng voedsel en klimaat in gevaar Achteruitgang van het platteland niet gedreven door waterterugwinning
Achteruitgang van het platteland niet gedreven door waterterugwinning
Hoofdlijnen
- Ondersteuning van de vorm van een hele cel?
- Wordt uw huisdier blootgesteld aan passief roken? Dit zijn de (ernstige) gezondheidsrisico’s
- In welk koninkrijk is sporen?
- Onderzoeken waarom cellen regelmatige geometrische patronen vormen
- Is het waar dat sommige bacteriën geen ziekteverwekkers zijn?
- Wat is de symbiotische relatie tussen mug en mensen?
- Wat is een voorbeeld van een kanaaleiwit?
- Welke psycholoog zei nog dat wat we bereiken te wijten is aan de samenstelling van onze genen?
- Waarom produceren gymnospermen en angiospermen pollenzaden?
- Techniek verdubbelt conversie van CO2 naar plastic component

- Klimaat terugspoelen:wetenschappers zetten koolstofdioxide weer om in steenkool

- Ingenieurs lossen mysterie op van de relatie tussen structuur en eigenschappen in katalysatoren voor emissiebeheersing
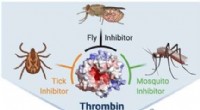
- Krachtige trivalente remmers van trombine uit antistollingspeptiden in speeksel van insecten
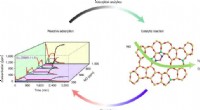
- Verbetering van condensatie:op weg naar praktische energie- en watertoepassingen

 Een ongemakkelijke waarheid over een ongemakkelijke waarheid
Een ongemakkelijke waarheid over een ongemakkelijke waarheid Onderzoeker bestudeert effecten van wind nabij het oppervlak op landschapsevolutie
Onderzoeker bestudeert effecten van wind nabij het oppervlak op landschapsevolutie Hoeveel gram appelmoes in één beker?
Hoeveel gram appelmoes in één beker?  Lobbyen of groene innovatie? Wat beschermt bedrijven tegen het risico van klimaatverandering?
Lobbyen of groene innovatie? Wat beschermt bedrijven tegen het risico van klimaatverandering?  Klimaatverandering, bosverlies en branden:wetenschappers leggen uit hoe Amazon vastzit in een vicieuze cirkel
Klimaatverandering, bosverlies en branden:wetenschappers leggen uit hoe Amazon vastzit in een vicieuze cirkel  Wanneer een organisme zichzelf op iets anders laat lijken om te overleven?
Wanneer een organisme zichzelf op iets anders laat lijken om te overleven?  Onderzoekers bestuderen historische ontwikkelingen van het periodiek systeem van chemische elementen
Onderzoekers bestuderen historische ontwikkelingen van het periodiek systeem van chemische elementen Wat gebeurt er met de opbrengst aan zwaveltrioxide als je de druk verhoogt en verlaagt?
Wat gebeurt er met de opbrengst aan zwaveltrioxide als je de druk verhoogt en verlaagt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

