
Wetenschap
Welk type reactie is 2KCLO3 plus 3s ---- 2KCl 3SO2?
De reactie die u hebt gegeven is een redox -reactie .
Dit is waarom:
* oxidatie: Zwavel (s) gaat van een oxidatietoestand van 0 in elementaire zwavel naar +4 in zwaveldioxide (SO2). Dit is een toename van de oxidatietoestand, wat betekent dat zwavel wordt geoxideerd.
* reductie: Chloor (CL) gaat van een oxidatietoestand van +5 in kaliumchloraat (KCLO3) naar -1 in kaliumchloride (KCL). Dit is een afname van de oxidatietoestand, wat betekent dat chloor wordt verminderd.
Daarom omvat de reactie zowel oxidatie als reductie, waardoor het een redox -reactie is.
Laat het me weten als je een meer gedetailleerde uitleg van oxidatietoestanden wilt of andere soorten chemische reacties wilt verkennen!
 Hoe effectieve nucleaire kosten te berekenen
Hoe effectieve nucleaire kosten te berekenen  Is CH4 een niet-polaire covalente binding?
Is CH4 een niet-polaire covalente binding?  Vier vormen van energie die kunnen worden geabsorbeerd of vrijgegeven tijdens een chemische reactie?
Vier vormen van energie die kunnen worden geabsorbeerd of vrijgegeven tijdens een chemische reactie?  What Is Bacteria Homeostasis?
What Is Bacteria Homeostasis?  Hoe veranderende laboratoria een chemische reactie onthulden die sleutel is tot de vorming van cataract
Hoe veranderende laboratoria een chemische reactie onthulden die sleutel is tot de vorming van cataract
 De grootste verscheidenheid aan klimaten wordt gevonden in welke regio?
De grootste verscheidenheid aan klimaten wordt gevonden in welke regio?  Nieuwe studie heeft aangetoond dat chemische dispergeermiddelen in de diepzee niet effectief zijn bij olieramp in Deepwater Horizon
Nieuwe studie heeft aangetoond dat chemische dispergeermiddelen in de diepzee niet effectief zijn bij olieramp in Deepwater Horizon Concurrerende Colorado River-plannen laten zien dat zeven staten het niet eens kunnen worden over de manier waarop ze de kritieke watervoorziening moeten beheren
Concurrerende Colorado River-plannen laten zien dat zeven staten het niet eens kunnen worden over de manier waarop ze de kritieke watervoorziening moeten beheren  Hebben varens chloroplast erin?
Hebben varens chloroplast erin?  IJs is een reddingslijn voor 's werelds koudste regio
IJs is een reddingslijn voor 's werelds koudste regio
Hoofdlijnen
- Onderzoekers vinden dat er minstens 14, 003 plantensoorten in het Amazonebekken
- Waarom de wetenschap niet helpt bij het verkopen van chocoladekoekjes
- Wat kan er worden geërfd?
- Kleine eiwitten spelen grote rol in cellulaire energiebalans
- Waar worden eiwitten in de cel gebouwd?
- Wat is een mutatie en waarom zijn mutaties belangrijk in evolutie?
- Wat zijn halfgeleiders?
- Hoe weet het lichaam hoe hij mRNA moet produceren?
- Hoeveel spieren heb je nodig om te glimlachen?
- Uitbreidbaar schuim voor 3D-printen van grote objecten

- Elementen in planten gebruiken om de efficiëntie van de brandstofcel te verhogen en tegelijkertijd de kosten te verlagen

- Stampede2, Bridges-simulaties tonen zwakke plekken in Ebola-virus nucleocapsid

- de tijdloze, complementaire smaak van oesters en champagne - uitgelegd

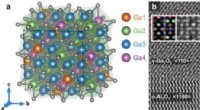
- Galliumoxidekristalcomplexiteit getemd door machine learning
 Kunnen oesters worden gebruikt om Chesapeake Bay schoon te maken?
Kunnen oesters worden gebruikt om Chesapeake Bay schoon te maken?  Regionale scenario's op zeeniveau helpen het noordoosten bij het plannen van een snellere dan wereldwijde stijging
Regionale scenario's op zeeniveau helpen het noordoosten bij het plannen van een snellere dan wereldwijde stijging Wat is het verschil tussen een homogeen en heterogeen mengsel?
Wat is het verschil tussen een homogeen en heterogeen mengsel?  Video:lancering van Sentinel-2B
Video:lancering van Sentinel-2B Grote delen van het Braziliaanse regenwoud dreigen hun bescherming te verliezen
Grote delen van het Braziliaanse regenwoud dreigen hun bescherming te verliezen Als de trillingsfrequentie op aarde n is, zal de maan dat ook zijn?
Als de trillingsfrequentie op aarde n is, zal de maan dat ook zijn?  Kleverige elektronen:wanneer afstoting verandert in aantrekking
Kleverige elektronen:wanneer afstoting verandert in aantrekking Ingenieurs laten zien dat licht een wip kan spelen op nanoschaal
Ingenieurs laten zien dat licht een wip kan spelen op nanoschaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

