
Wetenschap
Wat zou er gebeuren als het volume gas afnam en vervolgens zou worden verhoogd?
Volume afnemen
* Drukverhoging: Wanneer u het volume van een gas vermindert terwijl u de temperatuur constant houdt, hebben de gasmoleculen minder ruimte om te bewegen. Dit leidt tot frequentere botsingen met de containerwanden, wat resulteert in een toename van de druk. Zie het als het knijpen van een ballon - de lucht binnen wordt gecomprimeerd en duwt harder tegen de ballon.
* Dichtheidsverhoging: Omdat dezelfde hoeveelheid gas nu in een kleinere ruimte wordt verpakt, neemt de dichtheid van het gas toe. Er zijn meer gasmoleculen per volume -eenheid.
Verhogend volume
* Drukafname: Wanneer u het volume van het gas verhoogt, hebben de moleculen meer ruimte om te bewegen. Dit leidt tot minder botsingen met de containerwanden, wat resulteert in een afname van de druk. Zoals lucht uit een ballon laten, daalt de druk binnen.
* Dichtheid afnemen: Naarmate het gas zich uitbreidt, wordt dezelfde hoeveelheid gas verspreid over een groter volume, waardoor de dichtheid lager wordt.
Sleutelpunten:
* de wet van Boyle: Deze relatie tussen volume en druk voor een gas wordt beschreven door de wet van Boyle, waarin staat dat de druk van een gas omgekeerd evenredig is met het volume bij constante temperatuur.
* Temperatuur: We gaan ervan uit dat de temperatuur in dit scenario constant blijft. Als de temperatuur verandert, wordt de relatie tussen volume en druk complexer.
* Real-World voorbeeld: Stel je een fietspomp voor. Wanneer u op het handvat naar beneden duwt, vermindert u het volume lucht binnen, waardoor de druk toeneemt, waardoor de lucht vervolgens in de band dwingt.
Samenvattend:
Het verminderen van het volume van een gas verhoogt de druk en dichtheid ervan. Het verhogen van het volume van een gas vermindert de druk en de dichtheid. Deze relatie wordt beheerst door de wet van Boyle en is van fundamenteel belang voor het begrijpen van het gedrag van gassen.
 Een materiaal met een bijzondere twist:2-D molybdeendiselenidekristal
Een materiaal met een bijzondere twist:2-D molybdeendiselenidekristal Waarom verandert de hoeveelheid waterdamp altijd?
Waarom verandert de hoeveelheid waterdamp altijd?  Goede en slechte effecten van fysisch-chemische verandering?
Goede en slechte effecten van fysisch-chemische verandering?  Nieuwe methode voor nauwkeurigere bepaling van het tijdstip van overlijden op plaats delict
Nieuwe methode voor nauwkeurigere bepaling van het tijdstip van overlijden op plaats delict Een goedkope vervanger voor duur metaal in een industrieel gebruikelijke chemische reactie
Een goedkope vervanger voor duur metaal in een industrieel gebruikelijke chemische reactie
 Gebeiteld in steen? Kooldioxide omzetten in steen, voor goed
Gebeiteld in steen? Kooldioxide omzetten in steen, voor goed Waarom plastic tassen zo moeilijk te verwijderen zijn
Waarom plastic tassen zo moeilijk te verwijderen zijn Wildvuur in West-Australië verbrandt meer huizen bij droge wind
Wildvuur in West-Australië verbrandt meer huizen bij droge wind Hebben Black Lives Matt-protesten invloed op dodelijke politie-interacties en misdaad?
Hebben Black Lives Matt-protesten invloed op dodelijke politie-interacties en misdaad?  Zullen recente stormen Californië redden van een brutaal brandseizoen?
Zullen recente stormen Californië redden van een brutaal brandseizoen?
Hoofdlijnen
- Laboratoriumexperimenten met hoge resolutie laten zien hoe cellen 'eten'
- Wat zijn de soorten dichte bindweefsels?
- Granaatappelkracht:duurzame antimicrobiële oplossingen uit schillen ontsluiten
- Hoe evolutie werkt
- Waarom worden experimenten waarbij transplanterende soorten worden uitgevoerd die vandaag zelden worden uitgevoerd?
- Tandheelkundig bewijs daagt de oorsprongstijd van zoogdieren uit
- Wetenschappers laten zien hoe DNA-reparaties het genoom kunnen hervormen
- Onderzoekers ontdekken de echte reden waarom schildpadden schelpen hebben
- Vraag en antwoord:Hoe je duurzame producten sneller kunt maken met kunstmatige intelligentie en automatisering
- Machine learning-model voorspelt fenomeen dat essentieel is voor het begrijpen van materiaaleigenschappen

- Biosensor maakt realtime zuurstofmonitoring mogelijk voor organen-op-een-chip

- Een hydrogel die stevig hecht aan kraakbeen en meniscus

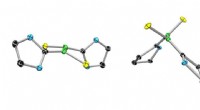
- Generatie van een stabiel biradicaal
- Studie onthult geheim 18e-eeuws portret

 Onderzoekers leggen uit hoe wanorde kwantumspinvloeistoffen verandert en een nieuwe fase van materie vormt
Onderzoekers leggen uit hoe wanorde kwantumspinvloeistoffen verandert en een nieuwe fase van materie vormt  Zonneverdamper biedt een frisse route naar zoet water
Zonneverdamper biedt een frisse route naar zoet water Geef het door:werk-privéadvies van de curator van Twitter
Geef het door:werk-privéadvies van de curator van Twitter Wat is het derde deel van nucleotiden?
Wat is het derde deel van nucleotiden?  Een rots op goud testen
Een rots op goud testen Een-nm dikke grafeenmotor bootst tweetaktmotor na
Een-nm dikke grafeenmotor bootst tweetaktmotor na Een kwantumthermometer om de koudste temperaturen in het heelal te meten (update)
Een kwantumthermometer om de koudste temperaturen in het heelal te meten (update) Haaienaanvallen nemen wereldwijd toe, zegt onderzoek:hoe vaak komen ze voor in Californië?
Haaienaanvallen nemen wereldwijd toe, zegt onderzoek:hoe vaak komen ze voor in Californië?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

