
Wetenschap
Hoe wordt de gaswet van toepassing op vacuümverdamper?
1. Dalton's wet van gedeeltelijke druk:
* Verdampingsdrijfkracht: De wet van Dalton stelt dat de totale druk van een gasmengsel de som is van de gedeeltelijke druk van zijn individuele componenten. In een vacuümverdamper is de gedeeltelijke druk van het verdampte oplosmiddel boven het vloeibare oppervlak belangrijk. Het verlagen van de totale druk in de verdamper door een vacuüm te creëren, vermindert direct de partiële druk van de oplosmiddeldamp, waardoor de verdampingssnelheid wordt verbeterd.
2. Ideale gaswet (PV =NRT):
* Dampdruk en temperatuur: De ideale gaswet relateert druk, volume, temperatuur en het aantal mol gas. In een vacuümverdamper, naarmate de temperatuur van de vloeistof toeneemt, neemt de dampdruk van het oplosmiddel ook toe. Dit leidt tot een hogere verdampingssnelheid.
* Vacuümsysteemontwerp: De ideale gaswet helpt het vereiste vacuümniveau en systeemcapaciteit te bepalen. Hiermee kunnen ingenieurs het volume damp berekenen dat wordt geproduceerd bij een bepaalde temperatuur en druk, helpt bij de selectie van pompen en vacuümkamergroottes.
3. Graham's Diffusion Law:
* Dampverwijdering: Deze wet stelt dat de diffusiesnelheid van een gas omgekeerd evenredig is met de vierkantswortel van zijn molecuulgewicht. Lichte moleculen, zoals waterdamp, diffunderen sneller dan zwaardere. In een vacuümverdamper berust een efficiënte verwijdering van het verdampte oplosmiddel op dit principe. Het vacuümsysteem is ontworpen om het verdampte oplosmiddel snel uit de kamer te verwijderen, waardoor het geen verzadiging bereikt en verdere verdamping belemmert.
4. Raoult's Law:
* Volatiliteit van oplosmiddelen: Deze wet regelt de dampdruk van een oplossing. Het stelt dat de partiële druk van een oplosmiddel boven een oplossing gelijk is aan de dampdruk van het zuivere oplosmiddel vermenigvuldigd met zijn molfractie in de oplossing. In een vacuümverdamper heeft de volatiliteit van het oplosmiddel direct invloed op zijn verdampingssnelheid. Zeer vluchtige oplosmiddelen, zoals ethanol, verdampen gemakkelijk bij lagere druk, terwijl minder vluchtige oplosmiddelen hogere temperaturen en/of lagere drukken vereisen.
5. Toepassingen in vacuümverdamping:
* voedselverwerking: Vacuümverdampers worden gebruikt om vruchtensappen, melk en andere voedselproducten te concentreren met behoud van hun smaak en voedingsstoffen. Gaswetten bepalen het verdampingspercentage en helpen de consistentie van het eindproduct te beheersen.
* chemische verwerking: Veel industriële processen zijn afhankelijk van vacuümverdamping om oplosmiddelen van oplossingen te scheiden of om materialen te concentreren. Inzicht in de gaswetten maakt een efficiënte optimalisatie van deze processen mogelijk.
* Farmaceutische productie: Vacuümverdampers zijn cruciaal voor het isoleren en zuiveren van actieve ingrediënten in de farmaceutische productie. De gecontroleerde omgeving en precieze temperatuurregeling, geleid door gaswetten, zorgen voor productkwaliteit.
Samenvattend is het begrijpen van gaswetten essentieel voor het ontwerpen, bedienen en optimaliseren van vacuümverdampers. Deze wetten helpen bij het bepalen van de verdampingssnelheid, regelen het vacuümniveau en zorgen voor een efficiënte verwijdering van het verdampte oplosmiddel, wat bijdraagt aan de effectiviteit en efficiëntie van het totale proces.
 Maak kennis met de made:hoe dit vleesminnende, kontademende wonder ons helpt moorden op te lossen
Maak kennis met de made:hoe dit vleesminnende, kontademende wonder ons helpt moorden op te lossen  Laat het sneeuwen:onderzoekers testen cloud seeding
Laat het sneeuwen:onderzoekers testen cloud seeding Glasvezelkabel bewaakt microseismiciteit op Antarctica
Glasvezelkabel bewaakt microseismiciteit op Antarctica Vervuiling door mijnen beperkt de toegang tot schoon water in Papoea-Nieuw-Guinea
Vervuiling door mijnen beperkt de toegang tot schoon water in Papoea-Nieuw-Guinea Nieuwe software 'leert' computers hoe ze schoonheid kunnen identificeren
Nieuwe software 'leert' computers hoe ze schoonheid kunnen identificeren
Hoofdlijnen
- Informatieverwerking beperkt de manier waarop E. coli-bacteriën door chemische gradiënten navigeren
- Welke rol speelt een kikker in het ecosysteem?
- Hoeveel dennen met bloed bevat het menselijk lichaam?
- Bijen vertonen geavanceerde leervaardigheden
- Wat is een hypothesevariabele?
- Wat zijn de bouwstenen van DNA en RNA?
- Studie werpt nieuw licht op hoe dieren en planten reageren op veranderingen in de omgeving
- Wat maakt eiwitten driedimensionaal?
- Ongebreidelde bosbranden hebben ooit geleid tot wereldwijde massale uitsterving, zeggen wetenschappers. Kan het nog een keer gebeuren?
- Team ontwikkelt adhesiesysteem voor meerdere oppervlakken, gemodelleerd naar sprinkhanenvoeten

- Opvallen:ongebruikelijke magnetische overgang in perovskietoxide kan spintronica helpen stimuleren
- Onderzoekers ontwikkelen test van 15 minuten om immuunrespons te beoordelen

- Wetenschappers ontwikkelen lijm met industriële sterkte die kan worden losgemaakt in een magnetisch veld

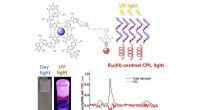
- Lichtgevende gels voor een groot aantal toepassingen, van namaak tot bio-sensing
 Hoe bouwimplosies werken
Hoe bouwimplosies werken  Onderzoekers ontwikkelen grafeen nano-pincetten die individuele biomoleculen kunnen grijpen
Onderzoekers ontwikkelen grafeen nano-pincetten die individuele biomoleculen kunnen grijpen Voordelen van herstellend plasma voor COVID-19 zijn nog onduidelijk
Voordelen van herstellend plasma voor COVID-19 zijn nog onduidelijk Wat is het verschil tussen fruit en zaad?
Wat is het verschil tussen fruit en zaad?  Ontbossing vernietigde 8% van Amazon in 18 jaar:studie
Ontbossing vernietigde 8% van Amazon in 18 jaar:studie Touchibo, een robot die door middel van aanraking inclusie in het onderwijs bevordert
Touchibo, een robot die door middel van aanraking inclusie in het onderwijs bevordert  Rozen zijn rood – waarom sommige petunia’s blauw zijn
Rozen zijn rood – waarom sommige petunia’s blauw zijn  Hoe NZ een wereldleider kan worden in decarbonisatie met behulp van bosbouw en geothermische technologie
Hoe NZ een wereldleider kan worden in decarbonisatie met behulp van bosbouw en geothermische technologie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

