
Wetenschap
Als er 3 mol waterstof 6 zuurstof en 9 helium in een vaartuig van 10 l bij 27 graden zijn, zal het totale drukgasmengsel zijn?
Hier leest u hoe u de totale druk van het gasmengsel kunt berekenen:
1. Converteer de temperatuur naar Kelvin
* T (k) =t (° C) + 273.15
* T (k) =27 ° C + 273.15 =300,15 k
2. Bereken de totale mol gas
* Totale mol =mol waterstof + mol zuurstof + mol helium
* Totale mol =3 + 6 + 9 =18 mol
3. Gebruik de ideale gaswet
* Pv =nrt
* P =druk (wat we willen vinden)
* V =volume (10 l)
* n =aantal mol (18 mol)
* R =ideale gasconstante (0,0821 l · atm/mol · k)
* T =temperatuur (300,15 K)
4. Oplossen voor druk
* P =(nrt) / v
* P =(18 mol * 0,0821 l · atm / mol · k * 300,15 k) / 10 l
* P ≈ 44.5 ATM
Daarom is de totale druk van het gasmengsel in het vat ongeveer 44,5 atmosferen.
 Waarom is een oplossing van aluminiumchloride zuurder dan natriumchloride?
Waarom is een oplossing van aluminiumchloride zuurder dan natriumchloride?  Wat is het mechanische chemische of nucleaire mechanische water?
Wat is het mechanische chemische of nucleaire mechanische water?  Op koolstof gebaseerde katalysatoren die worden gebruikt voor Fischer-Tropsch-synthese
Op koolstof gebaseerde katalysatoren die worden gebruikt voor Fischer-Tropsch-synthese Tijdmachine biedt nieuwe aanpak voor het testen van geneesmiddelen voor alvleesklierkanker
Tijdmachine biedt nieuwe aanpak voor het testen van geneesmiddelen voor alvleesklierkanker Hoe de pH te bepalen van pKa
Hoe de pH te bepalen van pKa
Hoofdlijnen
- Wat is de chemische formule van creatinekinase?
- Hoe betrouwbaar is de DNA-test van uw hond?
- De Krebs-cyclus en de Homeostasis
- Hoe zwemmen waterschimmelsporen?
- Hoe ademen vogels beter? De ontdekking van onderzoekers zal je voor de gek houden
- Chimpansees in gevangenschap vertonen tekenen van een aangetaste geestelijke gezondheid
- Welke organel biedt ondersteuning voor kleine planten?
- Wat is het molecuulgewicht van glucoseoxidase?
- De cel voert zijn normale functies uit tijdens.?
- Fluorescerende breathalyzer maakt optimalisatie van katalysatoren veel gemakkelijker
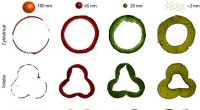
- Franse wetenschappers beweren metallische waterstof te hebben gemaakt
- Video:Waarom plastic flessen worden gerecycled tot kleding

- een medicijn, veel ziekten

- Machine learning kraakt de oxidatietoestanden van kristalstructuren

 Wat is de reactie tussen kaliumdichromaat en natriumthiosulfaat?
Wat is de reactie tussen kaliumdichromaat en natriumthiosulfaat?  Nieuw onderzoek identificeert de sterke en zwakke punten van supermateriaal
Nieuw onderzoek identificeert de sterke en zwakke punten van supermateriaal Commercieel ruimteschip klaar voor maanlanding, als test voor de Amerikaanse industrie
Commercieel ruimteschip klaar voor maanlanding, als test voor de Amerikaanse industrie  Wat is een coëfficiënt in een chemische formule?
Wat is een coëfficiënt in een chemische formule?  Waarom de batterij van uw laptop u niet zal doden
Waarom de batterij van uw laptop u niet zal doden  Onderzoekers identificeren hoe bacterie overleeft in zuurstofarme omgevingen
Onderzoekers identificeren hoe bacterie overleeft in zuurstofarme omgevingen Het ladingspompen en ontspannen van de chirale anomalie in een Dirac-halfmetaal begrijpen
Het ladingspompen en ontspannen van de chirale anomalie in een Dirac-halfmetaal begrijpen Halverwege voor NOEMA constructie
Halverwege voor NOEMA constructie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

