
Wetenschap
Waarom slaat chemische binding de meeste energie op?
* Energie wordt opgeslagen in de opstelling van atomen: Chemische bindingen vertegenwoordigen een stabiele opstelling van atomen die bij elkaar worden gehouden door elektrostatische krachten. Deze opstelling heeft lagere energie dan de individuele, ongebonden atomen.
* Energie wordt vrijgegeven wanneer bindingen worden verbroken: Om een chemische binding te verbreken, moet je energie doen om de aantrekkelijke krachten te overwinnen die de atomen bij elkaar houden. Wanneer de binding breekt, wordt de energie die u erin legt vrijgegeven, vaak als warmte of licht.
Denk er zo aan: Stel je een rots voor op een heuvel. De rots heeft potentiële energie vanwege zijn positie. Als je de rots door de heuvel duwt, krijgt het kinetische energie en laat het potentiële energie vrij. Evenzo slaan chemische bindingen potentiële energie op bij de opstelling van hun atomen. Het doorbreken van de binding geeft deze potentiële energie vrij.
sterkere bindingen vereisen meer energie om te breken: Sterkere bindingen, zoals die in moleculen met meerdere bindingen (dubbele of drievoudige bindingen), of bindingen tussen zeer elektronegatieve atomen, vereisen meer energie om te breken en daarom meer energie vrij te geven wanneer ze breken.
Samenvattend:
* Chemische bindingen slaan de meeste energie niet op in de zin van vasthouden aan een grote hoeveelheid energie.
* De energie die is opgeslagen in een chemische binding is de potentiële energie van de opstelling van atomen.
* breken Chemische bindingen geven deze potentiële energie vrij. Hoe sterker de binding, hoe meer energie wordt vrijgegeven bij het breken.
 Welke kleurverandering treedt op als fenolftaleïne in de base wordt gebracht?
Welke kleurverandering treedt op als fenolftaleïne in de base wordt gebracht?  Waarom moeten chemische vergelijkingen in evenwicht zijn?
Waarom moeten chemische vergelijkingen in evenwicht zijn?  Neutronen vangen vormveranderend coronavirus-eiwitcomplex op heterdaad
Neutronen vangen vormveranderend coronavirus-eiwitcomplex op heterdaad De lading van een in een vakbond verenigd atoom is?
De lading van een in een vakbond verenigd atoom is?  Innovatieve nanosensor voor ziektediagnose
Innovatieve nanosensor voor ziektediagnose
Hoofdlijnen
- Wat is de oorsprong van het woord vadom?
- Welk weefsel vormt de aveoli?
- Is parasitisme een vorm van symbiose?
- Is Magic Mushroom een natuurlijke vorm van zuur?
- Wat is de rol van rodopsinen bij mensen met kegeltjes?
- Een genetische trigger voor de Cambrische explosie ontrafeld?
- Cryo-EM-beeldvorming suggereert hoe de dubbele helix scheidt tijdens replicatie
- Wat hebben organismen nodig om zich voort te planten?
- Kunstmatige intelligentie kan worden gebruikt om bossen in Maines beter te monitoren, vondsten te bestuderen
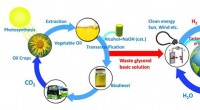
- Van een bijproduct van de biodieselindustrie tot duurzame productie van een waardevolle chemische stof
- Ingenieurs onthullen moleculaire geheimen van de krachten van koppotigen

- Spinzijde kan worden gebruikt als robotspier

- Nieuw NIST-onderzoek kan de kosten van het maken van stuivers verlagen

- Wetenschappers ontwikkelen efficiënte methode om zeer sterke materialen te maken voor flexibele elektronica

 Kajakkers vinden gedeeltelijk versteende berenschedel in Kansas
Kajakkers vinden gedeeltelijk versteende berenschedel in Kansas Wat je op school niet hebt geleerd over seksuele gezondheid
Wat je op school niet hebt geleerd over seksuele gezondheid Met welke kracht trekt de zwaartekracht aan een hoeveelheid materie die we noemen?
Met welke kracht trekt de zwaartekracht aan een hoeveelheid materie die we noemen?  Meest complexe nanodeeltjeskristal ooit gemaakt door ontwerp
Meest complexe nanodeeltjeskristal ooit gemaakt door ontwerp Er zijn aanwijzingen dat de opwarming van de aarde een negatief effect kan hebben op sommige overheidsmedewerkers
Er zijn aanwijzingen dat de opwarming van de aarde een negatief effect kan hebben op sommige overheidsmedewerkers Mendelejev combineerde de ideeën van twee eerdere wetenschappers:wie waren zij en wat deden zij?
Mendelejev combineerde de ideeën van twee eerdere wetenschappers:wie waren zij en wat deden zij?  Hoe kunnen we ervoor zorgen dat woningbouwprojecten met een hogere dichtheid nog steeds voldoende ruimte bieden voor de recreatiebehoeften van de bewoners?
Hoe kunnen we ervoor zorgen dat woningbouwprojecten met een hogere dichtheid nog steeds voldoende ruimte bieden voor de recreatiebehoeften van de bewoners?  Ford onthult nieuwste Mustang, waarmee de levensduur van benzinemotoren wordt verlengd
Ford onthult nieuwste Mustang, waarmee de levensduur van benzinemotoren wordt verlengd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

