
Wetenschap
Waarom is stikstof veel minder reactief dan zuurstof?
Eén reden is dat stikstof een drievoudige binding tussen zijn atomen heeft, terwijl zuurstof een dubbele binding heeft. Dit betekent dat het stikstofmolecuul veel stabieler is dan het zuurstofmolecuul, en dat het meer energie kost om de stikstofbinding te verbreken dan de zuurstofbinding. Deze hogere bindingsenergie betekent dat stikstof minder snel reageert met andere elementen.
Een andere reden waarom stikstof minder reactief is, is dat het een hogere ionisatie-energie heeft dan zuurstof. Dit betekent dat het meer energie kost om een elektron uit een stikstofatoom te verwijderen dan uit een zuurstofatoom. Deze hogere ionisatie-energie zorgt er ook voor dat stikstof minder snel reageert met andere elementen.
Ten slotte is stikstof een niet-polair molecuul, terwijl zuurstof een polair molecuul is. Dit betekent dat stikstof geen gedeeltelijk positieve lading of gedeeltelijk negatieve lading heeft, terwijl zuurstof dat wel heeft. Dit gebrek aan polariteit zorgt ervoor dat stikstof minder snel reageert met andere elementen.
 Nieuwe methode om het comfort van slim en functioneel textiel te evalueren
Nieuwe methode om het comfort van slim en functioneel textiel te evalueren Wat zijn de niet-Welke van deze is geen type chemische binding?
Wat zijn de niet-Welke van deze is geen type chemische binding?  Polymere membranen gebruiken om industriële scheidingen op te ruimen
Polymere membranen gebruiken om industriële scheidingen op te ruimen Rekbare plastic elektrolyten kunnen een nieuw ontwerp van lithium-ionbatterijen mogelijk maken
Rekbare plastic elektrolyten kunnen een nieuw ontwerp van lithium-ionbatterijen mogelijk maken Hulp nodig bij wetenschappelijk huiswerk. Heeft iemand deze vraag beantwoord. Zijn de veranderingen van a naar b en c fysisch of chemisch verklaren uw antwoord?
Hulp nodig bij wetenschappelijk huiswerk. Heeft iemand deze vraag beantwoord. Zijn de veranderingen van a naar b en c fysisch of chemisch verklaren uw antwoord?
 Superdiepe diamanten bevestigen het oude reservoir diep onder het aardoppervlak
Superdiepe diamanten bevestigen het oude reservoir diep onder het aardoppervlak Klimaatverandering, houtkap botst - en een bos krimpt
Klimaatverandering, houtkap botst - en een bos krimpt Voorspellingen ijsbedekking Grote Meren:nieuwe aanpak maakt lokale voorspellingen mogelijk
Voorspellingen ijsbedekking Grote Meren:nieuwe aanpak maakt lokale voorspellingen mogelijk 80% van het huishoudelijk water wordt verspild
80% van het huishoudelijk water wordt verspild NASA zag de eens orkaan Aletta intensiveren, nu snel aan het verzwakken
NASA zag de eens orkaan Aletta intensiveren, nu snel aan het verzwakken
Hoofdlijnen
- Het belang van diffusie in organismen
- Cross-species cellandschap gebouwd op eencellig niveau
- Een nieuw mechanisme voor hoe dierlijke cellen intact blijven
- Verander je geliefde in een boom met Bios Urn
- Noemen olifanten 'mensen!'?
- Een biobank van omkeerbare mutante embryonale stamcellen
- Hoe hersendood werkt
- Hoe de cellen van planten, dieren en eencellige organismen te vergelijken
- Kunnen nieuwe kankermedicijnen uit aardappelen en tomaten komen?
- Een bioplastic dat beschermt tegen UV-straling

- Onderzoekers infuseren bacteriën met zilver om de energie-efficiëntie in brandstofcellen te verbeteren

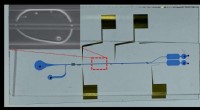
- Microfluïdisch systeem met celscheidende krachten kan ontrafelen hoe nieuwe pathogenen aanvallen
- Atomaire afstemming op kobalt maakt een achtvoudige toename van de productie van waterstofperoxide mogelijk

- Nieuwe technologie kan antivirusantilichamen in 20 minuten detecteren

 Preprints:hoe concept-academische papers essentieel zijn geworden in de strijd tegen COVID
Preprints:hoe concept-academische papers essentieel zijn geworden in de strijd tegen COVID  3 innovaties helpen daklozen in Eugene, Oregon
3 innovaties helpen daklozen in Eugene, Oregon Snowpack Californië meet laag, maar er komen grote stormen aan
Snowpack Californië meet laag, maar er komen grote stormen aan Röntgenbeeldvorming onthult inzichten in een natuurlijke mug-dodende verbinding
Röntgenbeeldvorming onthult inzichten in een natuurlijke mug-dodende verbinding Licht in combinatie met kracht onthult hoe materialen harder worden wanneer ze verlicht worden
Licht in combinatie met kracht onthult hoe materialen harder worden wanneer ze verlicht worden Hoe de F15 werkt
Hoe de F15 werkt  Aardworm Phylum Kenmerken
Aardworm Phylum Kenmerken Laat de europium helderder schijnen
Laat de europium helderder schijnen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

