
Wetenschap
Hoe verschilt een binaire verbinding van een polyatomair ion?
Compositie:
* Binaire verbindingen bevatten slechts twee elementen, terwijl polyatomaire ionen drie of meer elementen bevatten.
Kosten:
* Binaire verbindingen hebben geen elektrische lading, terwijl polyatomaire ionen een negatieve of positieve lading hebben.
Formatie:
* Binaire verbindingen worden gevormd wanneer twee elementen chemisch reageren en combineren in een eenvoudige gehele getalsverhouding. Omgekeerd worden polyatomaire ionen gevormd wanneer een groep atomen zich met elkaar verbindt en een lading verkrijgt door elektronen te verliezen of te winnen.
Stabiliteit:
* Binaire verbindingen zijn over het algemeen stabieler dan polyatomaire ionen.
Oplosbaarheid:
* De oplosbaarheid van binaire verbindingen en polyatomaire ionen in water en andere oplosmiddelen kan sterk variëren. Sommige binaire verbindingen en polyatomaire ionen kunnen oplosbaar zijn, terwijl andere onoplosbaar kunnen zijn.
Ionische versus covalente bindingen:
* Binaire verbindingen kunnen ontstaan door ionische of covalente binding, afhankelijk van de aard van de betrokken elementen.
Aan de andere kant worden de meeste polyatomaire ionen bij elkaar gehouden door covalente bindingen, hoewel ze ionische binding vertonen met de soort waarmee ze reageren om verbindingen te vormen.
Polyatomaire ionen gedragen zich als afzonderlijke eenheden binnen chemische verbindingen en nemen deel aan ionische binding of covalente binding als geheel, waardoor hun collectieve lading bijdraagt aan de algehele elektrische neutraliteit van de verbinding.
Voorbeelden van binaire verbindingen zijn water (H₂O), kooldioxide (CO₂) en natriumchloride (NaCl). Voorbeelden van polyatomaire ionen zijn hydroxide (OH⁻), carbonaat (CO3²⁻) en ammonium (NH4⁺).
 Klimaat uitgelegd:waarom Mars koud is ondanks een atmosfeer van voornamelijk koolstofdioxide
Klimaat uitgelegd:waarom Mars koud is ondanks een atmosfeer van voornamelijk koolstofdioxide India zet zich schrap voor cycloon, zet marine op scherp
India zet zich schrap voor cycloon, zet marine op scherp Californische firma begraaft 10, 000 mijl aan elektriciteitskabels om bosbranden te stoppen
Californische firma begraaft 10, 000 mijl aan elektriciteitskabels om bosbranden te stoppen Is de bodem uit het regenwoud goed of slecht?
Is de bodem uit het regenwoud goed of slecht?  Supercomputers en ruimtelaser om extreme weersomstandigheden te voorspellen
Supercomputers en ruimtelaser om extreme weersomstandigheden te voorspellen
Hoofdlijnen
- De frisdrankmeren in Oost-Afrika stijgen en vormen een bedreiging voor hun iconische flamingo's
- Wat gebeurt er als er sprake is van mitose?
- Hoe technologie een revolutie teweegbrengt in het insectenonderzoek
- Hoe boerderijen kunnen helpen het eigen microbioom van de aarde te verdedigen
- Varens krijgen eindelijk een genoom en onthullen een geschiedenis van DNA-hamsteren en kleptomanie
- Een nieuw hulpmiddel voor de identificatie van niet-coderend RNA van planten
- Waarom zijn kalkoenen genetisch gemodificeerd?
- Nieuwe online database brengt het genoom in beeld met behulp van moleculaire structuur
- Hoe werkt het hoornvlies?
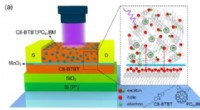
- Wetenschappers ontwikkelen ultragevoelige organische fototransistoren op basis van nieuwe hybride gelaagde architectuur
- Een nieuwe gelelektroforesetechniek voor snelle biomarkerdiagnose via massaspectrometrie

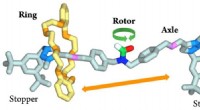
- Mechanica van het oneindig kleine:NanoGear, naar een moleculaire versnelling
- Chemici bieden theoretische interpretatie om chemische reacties te begrijpen

- Waterstof als traphulp

 Belangrijke innovatie op het gebied van fotonische componenten zou de supercomputertechnologie kunnen transformeren
Belangrijke innovatie op het gebied van fotonische componenten zou de supercomputertechnologie kunnen transformeren  Daling van huismus in verband met luchtvervuiling en slechte voeding
Daling van huismus in verband met luchtvervuiling en slechte voeding Groeiende bergen of verschuivende grond:wat gebeurt er in de binnenste kern van de aarde?
Groeiende bergen of verschuivende grond:wat gebeurt er in de binnenste kern van de aarde?  Kosmologische zwaartekrachtsgolven:een nieuwe benadering om terug te reiken naar de oerknal
Kosmologische zwaartekrachtsgolven:een nieuwe benadering om terug te reiken naar de oerknal Kids Science Projects on Things That Melt
Kids Science Projects on Things That Melt Seksueel pesten onder meisjes:we moeten het serieus nemen
Seksueel pesten onder meisjes:we moeten het serieus nemen Hoe overleven planten en dieren in de Arctische toendra?
Hoe overleven planten en dieren in de Arctische toendra?  Macron wil van Frankrijk toegangspoort tot Europa maken voor technologiebedrijven
Macron wil van Frankrijk toegangspoort tot Europa maken voor technologiebedrijven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

