
Wetenschap
Welke producten ontstaan als je zoutzuur aan magnesiummetaal toevoegt?
De uitgebalanceerde chemische vergelijking voor deze reactie is:
```
Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g)
```
Bij deze reactie reageren magnesiumatomen (Mg) uit het metaal met waterstofionen (H+) uit het zoutzuur om waterstofgas (H2) te vormen. Tegelijkertijd combineren de chloride-ionen (Cl-) uit het zoutzuur zich met magnesiumionen (Mg2+) om magnesiumchloride (MgCl2) te vormen.
De reactie tussen magnesium en zoutzuur is exotherm, wat betekent dat er warmte vrijkomt. Het waterstofgas dat tijdens de reactie wordt geproduceerd, is brandbaar en kan in de lucht verbranden.
Deze reactie is een voorbeeld van een enkelvoudige verdringingsreactie, waarbij één element (in dit geval magnesium) een ander element (waterstof) verdringt uit een verbinding (zoutzuur).
 Papierspoor leidt tot ontdekkingen van hartkleppen
Papierspoor leidt tot ontdekkingen van hartkleppen Studie onthult unieke fysieke, chemische eigenschappen van cicadevleugels
Studie onthult unieke fysieke, chemische eigenschappen van cicadevleugels Nieuwe test vindt nieuw mechanisme dat ten grondslag ligt aan veroudering van rode bloedcellen
Nieuwe test vindt nieuw mechanisme dat ten grondslag ligt aan veroudering van rode bloedcellen Is het verdampen van alcohol een chemische verandering?
Is het verdampen van alcohol een chemische verandering?  Wat vuurmieren ons kunnen leren over het maken van betere zelfherstellende materialen
Wat vuurmieren ons kunnen leren over het maken van betere zelfherstellende materialen
 De megasteden van Afrika worden bedreigd door hitte, overstromingen en ziekten – actie is nodig om te beginnen met vergroenen en zich aan te passen aan de klimaatverandering
De megasteden van Afrika worden bedreigd door hitte, overstromingen en ziekten – actie is nodig om te beginnen met vergroenen en zich aan te passen aan de klimaatverandering  Amerikaanse wetenschappers bestuderen de impact van uranium in de Grand Canyon-regio
Amerikaanse wetenschappers bestuderen de impact van uranium in de Grand Canyon-regio Nepnieuws over vulkaanuitbarstingen kan levens in gevaar brengen
Nepnieuws over vulkaanuitbarstingen kan levens in gevaar brengen Wat elk land wel en niet kan doen op Antarctica, de naam van wetenschap
Wat elk land wel en niet kan doen op Antarctica, de naam van wetenschap  Kun je een hogedrukreiniger met een regenton gebruiken?
Kun je een hogedrukreiniger met een regenton gebruiken?
Hoofdlijnen
- De prevalentie van antimicrobiële resistentie varieert per leeftijd en geslacht bij bloedbaaninfecties in Europese ziekenhuizen:onderzoek
- Menselijke intelligentie:hoe cognitieve circuits, in plaats van hersengrootte, de evolutie ervan aandreven
- Hoe bloedparasieten koloniseren en blijven bestaan in vogelpopulaties op kleine eilanden
- Sinds de beursintroductie heeft Snap Inc. precies gedaan wat het beloofde, dus waarom hebben aandelen het moeilijk?
- Vergelijking & identificatie van kikkers en menselijke bloedcellen
- Welke monosacharide zit in fruit?
- Wat is er in uw lichaam gevuld met een stof die merg wordt genoemd?
- Kan glucose door het celmembraan diffunderen door eenvoudige diffusie?
- Waarom verwekken oudere mannetjesvogels meer onwettige kinderen?
- Gasopslagmethode kan de volgende generatie schone energievoertuigen helpen

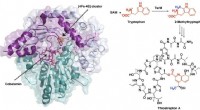
- Synthese van krachtig antibioticum volgt ongebruikelijke chemische route
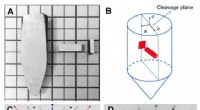
- Hoge thermo-elektrische prestaties in goedkope SnS0.91Se0.09-kristallen
- Meer zonne-energie dankzij titanium

- Controleren en visualiseren van receptorsignalen in neurale cellen met licht

 Wat is de chemische formule van gemodificeerd voedselzetmeel?
Wat is de chemische formule van gemodificeerd voedselzetmeel?  Senegals oude hoofdstad in frontlinie tegen stijgende zee
Senegals oude hoofdstad in frontlinie tegen stijgende zee Onderzoekers die plantensoorten catalogiseren proberen te ontcijferen wat sommige groepen zo succesvol maakt
Onderzoekers die plantensoorten catalogiseren proberen te ontcijferen wat sommige groepen zo succesvol maakt  Hoe werkt ruw ER met Ribosomes?
Hoe werkt ruw ER met Ribosomes?  Een hoek naar een decimal
Een hoek naar een decimal Nieuwe netwerken
Nieuwe netwerken Close-ups van de zon
Close-ups van de zon Hoe het Scroll Grid te gebruiken in het Everyday Math-programma
Hoe het Scroll Grid te gebruiken in het Everyday Math-programma
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

