
Wetenschap
Hoeveel gram Ca-OH-2 is nodig om 100 ml oplossing 0,1 M Ca-OH-2 te bereiden?
De molaire massa van Ca(OH)2 is 74,09 g/mol.
Stap 2:Bereken het aantal mol Ca(OH)2 dat nodig is om 100 ml van een 0,1 M-oplossing te bereiden.
Het benodigde aantal mol Ca(OH)2 kan worden berekend met de formule:
```
Mol Ca(OH)2 =Concentratie (in mol/L) × Volume oplossing (in L)
```
In dit geval is de concentratie 0,1 M en het volume van de oplossing 100 ml, wat overeenkomt met 0,1 l.
```
Mol Ca(OH)2 =0,1 mol/L × 0,1 L =0,01 mol
```
Stap 3:Bereken de benodigde massa Ca(OH)2.
De benodigde massa Ca(OH)2 kan worden berekend door het aantal mol te vermenigvuldigen met de molaire massa.
```
Massa van Ca(OH)2 =Mol Ca(OH)2 × Molaire massa van Ca(OH)2
```
In dit geval is het aantal mol 0,01 mol en de molaire massa van Ca(OH)2 74,09 g/mol.
```
Massa van Ca(OH)2 =0,01 mol × 74,09 g/mol =0,7409 g
```
Daarom is 0,7409 gram Ca(OH)2 nodig om 100 ml van een 0,1 M Ca(OH)2-oplossing te bereiden.
 Wetenschappers observeren de rol van cavitatie bij het breken van glas
Wetenschappers observeren de rol van cavitatie bij het breken van glas Waarom beïnvloedt de aard van materialen de weerstand?
Waarom beïnvloedt de aard van materialen de weerstand?  Vaccin-ingrediënten kunnen zich verbergen in bibliotheken met kleine moleculen
Vaccin-ingrediënten kunnen zich verbergen in bibliotheken met kleine moleculen Klei gebruiken om eeuwige gifstoffen te bestrijden:wetenschappers verduidelijken de basis voor een innovatief PFAS-filter gemaakt van klei
Klei gebruiken om eeuwige gifstoffen te bestrijden:wetenschappers verduidelijken de basis voor een innovatief PFAS-filter gemaakt van klei  Olievlekken behandelen met chemische dispergeermiddelen:is het middel erger dan de kwaal?
Olievlekken behandelen met chemische dispergeermiddelen:is het middel erger dan de kwaal?
 Orkanen en andere rampen met extreem weer zetten sommige mensen ertoe aan te verhuizen en anderen op hun plaats te houden
Orkanen en andere rampen met extreem weer zetten sommige mensen ertoe aan te verhuizen en anderen op hun plaats te houden De geesteswetenschappen in Amerika – een bedreigde diersoort?
De geesteswetenschappen in Amerika – een bedreigde diersoort?  Ernstige droogte doet dromen van Turkse boeren opdrogen
Ernstige droogte doet dromen van Turkse boeren opdrogen De moleculaire kenmerken van opgeloste organische stof in een eutrofe kustbaai
De moleculaire kenmerken van opgeloste organische stof in een eutrofe kustbaai Nepal probeert record met een Dode Zee van plastic zakken
Nepal probeert record met een Dode Zee van plastic zakken
Hoofdlijnen
- Transformatief onderzoek onrealistisch om te voorspellen, wetenschappers vertellen subsidieverstrekkers
- Microscopie onthult mechanisme achter nieuwe CRISPR-tool
- Nieuwe hypothese legt uit hoe menselijke voorouders vuur in hun voordeel gebruikten
- Nieuw onderzoek onderzoekt hoe ziekten zich verspreiden bij primaten
- Hoe empathie werkt
- Hoe viraal afgeleide transposons worden gedomesticeerd om nieuwe levensvormen te ontwikkelen
- Wat zit er in een ei? Eicelfactoren die volwassen cellen kunnen herprogrammeren
- IJzer-zwavelmineralen kunnen getuigen van de eerste microben op aarde die miljarden jaren geleden leefden
- Staat, FBI onderzoekt ziekte die ziek is, dode honden
- Op hematiet gebaseerde nanodraadstructuren om de conversie van zonne-energie naar brandstof bij foto-elektrochemische watersplitsing te verbeteren

- Nieuwe methode stimuleert de vorming van syngas uit biopolyolen
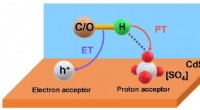
- Elektrolytisch gedeponeerde oppervlakken met omkeerbaar schakelende grensvlakeigenschappen
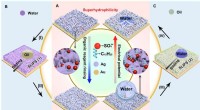
- De eigenschappen van composieten voor het bouwen van betrouwbare treinen

- PNNL-technologie maakt de weg vrij voor van ethanol afgeleide vliegtuigbrandstof

 Tropische regenwouden tonen de fosforsleutel om de ecosystemen van de wereld te begrijpen
Tropische regenwouden tonen de fosforsleutel om de ecosystemen van de wereld te begrijpen Wat is de netto ionische vergelijking van Na plus OH- H Cl- H2O Cl-?
Wat is de netto ionische vergelijking van Na plus OH- H Cl- H2O Cl-?  NASA-NOAA's Suomi NPP Satellite krijgt twee blikken op orkaan Maria
NASA-NOAA's Suomi NPP Satellite krijgt twee blikken op orkaan Maria Probleem met implementatie van Bluetooth naar voren gebracht door team dat tracking verkent
Probleem met implementatie van Bluetooth naar voren gebracht door team dat tracking verkent Wat zijn de vier eukaryote rijken?
Wat zijn de vier eukaryote rijken?  Voor Amerikanen, mobiele apparaten top voor nieuws:enquête
Voor Amerikanen, mobiele apparaten top voor nieuws:enquête Beschadigd schip dat olie lekt voor Mauritius kan splitsen:PM
Beschadigd schip dat olie lekt voor Mauritius kan splitsen:PM Wegen onderhouden met druiven- en landbouwafval
Wegen onderhouden met druiven- en landbouwafval
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

