
Wetenschap
Hoeveel liter zuurstof is er nodig om precies te reageren met 27,8 g methaan bij STP?
Bij STP neemt 1 mol van welk gas dan ook 22,4 liter in beslag. De molaire massa van methaan (CH₄) is 16 g/mol, dus 27,8 g methaan is 27,8 g / 16 g/mol =1,7375 mol.
De uitgebalanceerde chemische vergelijking voor de verbranding van methaan is:
CH₄ + 2O₂ → CO₂ + 2H₂O
Uit de uitgebalanceerde chemische vergelijking kunnen we zien dat 1 mol methaan reageert met 2 mol zuurstof. Daarom zal 1,7375 mol methaan reageren met 2 × 1,7375 mol =3,475 mol zuurstof.
Bij STP neemt 1 mol zuurstof 22,4 liter in beslag, dus 3,475 mol zuurstof neemt 3,475 mol x 22,4 l/mol =77,76 liter in beslag.
Daarom is er 77,76 liter zuurstof nodig om precies te reageren met 27,8 g methaan bij STP.
 Is keukenzout uniform of niet-uniform?
Is keukenzout uniform of niet-uniform?  Gemanipuleerde enzymen - onderzoekers zetten mijlpaal in onderzoek naar biokatalyse
Gemanipuleerde enzymen - onderzoekers zetten mijlpaal in onderzoek naar biokatalyse Versleten banden kunnen worden hergebruikt in nieuwe asfaltwegen
Versleten banden kunnen worden hergebruikt in nieuwe asfaltwegen Is foliumzuur het equivalent van foliumzuur?
Is foliumzuur het equivalent van foliumzuur?  Onderzoekers ontdekken het moleculaire mechanisme van de binding van methamfetamine aan de sporenaminereceptor
Onderzoekers ontdekken het moleculaire mechanisme van de binding van methamfetamine aan de sporenaminereceptor
 UMD en Resilinc Corp. creëren index van risico op klimaatverandering voor toeleveringsketens van bedrijven
UMD en Resilinc Corp. creëren index van risico op klimaatverandering voor toeleveringsketens van bedrijven Onderzoek wijst op ongekende en zorgwekkende stijging van de zeespiegel
Onderzoek wijst op ongekende en zorgwekkende stijging van de zeespiegel Kliffen storten in bij vulkaan Hawaï, het stoppen van de brandslangstroom
Kliffen storten in bij vulkaan Hawaï, het stoppen van de brandslangstroom Recordbrekende oceaanhitte veroorzaakte orkaan Harvey
Recordbrekende oceaanhitte veroorzaakte orkaan Harvey Smeltrotsmodellen voorspellen mechanische oorsprong van aardbevingen
Smeltrotsmodellen voorspellen mechanische oorsprong van aardbevingen
Hoofdlijnen
- Hoe cellen kunstmatige ingrediënten 'lezen' die in een genetisch recept worden gegooid
- Wat zijn de verschillen tussen een virus en een parasiet?
- Prolifereren of niet prolifereren? Een cellulaire lente antwoordt
- De onafhankelijke evolutie van vergelijkbare eigenschappen in organismen wordt veroorzaakt door?
- Verschuivende aanwezigheid van Noord-Atlantische walvissen gevolgd met passieve akoestiek
- Schimmel is afhankelijk van bacteriën om de belangrijkste componenten van zijn voortplantingsmechanisme te reguleren
- Wat zijn enkele problemen in de evolutietheorie?
- Onderzoekers presenteren nieuw wiskundig model voor het bestuderen van niercellen
- Team brengt in kaart hoe autofagie functioneert bij zoogdieren; SARS-CoV-2-infectie kan het proces verstoren
- Beton met verbeterd slagvastheid voor verdedigingsconstructies

- Elektrisch geleidende verven en andere polymeerlegeringen nu gemakkelijk te produceren

- Nieuwe biochemische route die meer veerkrachtige gewasvariëteiten kan ontwikkelen

- Hoogrenderende katalysator verbetert de elektrische reductieprestaties van kooldioxide

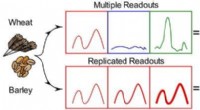
- Een stap in de richting van een gevoelige en snelle glutendetectie
 Hoe de lensdikte te meten
Hoe de lensdikte te meten Onderzoekers meten afzonderlijke atomen in een grafeen-petrischaal
Onderzoekers meten afzonderlijke atomen in een grafeen-petrischaal Wat is latente warmteoverdracht?
Wat is latente warmteoverdracht?  Onderzoekers onderzoeken het gebruik van licht om schijven in de mesosfeer te laten zweven
Onderzoekers onderzoeken het gebruik van licht om schijven in de mesosfeer te laten zweven Onbreekbare gsm-schermen een stap dichterbij
Onbreekbare gsm-schermen een stap dichterbij Onderzoekers onderzoeken hoe de subtiele keuze van synoniemen ervoor kan zorgen dat u weet welke politieke partij u steunt
Onderzoekers onderzoeken hoe de subtiele keuze van synoniemen ervoor kan zorgen dat u weet welke politieke partij u steunt  Fluctuerende koffieprijzen oefenen mentale druk uit op Vietnamese boeren
Fluctuerende koffieprijzen oefenen mentale druk uit op Vietnamese boeren  De oerknal – een ooggetuigenverslag
De oerknal – een ooggetuigenverslag
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

