
Wetenschap
Wat is de binding van zilverchloride?
De binding in zilverchloride (AgCl) is voornamelijk ionisch van aard. Dit betekent dat de binding tussen het zilverkation (Ag) en het chlorideanion (Cl) wordt gevormd door de overdracht van elektronen van het metaal naar het niet-metaal.
In AgCl verliest elk zilveratoom één valentie-elektron om een positief geladen zilverion (Ag+) te worden, terwijl elk chlooratoom het elektron wint om een negatief geladen chloride-ion (Cl-) te worden.
De algehele binding in AgCl wordt dus aangedreven door de elektrostatische aantrekking tussen de positief geladen zilverionen en de negatief geladen chloride-ionen, wat resulteert in de vorming van een stabiele ionische verbinding. De sterke elektrostatische krachten tussen de ionen houden het kristalrooster van AgCl bij elkaar.
 Nieuwe diagnostische strip voor jichtpatiënten met een enkele traan
Nieuwe diagnostische strip voor jichtpatiënten met een enkele traan Chemici vergroten het nut van boor:voorkomen dat verbindingen worden afgebroken, kan scheikundigen helpen bij het ontwerpen van nieuwe medicijnen
Chemici vergroten het nut van boor:voorkomen dat verbindingen worden afgebroken, kan scheikundigen helpen bij het ontwerpen van nieuwe medicijnen Algoritme identificeert optimale paren voor het samenstellen van metaal-organische raamwerken
Algoritme identificeert optimale paren voor het samenstellen van metaal-organische raamwerken Onderzoekers identificeren nieuwe verbindingen om RSV te behandelen, Zika-virus
Onderzoekers identificeren nieuwe verbindingen om RSV te behandelen, Zika-virus Een nikkelkatalysator met koolwaterstoffen gebruiken om vetzuren te maken
Een nikkelkatalysator met koolwaterstoffen gebruiken om vetzuren te maken
 Ernst van de droogte in het stroomgebied van de Gele Rivier in de afgelopen 55 jaar
Ernst van de droogte in het stroomgebied van de Gele Rivier in de afgelopen 55 jaar Een studie vergelijkt hoe water wordt beheerd in Spanje, Californië en Australië
Een studie vergelijkt hoe water wordt beheerd in Spanje, Californië en Australië Hoe u milieuvriendelijke producten kunt vinden
Hoe u milieuvriendelijke producten kunt vinden  Opinie:Waarom het organiseren van een Olympische wedstrijd op Tahiti een heel slecht idee is
Opinie:Waarom het organiseren van een Olympische wedstrijd op Tahiti een heel slecht idee is  80 jaar sinds de eerste berekeningen aantoonden dat de aarde opwarmde door de toenemende uitstoot van broeikasgassen
80 jaar sinds de eerste berekeningen aantoonden dat de aarde opwarmde door de toenemende uitstoot van broeikasgassen
Hoofdlijnen
- Hoe menselijke migratie werkt
- Een evenwicht vinden in de antibioticageneeskunde:kunnen we slechte bacteriën doden en tegelijkertijd de goede behouden?
- Waarom wordt mijn huis overspoeld door pantrymotten en hoe kom ik van ze af?
- Waarom sommige kevers van alcohol houden
- Onderbroken herprogrammering zet volwassen cellen om in hoge opbrengsten van voorloperachtige cellen
- Onderzoekers bepalen hoe de bacteriën van veteranenziekten zich vermenigvuldigen en ziekten veroorzaken
- Kunnen inheemse bijen, nu de kolonies van honingbijen instorten, de bestuiving aan?
- Sardines nemen ons mee naar de bronnen van biodiversiteit in de Amazone-rivier
- Wat betekent de term haploïde?
- Synthetische fysiologen ontwikkelen nieuwe receptor uitgeschakeld door groen licht

- Zeer gevoelige trigger maakt snelle detectie van biologische agentia mogelijk

- Onderzoekers vinden goedkoper, minder energie-intensieve manier om ethyleen te zuiveren

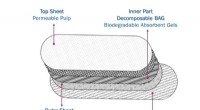
- Veiliger maandverband gemaakt van palmzetmeel
- De pH van calciumionen regelt de opening van het ionkanaal

 Ontdekking van een verborgen kwantumkritisch punt in tweedimensionale supergeleiders
Ontdekking van een verborgen kwantumkritisch punt in tweedimensionale supergeleiders  Zullen intensieve bospraktijken invloed hebben op de waterkwaliteit?
Zullen intensieve bospraktijken invloed hebben op de waterkwaliteit?  Het functioneren van terrestrische ecosystemen wordt bepaald door drie hoofdfactoren:
Het functioneren van terrestrische ecosystemen wordt bepaald door drie hoofdfactoren: Een nieuwe kijk op exoplaneten met de aankomende Webb-telescoop van NASA
Een nieuwe kijk op exoplaneten met de aankomende Webb-telescoop van NASA Wat is de chemische naam voor plastic?
Wat is de chemische naam voor plastic?  Degradatie van het ecosysteem op de Filippijnen
Degradatie van het ecosysteem op de Filippijnen  Hooggerechtshof behandelt Google class action-schikkingszaak
Hooggerechtshof behandelt Google class action-schikkingszaak Gegevens suggereren dat zwarte gaten stellaire brokstukken in uitbarstingen opslokken
Gegevens suggereren dat zwarte gaten stellaire brokstukken in uitbarstingen opslokken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

