
Wetenschap
Hoe breken waterstofbruggen tussen stikstof?
1. Protonoverdracht: Bij protonenoverdracht wordt een proton (H+) overgedragen van het ene stikstofatoom naar het andere. Dit kan gebeuren als het ene stikstofatoom zuurder is dan het andere, of als er een base aanwezig is om het proton te accepteren.
2. Splijting van waterstofbruggen: Bij het splitsen van waterstofbruggen wordt de waterstofbrug verbroken zonder de overdracht van een proton. Dit kan gebeuren als de temperatuur stijgt, als er een oplosmiddel wordt toegevoegd dat de waterstofbrug verbreekt, of als er een chemische reactie optreedt die de binding verbreekt.
3. Concurrentiebinding: Bij competitieve binding concurreert een ander molecuul of atoom met de stikstofatomen om waterstofbinding. Dit kan leiden tot het verbreken van waterstofbruggen tussen stikstofatomen als het concurrerende molecuul of atoom sterker waterstofgebonden is aan een van de stikstofatomen.
4. Elektrostatische afstoting: Bij elektrostatische afstoting stoten de negatieve ladingen van de stikstofatomen elkaar af, wat de waterstofbruggen kan verzwakken en uiteindelijk kan verbreken. Dit effect is meer uitgesproken bij polaire oplosmiddelen, die kunnen helpen de gescheiden stikstofatomen te stabiliseren.
Het specifieke mechanisme waarmee waterstofbruggen tussen stikstofatomen verbreken, hangt af van het specifieke systeem dat wordt overwogen.
 Peel-off coating houdt ontzilting schoner en groener
Peel-off coating houdt ontzilting schoner en groener Glas en de energiehervorming:duurzame productie dankzij elektriciteit?
Glas en de energiehervorming:duurzame productie dankzij elektriciteit? Hoe de verspreiding van dodelijke 'superbugs' te vertragen
Hoe de verspreiding van dodelijke 'superbugs' te vertragen  Succes bij het beheersen van de samenstelling van perovskitionen maakt de weg vrij voor apparaattoepassingen
Succes bij het beheersen van de samenstelling van perovskitionen maakt de weg vrij voor apparaattoepassingen Olie uit water halen in een wetenschapsproject
Olie uit water halen in een wetenschapsproject
 NASA volgt de Atlantische Oceaan Tropische storm Rina
NASA volgt de Atlantische Oceaan Tropische storm Rina NASA-NOAA-satelliet ziet tropische cycloon Wallace verdwijnen
NASA-NOAA-satelliet ziet tropische cycloon Wallace verdwijnen Overstromingen:Britse kuststeden en -dorpen staan voor een ontwerpuitdaging om het hoofd te bieden aan de klimaatnoodsituatie
Overstromingen:Britse kuststeden en -dorpen staan voor een ontwerpuitdaging om het hoofd te bieden aan de klimaatnoodsituatie De Green New Deal verandert al de voorwaarden van het debat over klimaatactie
De Green New Deal verandert al de voorwaarden van het debat over klimaatactie Hoe draagt het openbaar vervoer bij aan het milieu?
Hoe draagt het openbaar vervoer bij aan het milieu?
Hoofdlijnen
- Mutante bacteriën gebruiken om te bestuderen hoe veranderingen in membraaneiwitten de celfuncties beïnvloeden
- Waarom verzamelen vrouwelijke grote hamerhaaien zich elke zomer in Frans-Polynesië?
- Hebben alle planten vaatbundels?
- Uit mondiaal onderzoek blijkt dat er in het donker een derde meer insecten naar buiten komen
- Genetische onderzoeken bij honden onthullen waarom Shar-Peis gerimpeld zijn
- Gewassen evolueerden 10 millennia eerder dan gedacht
- Hoe de genetische blauwdrukken voor ledematen van vissen kwamen
- Nieuw mechanisme wijst de weg naar het doorbreken van de antibioticaresistentie van ribosoom
- Wetenschappers ontdekken hoe mysterieus 'circulair RNA' wordt gevormd, claimen een verband met spierdystrofie
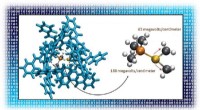
- Optimalisatie van elektrische velden levert betere katalysatoren op
- 3D-microstructuren in realtime vastleggen

- Ontdekking van natuurlijk chirale oppervlakken voor veiligere geneesmiddelen

- Onderzoekers leggen de unieke onderliggende atomaire structuur van PNCP-metaalglas uit

- Ingenieurs maken veelbelovend materiaal stabiel genoeg voor gebruik in zonnecellen

 Hoe jachtgeweren werken
Hoe jachtgeweren werken  NASA meet orkaan Marias hevige regenval, ziet oog weer opengaan
NASA meet orkaan Marias hevige regenval, ziet oog weer opengaan Veel meer bacteriën hebben elektrisch geleidende filamenten
Veel meer bacteriën hebben elektrisch geleidende filamenten Saffieren tonen hun ware kleuren:niet waterminnend
Saffieren tonen hun ware kleuren:niet waterminnend Nieuw raamwerk zorgt voor nauwkeurigheid, efficiëntie bij het identificeren van stopwoorden
Nieuw raamwerk zorgt voor nauwkeurigheid, efficiëntie bij het identificeren van stopwoorden NASA-missies bieden nieuwe inzichten in oceaanwerelden in ons zonnestelsel
NASA-missies bieden nieuwe inzichten in oceaanwerelden in ons zonnestelsel Robotstok waarvan is aangetoond dat het de stabiliteit bij het lopen verbetert
Robotstok waarvan is aangetoond dat het de stabiliteit bij het lopen verbetert De vorm van de gletsjer beïnvloedt de gevoeligheid voor dunner worden
De vorm van de gletsjer beïnvloedt de gevoeligheid voor dunner worden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

