
Wetenschap
Welk antwoord beschrijft hoe een ionische binding ontstaat?
Wanneer atomen met een groot verschil in elektronegativiteit op elkaar inwerken, neemt het ene atoom de elektronen volledig over van het andere atoom, wat resulteert in de vorming van een ionische binding. Wanneer het elektronegatieve atoom het elektron opneemt, wordt het negatief geladen en vormt het een anion, terwijl het atoom dat een elektron verliest positief geladen wordt en een kation vormt. De ionen worden vervolgens tot elkaar aangetrokken vanwege hun tegengestelde ladingen. De sterkte van de ionische binding houdt rechtstreeks verband met het elektronegativiteitsverschil tussen de twee ionen en de grootte van de ionen; hoe groter het elektronegativiteitsverschil en hoe kleiner de ionen, hoe sterker de ionische binding zal zijn.
 Met trucs voor materiaalverwerking kunnen ingenieurs nieuw lasermateriaal maken
Met trucs voor materiaalverwerking kunnen ingenieurs nieuw lasermateriaal maken Bevat het water van het mariene ecosysteem opgelost zout?
Bevat het water van het mariene ecosysteem opgelost zout?  Oude eiwitten vertellen verhalen over historische artefacten en de mensen die ze hebben aangeraakt
Oude eiwitten vertellen verhalen over historische artefacten en de mensen die ze hebben aangeraakt Welke grondstoffen kunnen worden gebruikt om synthetische diamanten te vervaardigen?
Welke grondstoffen kunnen worden gebruikt om synthetische diamanten te vervaardigen?  is bloed een mengsel of een pure substantie, heterohomogeen?
is bloed een mengsel of een pure substantie, heterohomogeen?
Hoofdlijnen
- Onderzoekers ontrafelen het eeuwenoude mysterie waarom cellen fermentatie gebruiken
- Als je jezelf zou kunnen klonen, zou je dan nog steeds seks hebben?
- Tsjaad breidt belangrijk natuurgebied in nationaal park uit
- Hoe blijven ijsberen warm? Onderzoek vindt een antwoord in hun genen
- Achtertuinen en stadsparken ondersteunen de diversiteit van vogels op unieke manieren
- Nieuwe studie biedt mechanistische inzichten in hoe gentranscriptie wordt gereguleerd in zoogdiercellen
- Hoe enzymen werken:UB-chemici publiceren een belangrijke ontdekking
- Hoe niet-verwante wespen slagen door anderen te helpen zich voort te planten
- Geofysicus vindt leermogelijkheden in filmfouten
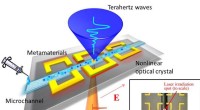
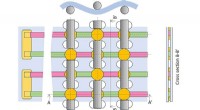
- Microanalyse van biologische monsters voor vroege detectie van ziekten
- Lichaamswarmte door flexibele stof kan IoT-apparaten aandrijven voor gezondheidsmonitoring voor mensen, huisdieren, machines
- Beeldvorming van de chemische structuur van individuele moleculen, atoom voor atoom

- Techniek kan het gemakkelijker maken om mRNA te gebruiken om ziekten te behandelen of vaccins af te leveren

- Galvaniseren levert hoge energie, krachtige batterijen
 Orkaan Marias nasleep: ecologische ramp gaat door
Orkaan Marias nasleep: ecologische ramp gaat door  Wat is de toekomst van aardwarmte?
Wat is de toekomst van aardwarmte?  Zelfrijdende machines van Amazon komen eerder dan mensen verwachten
Zelfrijdende machines van Amazon komen eerder dan mensen verwachten Hoe AI kan helpen de geschreven taal van oude beschavingen te vertalen
Hoe AI kan helpen de geschreven taal van oude beschavingen te vertalen Nieuwe techniek om nanokristallen te synthetiseren die zonne-energie oogsten
Nieuwe techniek om nanokristallen te synthetiseren die zonne-energie oogsten Is werk de overdracht van energie?
Is werk de overdracht van energie?  NASA begint met het laatste ijsonderzoek in de lucht
NASA begint met het laatste ijsonderzoek in de lucht Hawaii vulkaan stuurt meer lava, zwavelgas in gemeenschappen
Hawaii vulkaan stuurt meer lava, zwavelgas in gemeenschappen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

