
Wetenschap
Wat vertelt geleidbaarheid ons over de aard van chemische stoffen?
1. Ionische verbindingen:Geleidbaarheid is een bepalende eigenschap van ionische verbindingen. Wanneer opgelost in water of gesmolten, dissociëren ionische verbindingen in positief geladen kationen en negatief geladen anionen, waardoor een oplossing ontstaat die elektriciteit kan geleiden. De aanwezigheid van deze vrije ionen maakt de beweging van elektrische lading mogelijk, wat resulteert in een hoge geleidbaarheid.
2. Covalente verbindingen:In tegenstelling tot ionische verbindingen hebben covalente verbindingen over het algemeen een lage of geen geleidbaarheid. Covalente bindingen omvatten het delen van elektronen tussen atomen, en deze elektronen worden stevig vastgehouden in de moleculaire structuur. Als gevolg hiervan missen covalente verbindingen vrije ionen die elektrische lading kunnen dragen, waardoor ze slechte elektriciteitsgeleiders zijn.
3. Metalen:Metalen zijn uitstekende geleiders van elektriciteit vanwege hun unieke atomaire structuur. Metaalatomen hebben losjes gebonden valentie-elektronen die vrij kunnen bewegen binnen het metaalrooster. Deze mobiele elektronen kunnen gemakkelijk elektrische lading vervoeren, waardoor metalen efficiënt elektriciteit kunnen geleiden.
4. Zuren, basen en zouten:geleidbaarheidsmetingen kunnen helpen bij het identificeren van de aard van zuren, basen en zouten in waterige oplossingen. Zuren en basen dissociëren, wanneer ze in water worden opgelost, in ionen, waardoor hun oplossingen geleidend worden. Aan de andere kant vertonen neutrale zouten gevormd door de reactie van zuren en basen ook geleidbaarheid in water vanwege de aanwezigheid van vrije ionen.
5. Concentratie en sterkte:Geleidbaarheidsmetingen kunnen informatie verschaffen over de concentratie en sterkte van elektrolytoplossingen. Over het algemeen geldt dat hoe hoger de concentratie van ionen in een oplossing, hoe hoger de geleidbaarheid ervan. Deze eigenschap maakt het mogelijk de concentratie van ionische soorten en de sterkte van elektrolyten te bepalen.
6. Zuiverheidsbeoordeling:Geleidbaarheidsmetingen kunnen worden gebruikt om de zuiverheid van chemische stoffen te beoordelen. Onzuiverheden in de vorm van ionische verontreinigingen kunnen de geleidbaarheid van een stof verhogen. Door de geleidbaarheid van een stof te vergelijken met bekende normen of specificaties, kan de aanwezigheid en het niveau van onzuiverheden worden gedetecteerd.
Samenvattend bieden geleidbaarheidsmetingen waardevolle inzichten in de aard van chemische stoffen door hun vermogen om elektriciteit te geleiden te onthullen. Ze helpen onderscheid te maken tussen ionische en covalente verbindingen, beoordelen de aanwezigheid en concentratie van ionen in oplossingen en evalueren de zuiverheid van stoffen. Geleidbaarheidsmetingen spelen een cruciale rol op verschillende gebieden, waaronder de chemie, elektrochemie en analytische wetenschap, en verschaffen essentiële informatie voor het begrijpen van de eigenschappen en het gedrag van chemische stoffen.
 Bepaling van de bioaccumulatie van 9 metalen in ongewervelde waterdieren in mijngebieden
Bepaling van de bioaccumulatie van 9 metalen in ongewervelde waterdieren in mijngebieden Sanibel Island, Florida Scheitips
Sanibel Island, Florida Scheitips  Kleine kristallen leggen miljoenen jaren geschiedenis van bergketens vast:geoloog graaft de Himalaya op met een microscoop
Kleine kristallen leggen miljoenen jaren geschiedenis van bergketens vast:geoloog graaft de Himalaya op met een microscoop  NASA-studie verifieert trends in de opwarming van de aarde
NASA-studie verifieert trends in de opwarming van de aarde Na een grote aardbeving, naschokken blijven Alaska rammelen
Na een grote aardbeving, naschokken blijven Alaska rammelen
Hoofdlijnen
- Grizzlies vertonen opmerkelijke gencontrole vóór en tijdens de winterslaap
- Trechtervisie:nieuwe informatie over hoe cellen in het oog helpen licht naar het netvlies te geleiden
- Waaruit bestaan celwanden?
- Designer biosensor kan de productie van antibiotica door microben detecteren
- Wetenschappers identificeren genetische mechanismen die betrokken zijn bij de manier waarop vrouwen eigenschappen erven
- Problemen met parasieten? Gewoon migreren!
- Hoe Bracket-schimmels aan hun eigen voedsel komen?
- Heeft een boom een kern?
- Van motief naar methode,
- Een multidimensionaal beeld van SARS-CoV-2

- Scheurvoortplanting is asymmetrisch in polaire materialen

- Röntgenexperimenten dragen bij aan studies van een medicijn dat nu is goedgekeurd om tuberculose te bestrijden

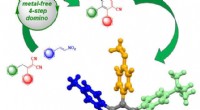
- Een innovatieve methode om complexe moleculen te produceren
- 3D-geprint apparaat vindt naald in hooiberg kankercellen door hooi te verwijderen

 De elektronische transistor waar je op hebt gewacht
De elektronische transistor waar je op hebt gewacht Nieuwe materialen vertonen een gespleten persoonlijkheid
Nieuwe materialen vertonen een gespleten persoonlijkheid Panel voert antitrustonderzoek in de VS op met Big Tech-verzoek
Panel voert antitrustonderzoek in de VS op met Big Tech-verzoek Wat deden mensen uit de Bronstijd met al dat brons? Nieuw onderzoek blaast oude argumenten over de aard van geld nieuw leven in
Wat deden mensen uit de Bronstijd met al dat brons? Nieuw onderzoek blaast oude argumenten over de aard van geld nieuw leven in  Wat zijn de effecten van uitloging?
Wat zijn de effecten van uitloging?  Kan een computerchip nul energieverlies hebben in 1,58 dimensies?
Kan een computerchip nul energieverlies hebben in 1,58 dimensies?  Hoe planetaire nevels hun vorm krijgen
Hoe planetaire nevels hun vorm krijgen  Welke naam metaalmix in goud?
Welke naam metaalmix in goud?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

