
Wetenschap
Welke reactie veroorzaakt wanneer natrium reageert met waterstof?
Na + 1/2 H2 -> NaH
In deze vergelijking reageert één natriumatoom met een half molecuul waterstofgas om één molecuul natriumhydride te produceren. De reactie vindt doorgaans plaats bij verhoogde temperaturen en er kan warmte en licht vrijkomen, waardoor het een exotherme reactie wordt.
Wanneer natriummetaal onder geschikte omstandigheden in contact wordt gebracht met waterstofgas, verliezen de natriumatomen gemakkelijk hun buitenste elektron aan de waterstofmoleculen. Dit resulteert in de vorming van positief geladen natriumionen (Na+) en negatief geladen waterstofionen (H-). De elektrostatische aantrekkingskracht tussen deze ionen leidt tot de vorming van ionische bindingen, resulterend in de vorming van natriumhydride (NaH).
Natriumhydride is een witte of kleurloze kristallijne substantie die zeer reactief is. Het is een ionische verbinding, met natriumkationen (Na+) en hydride-anionen (H-). NaH wordt vaak gebruikt als reductiemiddel bij verschillende chemische reacties, vooral bij de organische synthese. Het wordt ook vaak gebruikt als bron van waterstofgas in bepaalde industriële processen.
 Een elektrokatalysator voor de reactie van zuurstofontwikkeling bij het splitsen van water
Een elektrokatalysator voor de reactie van zuurstofontwikkeling bij het splitsen van water Egg in Bottle Science Projects
Egg in Bottle Science Projects  Elektrostatisch gecontroleerde oppervlakterandvoorwaarden in nematische vloeibare kristallen en colloïden
Elektrostatisch gecontroleerde oppervlakterandvoorwaarden in nematische vloeibare kristallen en colloïden Natuurkundigen maken een model om de eigenschappen van elk molecuul te voorspellen
Natuurkundigen maken een model om de eigenschappen van elk molecuul te voorspellen Bufferoplossingen voorbereiden
Bufferoplossingen voorbereiden
 Klimaatverandering - lessen van de Vikingen
Klimaatverandering - lessen van de Vikingen Gefossiliseerde boom en ijskernen helpen bij het dateren van enorme vulkaanuitbarsting 1, 000 jaar geleden tot binnen drie maanden
Gefossiliseerde boom en ijskernen helpen bij het dateren van enorme vulkaanuitbarsting 1, 000 jaar geleden tot binnen drie maanden Zware overstromingen treffen centraal China; metro's overstroomd
Zware overstromingen treffen centraal China; metro's overstroomd Snowpack in Californië onderzocht als indicator van droogte
Snowpack in Californië onderzocht als indicator van droogte Warmte, overstromingen, branden:jetstream belangrijke schakel bij klimaatrampen
Warmte, overstromingen, branden:jetstream belangrijke schakel bij klimaatrampen
Hoofdlijnen
- Kwallenexperts tonen aan dat toegenomen bloei een gevolg is van periodieke mondiale schommelingen
- Onthulling van de genetische blauwdruk van saffloer
- Waarom zou een natuurlijke antimicrobiële verbinding een gunstige ontwikkeling kunnen zijn?
- Beweging van DNA gekoppeld aan de reactie op schade, het vermogen om zichzelf te herstellen
- Scheiding komt vaker voor bij albatrosparen met verlegen mannen, studievondsten
- Wie is de vader van de moderne biotechnologie?
- Onderscheid Rigor Mortis van een Cadaveric Spasm
- Instrumenten die worden gebruikt in de biologie
- 10 slechtste aanpassingen in het dierenrijk
- Onderzoekers ontwikkelen materialen om geneesmiddelen uit afvalwater te verwijderen
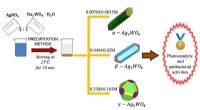
- Verdeel en heers:onderzoekers vinden de sleutel tot het maken van betere medicijnen met minder bijwerkingen

- Gevaarlijk wild gras zal worden gebruikt in batterijen

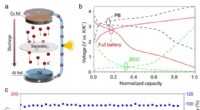
- Constructie van op koolstof gebaseerde celachtige bollen voor robuuste kaliumanode
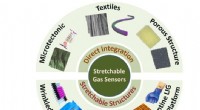
- Onderzoekers ontwikkelen sensoren die menselijke biomarkers en giftig gas detecteren
 Wat is de functie van een spanningsregelaar?
Wat is de functie van een spanningsregelaar?  Hoe klimaatverandering nieuwe epidemieën aan het licht zou kunnen brengen
Hoe klimaatverandering nieuwe epidemieën aan het licht zou kunnen brengen  Kleilagen en verre pompen veroorzaken arseenverontreiniging in het grondwater van Bangladesh
Kleilagen en verre pompen veroorzaken arseenverontreiniging in het grondwater van Bangladesh SpaceXs herstelde kernbooster beschadigd in ruwe zee
SpaceXs herstelde kernbooster beschadigd in ruwe zee Wat is een medische plant?
Wat is een medische plant?  VS voorspellen nog minder orkanen in de Atlantische Oceaan voor 2018
VS voorspellen nog minder orkanen in de Atlantische Oceaan voor 2018 Wat eet of doodt een Tasmaanse duivel?
Wat eet of doodt een Tasmaanse duivel?  Italië, China stelt oplossing voor waterprobleem in het Tsjaadmeer voor
Italië, China stelt oplossing voor waterprobleem in het Tsjaadmeer voor
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

