
Wetenschap
Hoeveel atomen zijn er aanwezig in 18 g C6H12O6?
1. Bereken de molaire massa van C6H12O6:
- C6H12O6 =(6 × 12,01 g/mol C) + (12 × 1,01 g/mol H) + (6 × 16,00 g/mol O)
- Molaire massa =180,16 g/mol
2. Converteer de gegeven massa (18 g) naar mol:
- Mol C6H12O6 =18 g / 180,16 g/mol
- Mol C6H12O6 =0,1 mol
3. Gebruik het getal van Avogadro om het aantal atomen te berekenen:
- Aantal moleculen in 0,1 mol =0,1 mol × 6,022 × 10^23 moleculen/mol
- Aantal moleculen =6,022 × 10^22 moleculen
4. Bepaal het totale aantal atomen in één enkel molecuul C6H12O6:
- C6H12O6 bevat 6 koolstofatomen, 12 waterstofatomen en 6 zuurstofatomen.
- Totaal atomen =6 C + 12 H + 6 O =24 atomen
5. Vermenigvuldig het aantal atomen per molecuul met het aantal moleculen:
- Totaal aantal atomen in 18 g C6H12O6 =24 atomen/molecuul × 6,022 × 10^22 moleculen
- Totaal atomen =1,445 × 10^24 atomen
Daarom zijn er ongeveer 1,445 × 10^24 atomen aanwezig in 18 g C6H12O6.
 Onderzoekers tonen aan dat een kankerverdedigingsmechanisme kan worden teruggedraaid om tumoren aan te vallen
Onderzoekers tonen aan dat een kankerverdedigingsmechanisme kan worden teruggedraaid om tumoren aan te vallen Gericht op verborgen zak voor behandeling van beroerte en epileptische aanvallen
Gericht op verborgen zak voor behandeling van beroerte en epileptische aanvallen Goedkoop organisch materiaal geeft veilige batterijen een langere levensduur
Goedkoop organisch materiaal geeft veilige batterijen een langere levensduur Temperatuur van de aarde Lithosfeer
Temperatuur van de aarde Lithosfeer Houtafval transformeren voor duurzame productie
Houtafval transformeren voor duurzame productie
 Overstromingsschade Canada neemt toe, maar zware regenval neemt af
Overstromingsschade Canada neemt toe, maar zware regenval neemt af Heeft de opwarming van het Noordpoolgebied invloed op het extreme weer in het VK?
Heeft de opwarming van het Noordpoolgebied invloed op het extreme weer in het VK? Projecties voor zeespiegelstijging vertroebeld door antarctische instabiliteit
Projecties voor zeespiegelstijging vertroebeld door antarctische instabiliteit In het oosten van de VS, volwassen bomen passen zich aan en acclimatiseren aan het lokale klimaat
In het oosten van de VS, volwassen bomen passen zich aan en acclimatiseren aan het lokale klimaat Klimaatverandering zal regiospecifieke gevolgen hebben voor de menselijke gezondheid, economie
Klimaatverandering zal regiospecifieke gevolgen hebben voor de menselijke gezondheid, economie
Hoofdlijnen
- Onderzoekers bereiken een parallelle meting van meerdere waterparameters met één sensorchip
- Waarom menselijke cellen identiek?
- Kevers felle kleuren gebruikt voor camouflage in plaats van roofdieren te waarschuwen
- Wat hebben bugs te maken met forensische wetenschap?
- Zijn koralen genetisch uitgerust om de klimaatverandering te overleven?
- Consumenten van neushoornhoorn onthullen waarom alleen legale handel neushoorns niet zal redden
- Wat zijn aanpassingen in planten?
- Het risico op een keizersnede is erfelijk:natuurlijke selectie kan het aantal belemmerde bevallingen niet verminderen
- Wat moet er gebeuren met de DNA-strengen in de kern voordat de cel kan delen?
- Nieuw, duurzame katalysator voor belangrijke brandstofcelreacties kan nuttig zijn in milieuvriendelijke voertuigen

- Onderzoekers bouwen eerste inzetbare, wandelen, zachte robot

- Video:Hoe superhydrofobe materialen volledig droog blijven

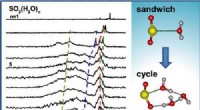
- Wetenschappers onthullen stapsgewijze hydratatiemotieven van zwaveldioxide
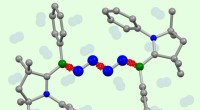
- Inerte stikstof gedwongen om met zichzelf te reageren
 Nieuwe techniek volgt individuele eiwitbeweging op levende cellen
Nieuwe techniek volgt individuele eiwitbeweging op levende cellen Hoe worden mineralen gevormd?
Hoe worden mineralen gevormd?  Cijfers berekenen met gewichten
Cijfers berekenen met gewichten Variabele emissie van het superzware zwarte gat van de Melkweg
Variabele emissie van het superzware zwarte gat van de Melkweg Hoe het gebied in Math te vinden
Hoe het gebied in Math te vinden  Een samengestelde staafgrafiek maken
Een samengestelde staafgrafiek maken  Uruguayaans project gebruikt virtueel geld om recycling van plastic aan te moedigen
Uruguayaans project gebruikt virtueel geld om recycling van plastic aan te moedigen Hydrogel-ondersteund microfluïdisch spinnen van rekbare vezels via vloeiende en grensvlak-zelfaanpassing
Hydrogel-ondersteund microfluïdisch spinnen van rekbare vezels via vloeiende en grensvlak-zelfaanpassing
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

