
Wetenschap
Een anorganische base dissocieert in water in?
Typisch is een anorganische base een verbinding die hydroxide-ionen (OH-) bevat, zoals natriumhydroxide (NaOH) of kaliumhydroxide (KOH). Wanneer deze verbindingen in water oplossen, komen de hydroxide-ionen vrij in de oplossing, wat resulteert in de vorming van vrije OH-ionen in het water. De dissociatie van een anorganische base in water kan worden weergegeven door de volgende algemene vergelijking:
Anorganische base(aq) → Kationen(aq) + Hydroxide-ionen(aq)
Wanneer natriumhydroxide (NaOH) bijvoorbeeld oplost in water, dissocieert het in natriumionen (Na+) en hydroxide-ionen (OH-), zoals weergegeven in de vergelijking:
NaOH(aq) → Na+(aq) + OH-(aq)
Op dezelfde manier, wanneer kaliumhydroxide (KOH) oplost in water, ondergaat het dissociatie in kaliumionen (K+) en hydroxide-ionen (OH-), zoals weergegeven door de vergelijking:
KOH(aq) → K+(aq) + OH-(aq)
Over het geheel genomen brengt de dissociatie van anorganische basen in water het vrijkomen van hydroxide-ionen in de oplossing met zich mee, wat bijdraagt aan de basische eigenschappen en een verhoogde pH van het water.
 Het creëren van lithium-ionbatterijen met een hogere energiedichtheid voor toepassingen op het gebied van hernieuwbare energie
Het creëren van lithium-ionbatterijen met een hogere energiedichtheid voor toepassingen op het gebied van hernieuwbare energie Kleurstoffen uit atmosferische kooldioxide
Kleurstoffen uit atmosferische kooldioxide Hoe worden covalente bindingen bij elkaar gehouden?
Hoe worden covalente bindingen bij elkaar gehouden?  Hoe zet je ethylchloride om in tetraethyllood?
Hoe zet je ethylchloride om in tetraethyllood?  Chemici ontwikkelen MRI-achtige techniek om te detecteren wat er aan de hand is met batterijen
Chemici ontwikkelen MRI-achtige techniek om te detecteren wat er aan de hand is met batterijen
 Feedbacklus die smeltende ijsplaten op West-Antarctica veroorzaakt onthuld
Feedbacklus die smeltende ijsplaten op West-Antarctica veroorzaakt onthuld  De schaaldieren ter wereld worden bedreigd naarmate onze oceanen zuurder worden
De schaaldieren ter wereld worden bedreigd naarmate onze oceanen zuurder worden De bodem is onze beste bondgenoot in de strijd tegen klimaatverandering, maar raakte snel uitgeput
De bodem is onze beste bondgenoot in de strijd tegen klimaatverandering, maar raakte snel uitgeput Nieuwe uitvinding vervoert veilig onbekende, diepwonende vissen naar het oppervlak van de oceanen
Nieuwe uitvinding vervoert veilig onbekende, diepwonende vissen naar het oppervlak van de oceanen Naar huis bellen? Ily vindt de vaste lijn slimmer en gebruiksvriendelijker
Naar huis bellen? Ily vindt de vaste lijn slimmer en gebruiksvriendelijker
Hoofdlijnen
- SARS-CoV-2:Hoe de geschiedenis van menselijke populaties hun immuunrespons beïnvloedt
- Welke evolutionaire betekenis geven wetenschappers deze in groene algen?
- Zijn kleine populieren de toekomst van biobrandstoffen? Studies zeggen ja
- Wil je de bijen redden? Let op ziekteverwekkers en bloemen
- Nieuw onderzoek naar speurhonden kan levens redden
- Hoe krijgt een met veroudering geassocieerd enzym toegang tot ons genetisch materiaal?
- Wat zijn de belangrijkste verschillen tussen plantaardige en dierlijke cellen?
- Nieuwe inzichten helpen verklaren waarom seksuele interacties tussen mensen van hetzelfde geslacht zo belangrijk zijn voor vrouwelijke bonobo's
- Onderzoek naar Siamese tweelingen laat zien hoe de paradox van de Amerikaanse identiteit zich afspeelde in de lichamen van Chang en Eng
- De heilige graal van peptidechemie:peptide-actieve stoffen oraal beschikbaar maken
- Microfluïdische chip kan bijwerkingen van radiotherapie verminderen
- Decodering van de structuur en eigenschappen van nabij-infrarood reflecterende pigmenten
- Een snel en goedkoop apparaat om virussen op te vangen en te identificeren
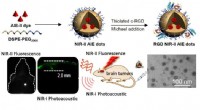
- Nieuwe methode helpt orthotope beeldvorming van hersentumoren duidelijker en sneller te maken
 Waarom worden vaste stoffen geen vloeistoffen genoemd?
Waarom worden vaste stoffen geen vloeistoffen genoemd?  Consumenten:Waarom vind jij wat ik leuk vind leuk, maar niet leuk?
Consumenten:Waarom vind jij wat ik leuk vind leuk, maar niet leuk?  Welke processen kunnen resulteren in de netto beweging van een stof naar de cel als deze geconcentreerder is dan de omgeving?
Welke processen kunnen resulteren in de netto beweging van een stof naar de cel als deze geconcentreerder is dan de omgeving?  Amazon roept op tot overheidsregulering van gezichtsherkenningstechnologie
Amazon roept op tot overheidsregulering van gezichtsherkenningstechnologie Een goedkope, nauwkeurige methode voor het onderzoeken van grondwater
Een goedkope, nauwkeurige methode voor het onderzoeken van grondwater Astronomen ontdekken 83 superzware zwarte gaten in het vroege heelal
Astronomen ontdekken 83 superzware zwarte gaten in het vroege heelal Wetenschapsexperimenten met Gem Stones
Wetenschapsexperimenten met Gem Stones Lijm gevormd uit bijenspuug en bloemenolie zou de basis kunnen vormen van nieuwe lijmen
Lijm gevormd uit bijenspuug en bloemenolie zou de basis kunnen vormen van nieuwe lijmen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

