
Wetenschap
Hoe kun je een chemische reactie sneller laten verlopen?
1. Temperatuur :Het verhogen van de temperatuur van een reactie verhoogt in het algemeen de snelheid van de reactie. Hogere temperaturen leveren meer energie aan de reagerende moleculen, waardoor ze de activeringsenergiebarrière kunnen overwinnen en sneller kunnen reageren. Dit principe staat bekend als de Arrhenius-vergelijking. Houd er echter rekening mee dat extreem hoge temperaturen bij bepaalde reacties enzymen kunnen denatureren of reactanten kunnen ontleden.
2. Concentratie :Het verhogen van de concentratie van de reactanten vergroot de kans op botsingen daartussen, wat leidt tot een hogere frequentie van succesvolle reacties. Bij een hogere concentratie zijn er meer reactantdeeltjes beschikbaar die aan de reactie kunnen deelnemen.
3. Oppervlakte :Door het oppervlak van vaste reactanten te vergroten, wordt het aantal blootgestelde deeltjes dat beschikbaar is voor reactie vergroot. Het vermalen van een vaste stof tot een poeder vergroot bijvoorbeeld het oppervlak en de reactiesnelheid.
4. Katalysatoren :Een katalysator is een stof die de snelheid van een chemische reactie verhoogt zonder tijdens de reactie te worden verbruikt. Katalysatoren bieden een alternatieve reactieroute met een lagere activeringsenergie, waardoor de reactie sneller kan plaatsvinden bij lagere temperaturen en concentraties. Enzymen zijn biologische katalysatoren die een cruciale rol spelen bij het faciliteren van biochemische reacties in levende organismen.
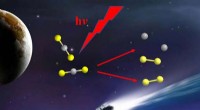
5. Licht :Bij fotochemische reacties wordt lichtenergie geabsorbeerd door reactanten, waardoor ze in een aangeslagen toestand met hogere energie terechtkomen. Dit kan chemische reacties initiëren of versnellen. Fotosynthese in planten is een bekend voorbeeld van een lichtafhankelijke reactie.
6. Druk :Het verhogen van de druk kan de reactiesnelheid verhogen als ten minste één van de reactanten een gas is. Een hogere druk verhoogt de concentratie van gasvormige reactanten, wat leidt tot frequentere botsingen en een hogere reactiesnelheid.
7. Mixen :Efficiënt mengen van reactanten zorgt ervoor dat ze vaker met elkaar in contact komen, waardoor snellere reacties worden bevorderd. Grondig roeren of roeren kan de reactiesnelheid aanzienlijk verbeteren.
Door deze factoren te manipuleren kunnen scheikundigen de snelheden van chemische reacties voor verschillende doeleinden controleren en optimaliseren, zoals industriële processen, de synthese van geneesmiddelen en bio-engineeringtoepassingen.
 De ontwikkeling van bacteriën markeert een nieuw tijdperk in cellulair ontwerp
De ontwikkeling van bacteriën markeert een nieuw tijdperk in cellulair ontwerp Nieuw composiet bevordert lignine als een hernieuwbaar 3D-printmateriaal
Nieuw composiet bevordert lignine als een hernieuwbaar 3D-printmateriaal Met behulp van chitine, een bio-geïnspireerd materiaal, om gereedschappen en schuilplaatsen op Mars te vervaardigen
Met behulp van chitine, een bio-geïnspireerd materiaal, om gereedschappen en schuilplaatsen op Mars te vervaardigen Nieuwe bevindingen helpen bij het ontwerpen van een zeer efficiënte metaaloxidekatalysator voor het verwijderen van ozon
Nieuwe bevindingen helpen bij het ontwerpen van een zeer efficiënte metaaloxidekatalysator voor het verwijderen van ozon Uitvinding van piepkleine organische films kan nieuwe elektronica mogelijk maken
Uitvinding van piepkleine organische films kan nieuwe elektronica mogelijk maken
 We moeten het centrale druktekort gebruiken, geen windsnelheid, orkaanschade voorspellen
We moeten het centrale druktekort gebruiken, geen windsnelheid, orkaanschade voorspellen Azuurblauwe eksters tonen mensachtige vrijgevigheid
Azuurblauwe eksters tonen mensachtige vrijgevigheid  Miljardair Bloomberg zegt $ 15 miljoen toe aan VN voor klimaatverandering
Miljardair Bloomberg zegt $ 15 miljoen toe aan VN voor klimaatverandering In nieuw papier, wetenschappers verklaren klimaatverandering met behulp van voor/na fotografisch bewijs
In nieuw papier, wetenschappers verklaren klimaatverandering met behulp van voor/na fotografisch bewijs Amazonewoud kan worden getraind door grotere variabiliteit in regenval
Amazonewoud kan worden getraind door grotere variabiliteit in regenval
Hoofdlijnen
- Hoe cellen kunstmatige ingrediënten 'lezen' die in een genetisch recept worden gegooid
- Hoe sociaal contact met zieke mieren hun nestgenoten beschermt
- Uit onderzoek blijkt dat het verlies van grote herbivoren de interacties tussen planten en hun natuurlijke vijanden beïnvloedt
- Bevindingen sonde cel samenwerking, massale migratie
- Welk type organisch macromolecuul is glucose?
- Crunchtijd voor voedselzekerheid
- Doe-het-zelf-virussen:hoe virussen zichzelf assembleren
- Onderzoek verklaart waarom hennep en marihuana verschillend zijn
- Onderzoek laat zien hoe tanden functioneerden en evolueerden bij gigantische megahaaien
- Ion biljart cue nieuwe materiaal synthese methode

- Dalian Coherent Light Source onthult de oorsprong van interstellaire disulfur
- Wetenschappers kunnen katalysatoren met één atoom voorspellen en ontwerpen voor belangrijke chemische reacties

- Onderzoeker creëert op hout gebaseerd alternatief voor plastic voor eenmalig gebruik

- In het begin, er was suiker

 Een snelle, gebruiksvriendelijke DNA-amplificatiemethode bij 37 Celsius
Een snelle, gebruiksvriendelijke DNA-amplificatiemethode bij 37 Celsius Notities nemen juryleden beïnvloeden uitspraken, studie vondsten
Notities nemen juryleden beïnvloeden uitspraken, studie vondsten De snelste fictieve ruimteschepen
De snelste fictieve ruimteschepen  GM voegt 700 banen in de VS toe aan fabrieksbouw SUV's
GM voegt 700 banen in de VS toe aan fabrieksbouw SUV's Beelden van het Gemini Observatorium onthullen opvallende details van komeet NEOWISE
Beelden van het Gemini Observatorium onthullen opvallende details van komeet NEOWISE Welke invloed hebben temperatuur en druk op het ideale gas?
Welke invloed hebben temperatuur en druk op het ideale gas?  Makers van gameconsoles verzetten zich tegen Chinese tarieven
Makers van gameconsoles verzetten zich tegen Chinese tarieven De dynamiek van een glimlach in kaart brengen om genderherkenning mogelijk te maken
De dynamiek van een glimlach in kaart brengen om genderherkenning mogelijk te maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

