
Wetenschap
Wat is reactiever c2h4 of c2h6?
Reactiviteit verwijst naar het vermogen van een stof om chemische reacties te ondergaan. Verschillende factoren beïnvloeden de reactiviteit, waaronder:
Hechtsterkte: Zwakkere bindingen worden gemakkelijker verbroken, waardoor moleculen reactiever worden. In het geval van C2H4 en C2H6 is de dubbele C=C-binding in C2H4 zwakker dan de enkele C-C-bindingen in C2H6. Dit betekent dat de kans groter is dat de C=C-binding breekt, waardoor C2H4 reactiever wordt.
Aantal reactieve sites: Hoe meer reactieve plaatsen een molecuul heeft, hoe waarschijnlijker het is dat het reageert. C2H4 heeft twee reactieve plaatsen (de twee koolstofatomen van de dubbele binding), terwijl C2H6 er maar één heeft (het koolstofatoom van de enkele binding). Dit betekent dat C2H4 meer reactiemogelijkheden heeft, waardoor het reactiever wordt.
Stabiliteit: Minder stabiele moleculen zullen eerder reageren om een stabielere toestand te bereiken. C2H4 is minder stabiel dan C2H6 omdat de dubbele binding een hogere energietoestand heeft dan de enkele binding. Dit betekent dat het waarschijnlijker is dat C2H4 reageert om de stabielere enkelvoudige bindingsconfiguratie van C2H6 te bereiken.
Over het geheel genomen maken de zwakkere bindingssterkte, het grotere aantal reactieve plaatsen en de lagere stabiliteit van C2H4 vergeleken met C2H6 C2H4 reactiever. Dit komt tot uiting in het feit dat C2H4 gemakkelijk een grote verscheidenheid aan reacties ondergaat, waaronder additie, polymerisatie en verbranding, terwijl C2H6 relatief niet-reactief is.
 Antivriesvissen inspireren nieuwe cryoprotectanten voor menselijke cellen en weefsels
Antivriesvissen inspireren nieuwe cryoprotectanten voor menselijke cellen en weefsels Nieuwe katalysator voor lagere CO2-uitstoot
Nieuwe katalysator voor lagere CO2-uitstoot Onderzoekers boeken vooruitgang in ontziltingstechnologie
Onderzoekers boeken vooruitgang in ontziltingstechnologie Metaal-organisch raamwerkonderzoek boekt belangrijke vooruitgang in de richting van het verwijderen van pesticiden uit grondwater
Metaal-organisch raamwerkonderzoek boekt belangrijke vooruitgang in de richting van het verwijderen van pesticiden uit grondwater  Een revolutie in kunststoffen:het upcyclen van landbouwafval verhoogt de prestaties en duurzaamheid
Een revolutie in kunststoffen:het upcyclen van landbouwafval verhoogt de prestaties en duurzaamheid
Hoofdlijnen
- Studies beoordelen de haalbaarheid van methoden voor de behandeling van afvalwater in de aquacultuur
- Wat gebeurt er met plasmalogenen, de fosfolipiden waar niemand graag aan denkt
- Onderzoekers ontdekken de onverwachte atomaire structuur van koude- en mentholsensor TRPM8
- Twee hersengebieden werken samen om vinken te helpen weten wanneer en hoe ze hun liedjes moeten afstemmen op specifieke situaties
- Kan een mos helpen bij het opruimen van waterwegen?
- Onderzoekers reconstrueren het genoom van de gemeenschappelijke voorouder van alle zoogdieren
- Reuzenzeebaars heeft meer waarde als levend, onderzeese wonderen ademen dan als commerciële vangst
- Angst voor de dood is van invloed op de manier waarop we stemmen
- Wat gebeurt er in de interfase van de celcyclus?
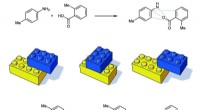
- Een kaart van reacties helpt bij het controleren van moleculaire eigenschappen
- Een methode bij lage temperaturen voor het maken van hoogwaardige thermo-elektrische materialen

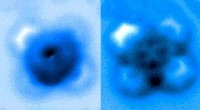
- Team meet het verbreken van een enkele chemische binding
- Asteroïde-inslagen creëren diamantmaterialen met uitzonderlijk complexe structuren

- De keten doorbreken - een groene toekomst voor de chemie katalyseren
 Mensen in de VS en Groot-Brittannië vertonen sterke overeenkomsten in hun houding ten opzichte van nanotechnologieën
Mensen in de VS en Groot-Brittannië vertonen sterke overeenkomsten in hun houding ten opzichte van nanotechnologieën  Een nieuwe micrometer dikke poreuze coating met ongeëvenaarde detectiemogelijkheden voor biomarkers
Een nieuwe micrometer dikke poreuze coating met ongeëvenaarde detectiemogelijkheden voor biomarkers  Rol van mierenzuur in verfafbijtmiddel?
Rol van mierenzuur in verfafbijtmiddel?  Gebruik van Spur Gears
Gebruik van Spur Gears Anti-klimaatspook Trump hangt boven VN-vergadering
Anti-klimaatspook Trump hangt boven VN-vergadering Nanosheet-groeitechniek kan een revolutie teweegbrengen in de productie van nanomaterialen
Nanosheet-groeitechniek kan een revolutie teweegbrengen in de productie van nanomaterialen Een middelzwaar zwart gat verbergt zich in het midden van een gigantische sterrenhoop
Een middelzwaar zwart gat verbergt zich in het midden van een gigantische sterrenhoop Hoe kan de pH van invloed zijn op uw vissen?
Hoe kan de pH van invloed zijn op uw vissen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

