
Wetenschap
Welke factor is de belangrijkste die bepaalt of water een vaste vloeistof of een gas is?
Hier ziet u hoe de temperatuur de toestand van het water beïnvloedt:
1. Vast (ijs): Bij temperaturen onder 0 °C (32 °F) hebben watermoleculen een lage kinetische energie en worden ze bij elkaar gehouden door sterke waterstofbruggen. Ze vormen een stijve kristallijne structuur, wat resulteert in de vaste toestand die bekend staat als ijs.
2. Vloeistof (water): Naarmate de temperatuur boven 0°C (32°F) stijgt, neemt de gemiddelde kinetische energie van watermoleculen toe. Dit verzwakt de waterstofbruggen, waardoor de moleculen vrijer kunnen bewegen. Bij kamertemperatuur bevindt water zich in vloeibare toestand, waarbij de moleculen dicht bij elkaar zijn maar niet stevig op hun plaats zijn gefixeerd.
3. Gas (waterdamp): Wanneer water op zeeniveau tot 100°C (212°F) wordt verwarmd, bereikt het zijn kookpunt. Bij deze temperatuur wordt de kinetische energie van watermoleculen hoog genoeg om de waterstofbruggen volledig te overwinnen. De moleculen ontsnappen uit de vloeistof en transformeren in een gasvormige toestand, bekend als waterdamp.
Daarom speelt temperatuur een cruciale rol bij het bepalen van de fysieke toestand van water, waardoor het verandert van vast (ijs) naar vloeibaar (water) en uiteindelijk naar gas (waterdamp) naarmate de temperatuur stijgt.
 Neutralisatie van pathogene schimmels met immunotherapeutica met kleine moleculen
Neutralisatie van pathogene schimmels met immunotherapeutica met kleine moleculen Wat zou er gebeuren als je een monster zwavel probeert af te breken?
Wat zou er gebeuren als je een monster zwavel probeert af te breken?  Is het mogelijk om anti-aromaticiteit te ontwikkelen door niet-benzenoïde aromatische verbindingen?
Is het mogelijk om anti-aromaticiteit te ontwikkelen door niet-benzenoïde aromatische verbindingen? Als 0,500 mol van een niet-elektrolytische opgeloste stof wordt opgelost in 500,0 g ether, wat is dan de vriespuntoplossing?
Als 0,500 mol van een niet-elektrolytische opgeloste stof wordt opgelost in 500,0 g ether, wat is dan de vriespuntoplossing?  Veelbelovende ontdekking zou kunnen leiden tot een betere, goedkopere zonnecel
Veelbelovende ontdekking zou kunnen leiden tot een betere, goedkopere zonnecel
 De geschiedenis van de Australische vegetatie uitleggen
De geschiedenis van de Australische vegetatie uitleggen Toenemende dominantie van diatomeeën in het estuarium van de Pearl River
Toenemende dominantie van diatomeeën in het estuarium van de Pearl River NASA werpt een infrarood oog op tropische storm Kujiras, zeer koude wolkentoppen
NASA werpt een infrarood oog op tropische storm Kujiras, zeer koude wolkentoppen Veranderingen in jetstream kunnen extreme weersomstandigheden tegen 2060 versterken
Veranderingen in jetstream kunnen extreme weersomstandigheden tegen 2060 versterken Textiel dat zich ontwikkelt om aan de vraag naar duurzame materialen te voldoen
Textiel dat zich ontwikkelt om aan de vraag naar duurzame materialen te voldoen
Hoofdlijnen
- Welke term beschrijft een proces dat alleen plaatsvindt in meercellige organismen en waarbij cellen verschillende gespecialiseerde functies hebben?
- Nieuwe minimaal invasieve procedure redt het leven van honden - en haar nier
- Meer wolfachtig worden is de sleutel tot de toekomst voor coyotes
- Wat is een lichaamsdeel dat begint met elke letter van het alfabet, waarvan er minstens één letter is?
- Bacteriën met synthetisch gencircuit zelf-assembleren om werkend apparaat te bouwen met gouden nanodeeltjes
- Baby bongo geboren, waarschijnlijk binnenkort in Species Survival Center
- Hoe planten een gevaarlijke wereld van ziekteverwekkers afweren
- Aziatische bossen tonen veerkracht ondanks toenemende verstoringen als gevolg van klimaatverandering en menselijke activiteiten
- Een nieuw quarantaineschema zou het risico op herintroductie van hondsdolheid in de EU na de Russische invasie kunnen verminderen, zo blijkt uit onderzoek
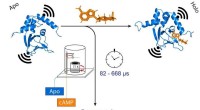
- Onderzoekers onderzoeken structurele veranderingen in snel ingevroren eiwitten
- Klittenbandachtige voedselsensor detecteert bederf en besmetting

- Een nieuwe betaalbare en gebruiksvriendelijke technologie voor de diagnose van droge ogen

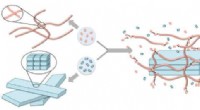
- Moleculaire steigers helpen constructie op nanoschaal
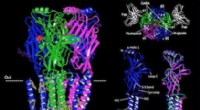
- Structuur van de belangrijkste hersenreceptor die het behandeldoel is voor epilepsie, angst opgelost
 Verbleking en veerkracht:kunnen riffen overleven?
Verbleking en veerkracht:kunnen riffen overleven?  Westelijke wind op zuidelijk halfrond zal waarschijnlijk toenemen naarmate het klimaat warmer wordt
Westelijke wind op zuidelijk halfrond zal waarschijnlijk toenemen naarmate het klimaat warmer wordt Begrijpen hoe elektronen chemische reacties aansturen
Begrijpen hoe elektronen chemische reacties aansturen  Hoe je veilige ruimtes kunt creëren met en voor zwarte meisjes
Hoe je veilige ruimtes kunt creëren met en voor zwarte meisjes  Waarom retourzendingen van klanten ertoe leiden dat bedrijven geld verliezen
Waarom retourzendingen van klanten ertoe leiden dat bedrijven geld verliezen  Welke kan chemisch worden ontleed natriumethanol, sucrose of water?
Welke kan chemisch worden ontleed natriumethanol, sucrose of water?  Wat is de term voor het maximale aantal individuen dat een ecosysteem kan ondersteunen?
Wat is de term voor het maximale aantal individuen dat een ecosysteem kan ondersteunen?  Anatomische structuren: homoloog, analoog & vestigiaal
Anatomische structuren: homoloog, analoog & vestigiaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

