
Wetenschap
Hoeveel dubbele bindingen in een koolstofmolecuul?
Koolstofmoleculen kunnen een variërend aantal dubbele bindingen hebben, afhankelijk van het specifieke molecuul en zijn structuur. Alkenen zijn bijvoorbeeld koolwaterstoffen die ten minste één dubbele koolstof-koolstofbinding bevatten. Het aantal dubbele bindingen in een koolstofmolecuul kan variëren van één tot meerdere, afhankelijk van de grootte en complexiteit van het molecuul. Etheen (C2H4) heeft bijvoorbeeld één dubbele binding, terwijl butadieen (C4H6) twee dubbele bindingen heeft. Bovendien kunnen sommige koolstofmoleculen meerdere dubbele bindingen hebben, zoals benzeen (C6H6), dat drie dubbele bindingen heeft. Het aantal dubbele bindingen in een koolstofmolecuul beïnvloedt de chemische eigenschappen en reactiviteit ervan.
 Wat is het smeltpunt van magnesiumsulfaat met heptahydraat?
Wat is het smeltpunt van magnesiumsulfaat met heptahydraat?  Nieuw opgeloste structuur onthult hoe cellen zuurstofschade weerstaan
Nieuw opgeloste structuur onthult hoe cellen zuurstofschade weerstaan  Wat is de uitgebalanceerde vergelijking voor de verbranding van heptaan in reactie met zuurstof?
Wat is de uitgebalanceerde vergelijking voor de verbranding van heptaan in reactie met zuurstof?  Video:Hoe de houdbaarheidsdatum van medicijnen werkt
Video:Hoe de houdbaarheidsdatum van medicijnen werkt Ook na handen wassen, nieuwe vingerafdruktest kan onderscheid maken tussen personen die heroïne hebben gebruikt of gebruikt
Ook na handen wassen, nieuwe vingerafdruktest kan onderscheid maken tussen personen die heroïne hebben gebruikt of gebruikt
 Dieren van het bamboebos
Dieren van het bamboebos  Algen:vijverschuim of voedsel van de toekomst?
Algen:vijverschuim of voedsel van de toekomst?  De koudegolf in de VS was een speling van de natuur, snelle analyse vindt
De koudegolf in de VS was een speling van de natuur, snelle analyse vindt Joshua-bomen met uitsterven bedreigd
Joshua-bomen met uitsterven bedreigd Werken aan betere aanbevelingen over hoe biodiversiteit kan worden benut om de levering van ecosysteemdiensten te bevorderen
Werken aan betere aanbevelingen over hoe biodiversiteit kan worden benut om de levering van ecosysteemdiensten te bevorderen
Hoofdlijnen
- Onderzoekers ontdekken hoe het Zika-virus zijn gastheercel hermodelleert om de virale productie te stimuleren
- Hoe natuurlijke selectie werkt
- Hoe transcriptie epigenetische silencing oplevert
- Onderzoekers genereren tomaten met verbeterde antioxiderende eigenschappen door genetische manipulatie
- Jonge, koelbloedige dieren lijden het meest door de opwarming van de aarde, blijkt uit onderzoek
- Kuikenembryo's leveren waardevolle genetische gegevens voor het begrijpen van de menselijke ontwikkeling
- Een kungfu-kick leidde onderzoekers naar 's werelds oudste complete visfossielen. Dit is wat ze hebben gevonden
- Wat zijn endorfines?
- Onderzoekers laten zien hoe de voedselkeuze van insecten kan worden gemanipuleerd
- Complexe moleculen samenstellen

- Wetenschappers hebben de diversiteit van koolwaterstofmoleculen verklaard door hun magie

- niet giftig, biologisch afbreekbaar orthopedisch implantaat kan superieure ondersteuning bieden aan beschadigde botten
- De weg vrijmaken voor zuinige meststoffen
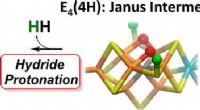
- Hoe efficiënte organische zonnecellen te bouwen?

 Hoe SCM naar SCF
Hoe SCM naar SCF Klimaatsystemen in musea blijken te streng gereguleerd
Klimaatsystemen in musea blijken te streng gereguleerd Geeft het aantal neutronen in de kern een atoom een unieke chemische aard?
Geeft het aantal neutronen in de kern een atoom een unieke chemische aard?  Onderzoeksteam demonstreert coherente, ultrasnelle foto-emissie van de emitter van koolstofnanobuisjes
Onderzoeksteam demonstreert coherente, ultrasnelle foto-emissie van de emitter van koolstofnanobuisjes  Wetenschappers ontwikkelen detectoren op basis van synthetische diamanten voor CERN
Wetenschappers ontwikkelen detectoren op basis van synthetische diamanten voor CERN Ionenstralen betekenen een kwantumsprong voor qubits met kleurcentrum
Ionenstralen betekenen een kwantumsprong voor qubits met kleurcentrum Welk zuur moet je gebruiken voor goudtest zout- en zwavelzuur?
Welk zuur moet je gebruiken voor goudtest zout- en zwavelzuur?  Deze robocalls willen niet met je praten, ze willen gewoon dat je terugbelt, FCC zegt:
Deze robocalls willen niet met je praten, ze willen gewoon dat je terugbelt, FCC zegt:
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

