
Wetenschap
Veranderingen in druk hebben, meer nog dan temperatuur, een sterke invloed op hoe snel vloeistoffen in gas veranderen
Effect van druk:
* Lagere druk, snellere verdamping: Wanneer de druk rond een vloeistof afneemt, daalt ook het kookpunt van de vloeistof. Dit betekent dat de moleculen van de vloeistof minder energie nodig hebben om de intermoleculaire krachten die ze bij elkaar houden te overwinnen en naar de gasfase te ontsnappen. Als gevolg hiervan vindt verdamping sneller plaats bij lagere drukken.
* Hogere druk, langzamere verdamping: Omgekeerd, wanneer de druk toeneemt, neemt het kookpunt van de vloeistof toe. De hogere druk biedt meer weerstand tegen het losbreken van de moleculen van de vloeistof, waardoor hun ontsnapping naar de gasfase wordt belemmerd. Daarom vertraagt de verdamping bij hogere drukken.
Effect van temperatuur:
* Hogere temperatuur, snellere verdamping: Naarmate de temperatuur stijgt, neemt ook de gemiddelde kinetische energie van de vloeistofmoleculen toe. Deze hogere energie betekent dat de moleculen een grotere neiging hebben om sneller te bewegen en de intermoleculaire krachten te overwinnen die ze bij elkaar houden. Hierdoor vindt verdamping sneller plaats bij hogere temperaturen.
* Lagere temperatuur, langzamere verdamping: Omgekeerd, wanneer de temperatuur daalt, neemt de gemiddelde kinetische energie van de vloeistofmoleculen af. Door de verminderde energie is het minder waarschijnlijk dat de moleculen zich losmaken van de intermoleculaire krachten, waardoor het verdampingsproces wordt vertraagd.
Dus hoewel zowel druk als temperatuur een rol spelen bij de verdampingssnelheid van vloeistoffen, hebben veranderingen in druk een sterkere invloed dan veranderingen in temperatuur. In praktische termen betekent dit dat het verlagen van de druk rond een vloeistof de verdampingssnelheid dramatisch kan verhogen, zelfs bij dezelfde temperatuur, terwijl het verhogen van de druk de verdamping aanzienlijk kan vertragen.
 Groene waterstof produceren door blootstelling van nanomaterialen aan zonlicht
Groene waterstof produceren door blootstelling van nanomaterialen aan zonlicht Nieuw systeem maakt snel, antibioticabehandelingen op maat mogelijk
Nieuw systeem maakt snel, antibioticabehandelingen op maat mogelijk Nieuwe ontdekking van plastic coatings geeft meer functionaliteit aan 3D-printen
Nieuwe ontdekking van plastic coatings geeft meer functionaliteit aan 3D-printen  Nieuwe microscooptechniek onthult interne structuur van levende embryo's
Nieuwe microscooptechniek onthult interne structuur van levende embryo's Een stap dichter bij biotechnologische vervangingen voor vaten en kanalen
Een stap dichter bij biotechnologische vervangingen voor vaten en kanalen
 Hoe maak je klimaatactie populair
Hoe maak je klimaatactie populair Impact van kolenverbranding op de Yangtze-rivier is vergelijkbaar met natuurlijke processen
Impact van kolenverbranding op de Yangtze-rivier is vergelijkbaar met natuurlijke processen Onderzoek identificeert hotspots van schendingen van de waterkwaliteit
Onderzoek identificeert hotspots van schendingen van de waterkwaliteit Koolstofterugkoppeling van bosbodems zal de opwarming van de aarde versnellen, 26-jarige studieprojecten
Koolstofterugkoppeling van bosbodems zal de opwarming van de aarde versnellen, 26-jarige studieprojecten Satellietgegevens gebruiken om mensen te waarschuwen voor vulkaanuitbarstingen
Satellietgegevens gebruiken om mensen te waarschuwen voor vulkaanuitbarstingen
Hoofdlijnen
- Wat is een molecuul dat wordt geproduceerd door DNA uit twee verschillende bronnen te combineren?
- Niveaus van celorganisatie
- Roze + roze =goud? De veren van hybride kolibries komen niet overeen met die van zijn ouders
- De motivaties van mensen beïnvloeden de manier waarop ze informatie verzamelen
- Hoe een moleculair signaal plantencellen helpt beslissen wanneer ze olie moeten maken
- Ryk heeft een begeleider nodig
- Biomassa versus energiepiramides
- Effecten van de microscoop op Science
- Genetisch manipulatiemechanisme gevisualiseerd
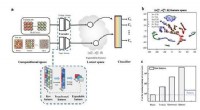
- Kristalstructuurvoorspelling van willekeurige legering met meerdere elementen
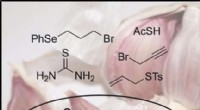
- Korte totale synthese van ajoen, een biologisch actieve component in olie-extracten van knoflook
- Een betere beoordeling van de gevoeligheid van bacteriën voor antibiotica kan de manier waarop medicijnen worden voorgeschreven veranderen

- Studie van zouten in water die opschudding veroorzaken

- Nieuw onderzoek toont de beperkingen van coördinatie in de chemie aan

 Ruimte-orkaan voor het eerst waargenomen
Ruimte-orkaan voor het eerst waargenomen Wat veroorzaakt ondergrondse thermohaliene vooroordelen in de nieuwste klimaatmodellen van de zuidelijke tropische Stille Oceaan?
Wat veroorzaakt ondergrondse thermohaliene vooroordelen in de nieuwste klimaatmodellen van de zuidelijke tropische Stille Oceaan?  Hoe SpaceShipOne werkt
Hoe SpaceShipOne werkt  Nanodraad gemaakt van verschillende materialen kan verkoopbaar worden
Nanodraad gemaakt van verschillende materialen kan verkoopbaar worden Blootstelling aan Tsjernobyl verandert de darmbacteriën van wilde dieren
Blootstelling aan Tsjernobyl verandert de darmbacteriën van wilde dieren Ruimte verenigt ons:eerste Iraans-Amerikaanse astronaut reikt naar sterren
Ruimte verenigt ons:eerste Iraans-Amerikaanse astronaut reikt naar sterren Feiten en verhalen:geweldige verhalen ondermijnen sterke feiten
Feiten en verhalen:geweldige verhalen ondermijnen sterke feiten NASA berekent kletsnatte regenval in tropische depressie Cristobal
NASA berekent kletsnatte regenval in tropische depressie Cristobal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

