
Wetenschap
Door licht geactiveerde moleculaire machines richten zich op antibioticaresistentie
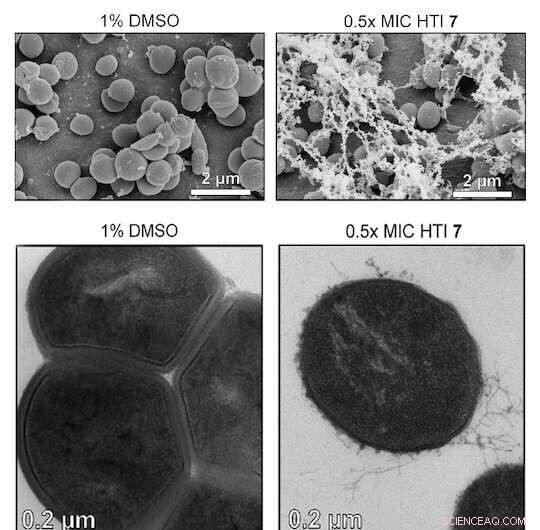
Krediet:Geavanceerde wetenschap (2022). DOI:10.1002/advs.202203242
Een nieuwe klasse van gemotoriseerde moleculen die specifieke bacteriën doden, belooft de dreiging van antibioticaresistentie voor de menselijke gezondheid te beteugelen.
Wetenschappers van Rice University leidden een team dat door licht geactiveerde hemithioindigo (HTI) -moleculen ontwikkelde die Gram-positieve bacteriën en de biofilms die ze vormen vernietigen. De moleculen doen dit door de lokale generatie van reactieve zuurstofsoorten (ROS) te versterken die medicijnresistente cellen chemisch aanvallen en vernietigen.
De nieuwe moleculen verschillen van, en zijn complementair aan, andere die bij Rice zijn gemaakt en die ook door licht worden geactiveerd, maar in celmembranen boren om ze te doden.
Net als de oefeningen op basis van Nobelprijswinnend werk van Bernard Feringa, worden de HTI-gebaseerde moleculen geactiveerd door zichtbaar licht in plaats van door schadelijke ultraviolette straling.
Beide zijn producten van Rice chemicus James Tour en zijn collega's. Rice-alumni Ana Santos, een postdoctoraal internationaal fellow bij het Health Research Institute of the Balearic Islands in Palma, Spanje, en Alexis van Venrooy, nu een senior scientist bij Genesis Therapeutics, San Diego, zijn co-hoofdauteurs van de nieuwe studie in Geavanceerde wetenschap .
De op HTI gebaseerde moleculaire machines bestaan uit twee helften:een thio-indigo-eenheid die via een centrale dubbele koolstofbinding aan een carbocyclus is gekoppeld. Wanneer geactiveerd door zichtbaar licht, ondergaat het molecuul een conformationele verandering die resulteert in ofwel een boorachtige beweging van 360 graden of een verschuiving tussen twee conformaties, zoals een "aan/uit"-schakelaar, afhankelijk van het moleculaire ontwerp.
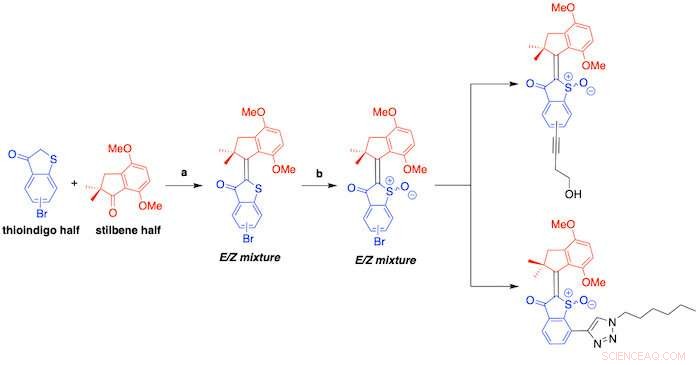
Een schema toont de synthese van hemithioindigos beschreven in een nieuwe studie onder leiding van Rice-onderzoekers. De moleculaire motoren worden geactiveerd door zichtbaar licht en doden schadelijke bacteriën door reactieve zuurstofsoorten te genereren. Credit:de reisgroep
Tijdens het proces reageren geactiveerde HTI's met de cel en moleculaire zuurstof, waarbij elektronen worden overgedragen om ROS te produceren die de doelcellen aantasten.
"Deze doden geen cellen door de membranen mechanisch open te scheuren zoals de eerdere doen," zei Tour. "Ze veroorzaken voldoende verstoring zodat reactieve zuurstofsoorten en vrije radicalen worden gegenereerd en uiteindelijk de cellen doden.
"Dus het is niet de snelle necrotische dood die we eerder zagen," zei hij. "Het is een beetje langzamer, maar het is extreem efficiënt."
"Een belangrijk voordeel van deze moleculen is dat ze een smal werkingsspectrum hebben en selectief een specifieke groep bacteriën, Gram-positieve bacteriën, doden," zei Santos. "Daarom veroorzaken ze minder vaak de bijwerkingen die worden gezien bij breedspectrumantibiotica die zonder onderscheid zowel 'slechte' als 'goede' bacteriën doden, en ze leiden ook minder snel tot resistentie omdat slechts één groep bacteriën wordt aangetast. "
Gram-positieve bacteriën missen een buitenmembraan (hoewel ze een dikke peptidoglycaanlaag hebben), en dit lijkt ze vatbaarder te maken voor ROS die hun celwanden oxideren en afbreken.
De onderzoekers testten verschillende HTI-varianten op zeven Gram-positieve bacteriestammen en ontdekten dat het molecuul ze allemaal doodde in de aanwezigheid van licht. (HTI's waren minder effectief tegen Gram-negatieve bacteriën, vermoedelijk omdat hun dubbele membraan voorkomt dat HTI de cel binnendringt. Maar door ze te permeabiliseren met een Tris-EDTA-bufferoplossing was de kans groter dat ze door HTI's werden gedood.)
Ze legden ook kolonies van Staphylococcus aureus bloot met en zonder de aanwezigheid van ROS-scavengers en ontdekten dat die met de aaseters de effectiviteit van de hemithioindigo-moleculen beknotten. Zonder aaseters had de ROS het gewenste effect op bacteriën.
De studie toonde aan dat HTI's ook antibiotica-tolerante persistente cellen van verschillende Gram-positieve stammen in slechts 25 minuten doodden, sneller dan conventionele antibiotica. In alle gevallen verhoogde herhaalde blootstelling aan HTI's de weerstand van de bacteriën tegen behandeling niet.
Omdat de behandeling gebaseerd is op ROS in plaats van op mechanische actie, is het niet schadelijk voor zoogdiercellen, zei Santos. "Dit maakt de weg vrij voor een nieuwe antimicrobiële therapie die zich veilig kan richten op Gram-positieve pathogenen die geassocieerd zijn met huidinfecties zoals brandwonden," zei ze.
"De resultaten helpen ook ons begrip van moleculaire machines in het algemeen te verdiepen door aan te tonen dat ze niet allemaal volgens dezelfde mechanismen werken en dat verschillen in de chemische kern van het molecuul kunnen leiden tot zeer verschillende biologische acties." + Verder verkennen
Bacteriëndodende nano-drills krijgen een upgrade:zichtbaar licht activeert moleculaire machines om infecties te behandelen
 Wat hebben lieveheersbeestjes nodig om te leven?
Wat hebben lieveheersbeestjes nodig om te leven?  Tropische storm Lidia laat vier doden achter in Mexico
Tropische storm Lidia laat vier doden achter in Mexico Ontwikkeling bedreigt tropische bossen, onderzoekers zeggen:
Ontwikkeling bedreigt tropische bossen, onderzoekers zeggen: Waarom op zoek waren naar chemicaliën in de zeebodem om klimaatverandering te helpen voorspellen?
Waarom op zoek waren naar chemicaliën in de zeebodem om klimaatverandering te helpen voorspellen? Lekken zijn verantwoordelijk voor de helft van de belangrijkste methaanbronnen bij het grootste Amerikaanse olieveld:studie
Lekken zijn verantwoordelijk voor de helft van de belangrijkste methaanbronnen bij het grootste Amerikaanse olieveld:studie
Hoofdlijnen
- Welk type RNA draagt aminozuren naar de vertaalsite?
- Waarom is diffusie belangrijk voor het leven van een cel?
- Waarom wordt magnesiumchloride gebruikt in PCR?
- Genoomgrootte beïnvloedt of planten invasief worden
- Onderzoek onthult geheimen van de ratrace van inheemse knaagdieren naar nieuwe landen
- Chimpansees bleken arm- en monduitdrukkingen te gebruiken om afstand over te brengen
- Actief transport: een overzicht van primair en secundair
- Gymnospermen: definitie, levenscyclus, typen en voorbeelden
- Onderzoekers ontdekken slecht begrepen bacteriële lijnen in de monden van dolfijnen
- Onderzoekers ontdekken drukgeïnduceerd polyamorfisme in dicht zwaveldioxide

- Lab verandert fluorescerende tags in kankermoordenaars
- Neutronen wijzen de weg naar geoptimaliseerde crashtolerante auto's

- Het toevoegen van een inert polymeer aan plastic zonnecellen zorgt voor een hoog rendement en eenvoudige productie

- Met molybdeen gecoate katalysator splitst water efficiënter voor waterstofproductie

 Sociale media opschonen met machine learning
Sociale media opschonen met machine learning Reclame-ellende trof NY Times, naarmate digitale abonnementen groeien
Reclame-ellende trof NY Times, naarmate digitale abonnementen groeien Global Gaia-campagne onthult geheimen van stellair paar
Global Gaia-campagne onthult geheimen van stellair paar Het beoordelen van nieuwsbronnen kan de verspreiding van verkeerde informatie helpen beperken
Het beoordelen van nieuwsbronnen kan de verspreiding van verkeerde informatie helpen beperken Het in kaart brengen van de snelwegen die door de eerste Australiërs werden afgelegd
Het in kaart brengen van de snelwegen die door de eerste Australiërs werden afgelegd Wetenschappers tonen aan dat grafeen zeer efficiënt is in het omzetten van licht in elektriciteit
Wetenschappers tonen aan dat grafeen zeer efficiënt is in het omzetten van licht in elektriciteit Onderzoekers zoeken naar bestaan van exotisch kwantumspin-ijs
Onderzoekers zoeken naar bestaan van exotisch kwantumspin-ijs Weer een dagje aan het werk, in het oog van een orkaan
Weer een dagje aan het werk, in het oog van een orkaan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

