
Wetenschap
Tatoeage gemaakt van gouden nanodeeltjes zorgt voor een revolutie in de medische diagnostiek
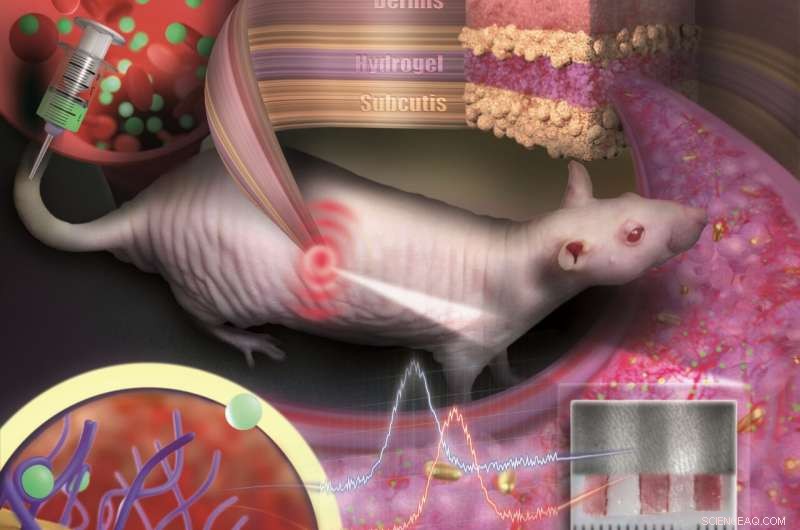
Gouden nanodeeltjes ingebed in een poreuze hydrogel kunnen onder de huid worden geïmplanteerd en als medische sensoren worden gebruikt. De sensor is als een onzichtbare tatoeage die concentratieveranderingen van stoffen in het bloed door kleurverandering onthult. Krediet:Nanobiotechnology Group, JGU Afdeling Chemie
Het idee van implanteerbare sensoren die continu informatie doorgeven over vitale waarden en concentraties van stoffen of medicijnen in het lichaam, fascineert artsen en wetenschappers al lang. Dergelijke sensoren maken een constante monitoring van ziekteprogressie en therapeutisch succes mogelijk. Echter, tot nu, implanteerbare sensoren zijn niet geschikt om permanent in het lichaam te blijven en moeten na een paar dagen of weken worden vervangen.
Er is ook het probleem van implantaatafstoting, aangezien het immuunsysteem de sensor als een vreemd voorwerp herkent. Met veel technologieën, de kleur van de sensor, wat wijst op concentratieveranderingen, is onstabiel en vervaagt na verloop van tijd. Wetenschappers van de Johannes Gutenberg University Mainz (JGU) hebben een nieuw type implanteerbare sensor ontwikkeld die gedurende enkele maanden in het lichaam kan worden geïmplanteerd. De sensor is gebaseerd op kleurstabiele gouden nanodeeltjes die zijn gemodificeerd met receptoren voor specifieke moleculen. Ingebed in een kunstmatig polymeer weefsel, de nanogold wordt onder de huid geïmplanteerd, waar het veranderingen in medicijnconcentraties meldt door de kleur te veranderen.
De onderzoeksgroep van professor Carsten Soennichsen bij JGU gebruikt al jaren gouden nanodeeltjes als sensoren om kleine hoeveelheden eiwitten in microscopisch kleine stroomcellen te detecteren. Gouden nanodeeltjes fungeren als kleine antennes voor licht:ze absorberen en verstrooien het sterk, en zien er kleurrijk uit. Ze reageren op veranderingen in hun omgeving door van kleur te veranderen. Het team van Soennichsen heeft dit concept gebruikt voor geïmplanteerde medische detectie.
Om te voorkomen dat de kleine deeltjes zich verspreiden of worden afgebroken door immuuncellen, ze zijn ingebed in een poreuze hydrogel met een weefselachtige consistentie. Eenmaal onder de huid geïmplanteerd, kleine bloedvaten en cellen groeien in de poriën. De sensor is geïntegreerd in het weefsel en wordt niet als vreemd lichaam afgewezen. "Onze sensor is als een onzichtbare tatoeage, niet veel groter dan een cent en dunner dan een millimeter, " zei professor Carsten Soennichsen, hoofd van de Nanobiotechnology Group bij JGU. Omdat de gouden nanodeeltjes worden gereflecteerd in de infrarode golflengte, ze zijn niet zichtbaar voor het oog. Echter, een speciaal soort meetapparaat kan hun kleur niet-invasief door de huid detecteren.
In hun studie gepubliceerd in Nano-letters , de JGU-onderzoekers implanteerden hun gouden nanodeeltjessensoren onder de huid van haarloze ratten. Kleurveranderingen in deze sensoren werden gevolgd na toediening van verschillende doses antibioticum. De medicijnmoleculen werden via de bloedbaan naar de sensor getransporteerd. Door zich te binden aan specifieke receptoren op het oppervlak van de gouden nanodeeltjes, ze veroorzaken kleurverandering die afhankelijk is van de geneesmiddelconcentratie. Dankzij de kleurstabiele gouden nanodeeltjes en de weefselintegrerende hydrogel, de sensor bleek gedurende meerdere maanden mechanisch en optisch stabiel te blijven.
"We zijn eraan gewend dat gekleurde objecten na verloop van tijd verbleken. Gouden nanodeeltjes, echter, niet bleken, maar behouden hun kleur permanent. Omdat ze gemakkelijk kunnen worden gecoat met verschillende receptoren, ze zijn een ideaal platform voor implanteerbare sensoren, " verklaarde Dr. Katharina Kaefer, eerste auteur van de studie.
Het nieuwe concept is generaliseerbaar en heeft het potentieel om de levensduur van implanteerbare sensoren te verlengen. In de toekomst, op gouden nanodeeltjes gebaseerde implanteerbare sensoren kunnen worden gebruikt om gelijktijdig concentraties van biomarkers of medicijnen in het lichaam te observeren. Dergelijke sensoren kunnen worden toegepast bij de ontwikkeling van geneesmiddelen, medisch onderzoek of gepersonaliseerde geneeskunde, zoals de behandeling van chronische ziekten.
Soennichsen kwam in 2004 op het idee om gouden nanodeeltjes te gebruiken als geïmplanteerde sensoren. toen hij zijn onderzoek in de biofysische chemie begon als junior professor in Mainz. Echter, het project werd pas 10 jaar later gerealiseerd in samenwerking met Dr. Thies Schroeder en Dr. Katharina Kaefer, beide wetenschappers van JGU. Schroeder had ervaring met biologisch onderzoek en proefdierwetenschap en had al enkele jaren onderzoekswerk in de V.S.
Kaefer was op zoek naar een spannend onderwerp voor haar doctoraat en was vooral geïnteresseerd in het complexe en interdisciplinaire karakter van het project. De eerste resultaten leidden tot een stipendium dat aan Kaefer werd toegekend door het Max Planck Graduate Center (MPGC) en tot financiële steun van Stiftung Rheinland-Pfalz für Innovation. “Zo’n project vraagt om veel mensen met verschillende wetenschappelijke achtergronden. Stap voor stap, konden we steeds meer mensen overtuigen van ons idee, " zei Soennichsen. Uiteindelijk, het was interdisciplinair teamwerk dat resulteerde in de succesvolle ontwikkeling van de eerste functionele geïmplanteerde sensor met gouden nanodeeltjes.
 Methoden voor het bepalen van de pH in pH-papier
Methoden voor het bepalen van de pH in pH-papier  Nikkelferriet bevordert de capaciteit en cyclusstabiliteit van lithium-zwavelbatterijen
Nikkelferriet bevordert de capaciteit en cyclusstabiliteit van lithium-zwavelbatterijen Wat is een mol?
Wat is een mol?  Door kwallen geïnspireerde elektronische huid gloeit als hij pijn doet
Door kwallen geïnspireerde elektronische huid gloeit als hij pijn doet Onderzoekers ontwikkelen semi-vloeibare metaalanode voor batterijen van de volgende generatie
Onderzoekers ontwikkelen semi-vloeibare metaalanode voor batterijen van de volgende generatie
 Studie onderzoekt hoe gesteente zich uitbreidt in de buurt van het bodemoppervlak in de zuidelijke Sierra Nevada
Studie onderzoekt hoe gesteente zich uitbreidt in de buurt van het bodemoppervlak in de zuidelijke Sierra Nevada De Indonesische Merapi-vulkaan ontketent een rivier van lava
De Indonesische Merapi-vulkaan ontketent een rivier van lava Met behulp van gegevens uit de echte wereld, wetenschappers beantwoorden belangrijke vragen over een atmosferische release
Met behulp van gegevens uit de echte wereld, wetenschappers beantwoorden belangrijke vragen over een atmosferische release Californië stelt strenge limiet voor giftige chemicaliën in drinkwater voor
Californië stelt strenge limiet voor giftige chemicaliën in drinkwater voor Sneeuwsmelt veroorzaakt een seismische zwerm in de buurt van Long Valley Caldera in Californië
Sneeuwsmelt veroorzaakt een seismische zwerm in de buurt van Long Valley Caldera in Californië
Hoofdlijnen
- Oorzaken van Cytoplasmic Streaming
- Angiospermen: definitie, levenscyclus, soorten en voorbeelden
- Competitie (biologie): definitie, types en voorbeelden
- Prehistorische soa's kunnen de reden zijn waarom mensen monogaam werden
- mRNA: definitie, functie en structuur
- Hoe het plasmamembraan regelt wat er in komt en uit een cel komt
- Het grote structurele voordeel Eukaryoten hebben over prokaryoten
- Wetenschappers identificeren nieuwe gastheren voor vectoren van de ziekte van Chagas
- Algen kunnen planeet voeden en voeden met behulp van nieuwe hightech tool
- Hoe maak je een perfecte zonneabsorber?

- Ziektekiemen verdwijnen:nieuwe nanotechnologie zorgt ervoor dat bacteriën zich niet aan oppervlakken hechten
- Beheersing van de eigenschappen van materie in tweedimensionale kristallen

- Ultrahoge thermische isolatie over heterogeen gelaagde tweedimensionale materialen
- Nanostructureringstechnologie zorgt voor energiezuinige en ultrakleine schermen
 Racisme waarvan wordt beweerd dat het inheemse kinderen zijn die uit gezinnen zijn weggenomen - hoewel de staatszorg hen vaak in de steek laat
Racisme waarvan wordt beweerd dat het inheemse kinderen zijn die uit gezinnen zijn weggenomen - hoewel de staatszorg hen vaak in de steek laat Onderzoekers ontwikkelen technologie waarmee standaardcamera's hyperspectrale beelden kunnen produceren
Onderzoekers ontwikkelen technologie waarmee standaardcamera's hyperspectrale beelden kunnen produceren Subtiele visuele aanwijzingen sporen gebruikers aan om meer te onthullen op het online forum
Subtiele visuele aanwijzingen sporen gebruikers aan om meer te onthullen op het online forum AT&T-aandelen dalen naarmate meer tv-klanten vertrekken
AT&T-aandelen dalen naarmate meer tv-klanten vertrekken Ongevoelig wit publiek zorgt ervoor dat zwarte mensen zich onwelkom voelen bij culturele evenementen
Ongevoelig wit publiek zorgt ervoor dat zwarte mensen zich onwelkom voelen bij culturele evenementen Raak opgewonden door neurale netwerken
Raak opgewonden door neurale netwerken Grafeen blijkt infrarood licht uit te zenden
Grafeen blijkt infrarood licht uit te zenden Nieuwe filmtechniek onthult bacteriële signalering in scherpere resolutie
Nieuwe filmtechniek onthult bacteriële signalering in scherpere resolutie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

