
Wetenschap
Hoe beïnvloedt deeltjesbeweging de temperatuur?
* Kinetische energie: De deeltjes die materie vormen, zijn constant in beweging. Deze beweging wordt kinetische energie genoemd. Hoe sneller de deeltjes bewegen, hoe meer kinetische energie ze hebben.
* Temperatuur: Temperatuur is een maat voor de gemiddelde kinetische energie van de deeltjes in een stof.
* relatie: Hoe hoger de temperatuur, hoe sneller de deeltjes bewegen en hoe hoger hun gemiddelde kinetische energie. Omgekeerd, hoe lager de temperatuur, hoe langzamer de deeltjes bewegen en hoe lager hun gemiddelde kinetische energie.
Voorbeelden:
* Verwarmingswater: Wanneer je water verwarmt, voeg je energie toe aan de watermoleculen. Deze energie zorgt ervoor dat de moleculen sneller bewegen, hun kinetische energie verhogen en de temperatuur van het water verhogen.
* bevriezen water: Wanneer u water bevriest, verwijdert u energie uit de watermoleculen. Dit zorgt ervoor dat de moleculen vertragen, waardoor hun kinetische energie wordt verlaagd en de temperatuur van het water wordt verlaagd totdat het het vriespunt bereikt.
Andere factoren:
* Staat van materie: De toestand van materie (vaste, vloeistof, gas) beïnvloedt ook deeltjesbeweging en temperatuur. Deeltjes in vaste stoffen bewegen het minst, gevolgd door vloeistoffen en vervolgens gassen.
* specifieke hitte: Verschillende stoffen hebben verschillende specifieke warmte. Dit betekent dat er meer energie nodig is om de temperatuur van sommige stoffen te verhogen dan andere.
Samenvattend:
Temperatuur is een directe maat voor de gemiddelde kinetische energie van deeltjes in een stof. Hoe sneller de deeltjes bewegen, hoe hoger de temperatuur.
 Waarom zou Cl in NaCl het elektron winnen?
Waarom zou Cl in NaCl het elektron winnen?  Wat is de functie van waterstoffluoride?
Wat is de functie van waterstoffluoride?  Tijdens het praktische in het laboratorium wanneer hydrozensulfidegas met een overgangen wordt gepringeerd voor een test, kunt u zelfs 50 mtr weg ruiken, het fenomeen verklaren?
Tijdens het praktische in het laboratorium wanneer hydrozensulfidegas met een overgangen wordt gepringeerd voor een test, kunt u zelfs 50 mtr weg ruiken, het fenomeen verklaren?  Welke van deze subatomaire deeltjes worden weergegeven door het atoomnummer?
Welke van deze subatomaire deeltjes worden weergegeven door het atoomnummer?  Video:Heldinnen van het periodiek systeem
Video:Heldinnen van het periodiek systeem
 Hoe wordt biomassa berekend?
Hoe wordt biomassa berekend?  Wat zijn enkele aanpassingen van een eend?
Wat zijn enkele aanpassingen van een eend?  Wat gebeurt er als een gletsjer smelt?
Wat gebeurt er als een gletsjer smelt?
Naarmate de gemiddelde wereldtemperatuur stijgt, smelten gletsjers en trekken ze de valleien terug die ze naar beneden zijn gegaan. Wanneer gletsjers verdwijnen, wordt het landschap niet meer aangetast door to
 Groeien of verdedigen:hoe planten beslissen
Groeien of verdedigen:hoe planten beslissen  Wat is een voorbeeld van een natuurlijke hulpbron op het land?
Wat is een voorbeeld van een natuurlijke hulpbron op het land?
Hoofdlijnen
- Zien hoe evolutionaire mechanismen biologische diversiteit opleveren
- Wat onderzoekt fysioligist?
- Welk haarachtige projecties van de cel die kloppen en trillen worden genoemd?
- Voerrelaties in ecosystemen worden het best vertegenwoordigd door wat?
- De afhankelijkheid van organismen op elkaar om te overleven staat bekend als wat?
- Hoe heet een mengsel dat er zelfs onder de microscoop overal hetzelfde uitziet?
- Wilt u voorbeelden weten van membraangebonden organellen en niet-organellen?
- Zeldzame witte tijger met kanker sterft in dierentuin
- Door te bezuinigen op milieu-uitgaven, de overheid snijdt kansen
- Team ontwikkelt nieuwe micro-embossingapparatuur voor optische precisiemicrostructuren

- Geschaalde laboratoriumexperimenten verklaren het knikgedrag van de Krabnevel-jet

- Hoe werkt een leugendetector (polygraaf)?

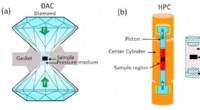
- Herziening van drukeffecten op op ijzer gebaseerde hogetemperatuursupergeleiders
- Nieuwe analytische benadering verbetert de detectie van kernspinresonantiesignalen in voorheen onzichtbare gebieden

 Onderzoekers genereren attoseconde licht van industriële laser
Onderzoekers genereren attoseconde licht van industriële laser Planten kunnen kiezen tussen alternatieve reacties op concurrentie
Planten kunnen kiezen tussen alternatieve reacties op concurrentie Hoe komt stikstof uit levende organismen terug in de lucht?
Hoe komt stikstof uit levende organismen terug in de lucht?  Cellen op een krappe plek
Cellen op een krappe plek De meeste oppervlakte -rotsen zijn?
De meeste oppervlakte -rotsen zijn?  Somt de stappen in de wetenschappelijke methode op?
Somt de stappen in de wetenschappelijke methode op?  Polymere membranen gebruiken om industriële scheidingen op te ruimen
Polymere membranen gebruiken om industriële scheidingen op te ruimen Wat hebben astronomen gedaan om waterdampvervuiling en atmosferische interferentie te voorkomen?
Wat hebben astronomen gedaan om waterdampvervuiling en atmosferische interferentie te voorkomen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

