
Wetenschap
Kun je de staat van materie veranderen door deeltjes aan te raken?
* schaal: Atomen en moleculen zijn ongelooflijk klein. Je vingers zijn gemaakt van miljarden atomen, en zelfs als je op de een of andere manier individuele atomen zou kunnen aanraken, zou de kracht die je uitoefent niet genoeg zijn om de krachten te overwinnen die hen in hun huidige staat in elkaar houden.
* Energieoverdracht: Het veranderen van de staat van materie vereist energie. Om ijs te smelten (vast aan vloeistof), moet u warmte -energie toevoegen. Om water te koken (vloeibaar naar gas), moet u nog meer energie toevoegen. Het aanraken van een deeltje met uw vinger brengt niet voldoende energie over om een significante toestandsverandering te veroorzaken.
* kwantumeffecten: Op atomair niveau gaan de regels van de klassieke fysica af. Atomen en moleculen werken op manieren die worden beheerst door de kwantummechanica. Het simpelweg aanraken van een deeltje zou niet noodzakelijkerwijs het gewenste effect hebben.
Hoe we staten van materie veranderen:
* Verwarming: Het toevoegen van warmte -energie verhoogt de kinetische energie van deeltjes, waardoor ze sneller bewegen en uit elkaar breken van hun vaste posities (vast tot vloeistof, vloeistof naar gas).
* Koeling: Het verwijderen van warmte -energie vertraagt deeltjes, waardoor ze sterkere bindingen kunnen vormen en meer georganiseerd worden (gas tot vloeistof, vloeistof tot vast).
* Druk: Toenemende druk kan deeltjes dichter bij elkaar dwingen, wat leidt tot een verandering in toestand (gas in vloeistof).
Conclusie:
Hoewel het een fascinerend gedachte -experiment is, is het veranderen van de toestand van materie door deeltjes aan te raken onmogelijk met ons huidige begrip van fysica en de beperkingen van onze fysieke mogelijkheden.
Hoofdlijnen
- Wat is de relatie tussen fysiologische en genetische differentiatiebacteriën met betrekking tot taxonomische classificatie van bacteriën?
- Wat zijn twee hoofdtypen wetenschappelijk onderzoek?
- Kunnen genetisch gemodificeerde muggen malaria uitroeien?
- Wat zijn de vleugtespieren van het menselijk lichaam?
- Waar bevinden lipiden zich in het lichaam?
- Wat Rosalind Franklin werkelijk heeft bijgedragen aan de ontdekking van structuur-DNA
- Hoe herhaalbaar is de evolutionaire geschiedenis?
- Wat is de ATP -rol bij cellulaire ademhaling?
- Wat is een kernreactor van een fokker?
- Nieuw onderzoek verdiept het mysterie van het genereren van deeltjes bij protonbotsingen
- Grasshopper-probleem geeft inzicht in kwantumtheorie

- Ultrakorte röntgentechniek om de omstandigheden in het hart van planeten te onderzoeken

- Onderzoekers onderzoeken het gebruik van licht om schijven in de mesosfeer te laten zweven

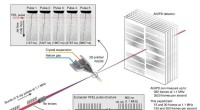
- Nieuwe technologie voor het eerste experiment met de grootste bron van röntgenstraling ter wereld
 Tweede wetenschappelijke ballon gelanceerd vanaf Antarctica
Tweede wetenschappelijke ballon gelanceerd vanaf Antarctica Hoe asteroïde-mijnbouw zal werken
Hoe asteroïde-mijnbouw zal werken  Meertalige studenten zijn sinds 2003 verbeterd in academische prestaties
Meertalige studenten zijn sinds 2003 verbeterd in academische prestaties Hoe promoot de VS onderzoek naar schone energie?
Hoe promoot de VS onderzoek naar schone energie?  Oog hebben voor kleuren:bedrukbare lichtsensoren
Oog hebben voor kleuren:bedrukbare lichtsensoren Hoeveel vierkante meter zal 5 kubieke voet erwtengrind bedekken?
Hoeveel vierkante meter zal 5 kubieke voet erwtengrind bedekken?  Winst Daimler loopt vooruit in derde kwartaal
Winst Daimler loopt vooruit in derde kwartaal Heeft u een constante kracht nodig om snelheid te produceren?
Heeft u een constante kracht nodig om snelheid te produceren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


