
Wetenschap
Beschrijf de staat van materie kwik en beweging zijn deeltjes omdat deze wordt verwarmd van -45 graden Celsius tot 356 Celsius?
startpunt:vaste toestand (-45 ° C)
* staat: Kwik is een vaste stof bij deze temperatuur.
* deeltjesbeweging: De kwikatomen zijn strak verpakt in een rigide, kristallijne structuur. Ze trillen in vaste posities, maar hun beweging is beperkt.
Verwarming tot smeltpunt (-38,83 ° C)
* staat: Terwijl kwik wordt verwarmd, absorberen de atomen energie. Deze verhoogde energie zorgt ervoor dat ze krachtiger trillen.
* deeltjesbeweging: De trillingen worden zo sterk dat ze de krachten beginnen te overwinnen die de atomen in hun vaste posities houden.
* smelten: Bij -38,83 ° C, het smeltpunt van Mercurius, breekt de structuur af en gaat het over naar een vloeibare toestand.
vloeibare toestand (-38,83 ° C tot 356,7 ° C)
* staat: Mercurius is nu een vloeistof.
* deeltjesbeweging: De atomen hebben meer vrijheid om te bewegen. Ze zijn nog steeds dicht bij elkaar, maar ze kunnen nu langs elkaar glijden, waardoor Mercurius de vloeibaarheid is. De atomen bewegen in een willekeurig, chaotisch patroon.
Verwarming tot kookpunt (356,7 ° C)
* staat: Naarmate kwik verder wordt verwarmd, krijgen de atomen nog meer energie.
* deeltjesbeweging: De atomaire trillingen worden zo intens dat ze de aantrekkelijke krachten overwinnen die de atomen in de vloeibare toestand houden.
* koken: Op 356,7 ° C, het kookpunt van Mercurius, breken de atomen los van de vloeistof en gaan ze over in een gasvormige toestand.
gasvormige toestand (boven 356,7 ° C)
* staat: Mercurius is nu een gas.
* deeltjesbeweging: De atomen liggen nu ver uit elkaar en bewegen willekeurig bij hoge snelheden, botsen met elkaar en de containerwanden.
Sleutelpunten:
* Warmte- en deeltjesbeweging: De belangrijkste afhaalmaaltijd is dat warmte energie biedt aan deeltjes, waardoor ze sneller bewegen en de krachten overwinnen die ze in een bepaalde staat van materie bij elkaar houden.
* staten van materie: De veranderingen in toestand (vaste, vloeistof, gas) worden veroorzaakt door de toenemende kinetische energie van de kwikatomen.
* Temperatuur en kinetische energie: Temperatuur is een directe maat voor de gemiddelde kinetische energie van de deeltjes in een stof.
Laat het me weten als je meer details wilt over een van deze fasen!
 Waarom is natrium minder reactief dan kalium?
Waarom is natrium minder reactief dan kalium?  Jodidezouten stabiliseren biokatalysatoren voor brandstofcellen
Jodidezouten stabiliseren biokatalysatoren voor brandstofcellen Wat is de volledige ionische vergelijking voor de reactie tussen na2So4 en cacl2?
Wat is de volledige ionische vergelijking voor de reactie tussen na2So4 en cacl2?  Zeldzame aarde-orthoferriet LnFeO3-nanodeeltjes voor bio-imaging
Zeldzame aarde-orthoferriet LnFeO3-nanodeeltjes voor bio-imaging Sneeuwvlokken informeren wetenschappers hoe tandglazuur wordt gevormd
Sneeuwvlokken informeren wetenschappers hoe tandglazuur wordt gevormd
 Samengestelde gevaren vormen een verhoogd risico voor dichtbevolkte regio's in de Himalaya
Samengestelde gevaren vormen een verhoogd risico voor dichtbevolkte regio's in de Himalaya Het vervangen van kolen door gas of hernieuwbare energie bespaart miljarden liters water
Het vervangen van kolen door gas of hernieuwbare energie bespaart miljarden liters water Boeren gebruiken technologie om elke druppel uit de Colorado-rivier te persen
Boeren gebruiken technologie om elke druppel uit de Colorado-rivier te persen Spanje bosbranden hervat en bedreigt natuurpark
Spanje bosbranden hervat en bedreigt natuurpark Himalaya winden spelen rol bij wolken- en vochttransport, water herverdeling
Himalaya winden spelen rol bij wolken- en vochttransport, water herverdeling
Hoofdlijnen
- Wat is er in vertibraat?
- Het grootste onderzoek naar de groei van de dinosauruspopulatie ooit laat zien hoe Maiasaura leefde en stierf
- Wat is biologie in uw eigen woorden?
- Hoe wordt het individu geproduceerd door aseksuele reproductie?
- Welk enzym transcribeert DNA naar mRNA?
- Wetenschappers ontdekken hoe bacteriën vloeibare eiwitdruppeltjes gebruiken om stress te overwinnen
- Identificeer de organismen die ook cupdieren worden genoemd?
- Leg uit waarom grote actieve organismen een speciaal oppervlak nodig hebben voor uitwisseling?
- Hoe heet de moderne naam van amoeba -cellen?
- Tijd bestaat misschien niet, volgens natuurkundigen en filosofen, maar dat geeft niet

- Ontkurken van champagne zorgt voor ondergeëxpandeerde supersonische vriesstralen van kooldioxide

- Hoe diep is een spiegel? Het hangt er van af, maar de berekeningen zijn nu nauwkeuriger

- Nieuwe kwantumparadox onthult tegenstrijdigheid tussen wijdverbreide overtuigingen

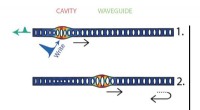
- Beheersing van niet-klassieke mechanische toestanden in een phononic waveguide-architectuur
 Welke cirkelvormige beweging is er een waarin een oblect een pad beweegt met constante snelheid?
Welke cirkelvormige beweging is er een waarin een oblect een pad beweegt met constante snelheid?  Klimaatmodellen worden vaak aangevallen, maar meestal zijn ze opmerkelijk goed
Klimaatmodellen worden vaak aangevallen, maar meestal zijn ze opmerkelijk goed Hoe een Bobcat af te weren
Hoe een Bobcat af te weren  Hoe ontstaat oxidatie bij bananen?
Hoe ontstaat oxidatie bij bananen?  Methanotrofen:kunnen bacteriën ons milieu helpen beschermen?
Methanotrofen:kunnen bacteriën ons milieu helpen beschermen?  Rechters veroordelen jeugddelinquenten tot schaken, met veelbelovende resultaten
Rechters veroordelen jeugddelinquenten tot schaken, met veelbelovende resultaten Is de eenheid van het bedrag van de hoeveelheid afgeleid of fundamenteel?
Is de eenheid van het bedrag van de hoeveelheid afgeleid of fundamenteel?  Waarom is de nebulaire hypothese het meest geaccepteerde theorie?
Waarom is de nebulaire hypothese het meest geaccepteerde theorie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

