
Wetenschap
Wat is het orbitale diagram voor FE?
1. Elektronische configuratie:
* IJzer heeft een atoomnummer van 26, wat betekent dat het 26 elektronen heeft.
* De elektronische configuratie voor ijzer is: 1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3D⁶
2. Orbitaal diagram:
* 1S: Twee elektronen vullen de 1s orbital (weergegeven als ↑ ↓).
* 2S: Twee elektronen vullen de 2s orbital (↑ ↓).
* 2p: Zes elektronen vullen de drie 2P -orbitalen, met één elektron in elk orbitaal vóór het paren (↑ ↑ ↑).
* 3S: Twee elektronen vullen de 3s orbital (↑ ↓).
* 3P: Zes elektronen vullen de drie 3P -orbitalen (↑ ↓ ↑ ↓ ↑ ↓).
* 4S: Twee elektronen vullen de 4s orbital (↑ ↓).
* 3D: Zes elektronen vullen de vijf 3D -orbitalen. Na de heerschappij van Hund vullen we elk orbitaal met één elektron vóór het koppelen:↑ ↑ ↑ ↑ ↑ ↑
3. Vertegenwoordiging:
Het volledige orbitale diagram voor ijzer ziet er zo uit:
`` `
1S:↑ ↓
2S:↑ ↓
2p:↑ ↑ ↑
3S:↑ ↓
3p:↑ ↓ ↑ ↓ ↑ ↓
4S:↑ ↓
3d:↑ ↑ ↑ ↑ ↑ ↑
`` `
Belangrijke opmerking: De 3D -orbitalen worden meestal weergegeven als een doosdiagram met vijf dozen, die elk een ander 3D -orbitaal vertegenwoordigen.
Laat het me weten als je wilt dat ik het doosdiagram teken!
 Vuurvliegjes werpen licht op de functie van mitochondriën
Vuurvliegjes werpen licht op de functie van mitochondriën Wat is de wet van de Mass State die niet kan worden gecreëerd of vernietigd tijdens een chemische reactie?
Wat is de wet van de Mass State die niet kan worden gecreëerd of vernietigd tijdens een chemische reactie?  Hoge veiligheid, flexibele en schaalbare oplaadbare planaire microbatterijen
Hoge veiligheid, flexibele en schaalbare oplaadbare planaire microbatterijen Een reactie op preparatieve schaal met behulp van platinaclusters met een gerealiseerde eencijferige atomiciteit
Een reactie op preparatieve schaal met behulp van platinaclusters met een gerealiseerde eencijferige atomiciteit Wanneer twee heldere vloeistoffen worden gemengd en er een gele kleur ontstaat, is er sprake van chemische verandering?
Wanneer twee heldere vloeistoffen worden gemengd en er een gele kleur ontstaat, is er sprake van chemische verandering?
 Voor het laaggelegen Napels in Florida, golvende zeeën vormen een dodelijke bedreiging
Voor het laaggelegen Napels in Florida, golvende zeeën vormen een dodelijke bedreiging Blootstelling aan luchtvervuiling verschuift van buiten naar binnen - dit is waarom
Blootstelling aan luchtvervuiling verschuift van buiten naar binnen - dit is waarom Welke aantrekkelijke bladeren zijn vaak kleurrijk en zoet geurend?
Welke aantrekkelijke bladeren zijn vaak kleurrijk en zoet geurend?  Ernstige gezondheidsrisico's door afvalverbranding in Libanon:rapport
Ernstige gezondheidsrisico's door afvalverbranding in Libanon:rapport Studie onthult trends van oppervlaktewaterlichaam in de VS gedurende drie decennia
Studie onthult trends van oppervlaktewaterlichaam in de VS gedurende drie decennia
Hoofdlijnen
- Nieuwe vissoorten vertonen opvallend kleurverschil tussen mannetjes en vrouwtjes
- Alle lichaamsorganen zijn van vitaal belang voor het leven of onwaar?
- Wat is intracellulaire bron van spijsverteringsenzymen?
- Onderzoek toont aan hoe het eiwit de ontwikkeling van fruitvliegvleugels regelt
- Wat is de oorzaak van sikkelcel?
- Welk type weefsel wordt in het embryo vervangen tijdens endochondrale ossificatie?
- Eetbaar diercelproject met Candy
- Hoe ernstig is inteelt bij showhonden?
- Uitbraken van hondsdolheid bij vee in Costa Rica houden verband met ontbossing
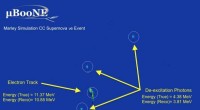
- Modelleren van botsingen tussen argonkernen en neutrino's van een supernova
- Natuurkundigen die steeds dieper in de materie van het universum tasten

- Terahertz-spectroscopie komt in het regime van één molecuul
- De transmissie van kwantuminformatie stroomlijnen

- Onderzoekers effenen de weg voor het ontwerpen van omnidirectionele onzichtbare materialen

 Hoe weet ik of iets een fysieke of chemische eigenschap is?
Hoe weet ik of iets een fysieke of chemische eigenschap is?  Waar zijn voorbeelden van Plains Mountains and Valleys?
Waar zijn voorbeelden van Plains Mountains and Valleys?  Wat zijn de componenten van een zuurstoftoevoersysteem?
Wat zijn de componenten van een zuurstoftoevoersysteem?  Nieuw nanomateriaal, in de vorm van Davidssterren, ontdekt door Israëlische wetenschappers
Nieuw nanomateriaal, in de vorm van Davidssterren, ontdekt door Israëlische wetenschappers Objecten ter grootte van een huis in de buurt van de aarde zeldzamer dan we dachten
Objecten ter grootte van een huis in de buurt van de aarde zeldzamer dan we dachten Is waterstofperoxide een chemische of fysische verandering?
Is waterstofperoxide een chemische of fysische verandering?  LS2-rapport:voor de terugkeer van de kou
LS2-rapport:voor de terugkeer van de kou Welke temperatuur verandert water in een vaste stof?
Welke temperatuur verandert water in een vaste stof?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

