
Wetenschap
Wat is de aantrekkingskracht tussen deeltjes in een vaste stof?
* intermoleculaire krachten: Vaste stoffen worden bij elkaar gehouden door sterke intermoleculaire krachten, die de aantrekkelijke krachten tussen moleculen zijn. Deze krachten kunnen zijn:
* van der Waals krachten: Dit zijn zwakke attracties die voortvloeien uit tijdelijke schommelingen in elektronenverdeling rond moleculen. Ze zijn aanwezig in alle vaste stoffen, maar zijn sterker in grotere moleculen.
* waterstofbinding: Dit is een speciaal type dipool-dipoolinteractie waarbij een waterstofatoom wordt gebonden aan een sterk elektronegatief atoom (zoals zuurstof of stikstof). Het is een bijzonder sterke intermoleculaire kracht.
* Dipole-Dipole Forces: Deze komen voort uit de permanente dipolen in polaire moleculen.
* ionische bindingen: In ionische vaste stoffen is de aantrekkingskracht tussen tegengesteld geladen ionen erg sterk. Dit is de elektrostatische kracht die de ionen bij elkaar houdt.
* metalen bindingen: In metalen worden de elektronen gedelokaliseerd en vormen ze een "zee" van elektronen die de metaalionen bij elkaar houden. Deze sterke aantrekkingskracht geeft metalen hun karakteristieke eigenschappen zoals geleidbaarheid en kneedbaarheid.
Key Takeaway: De sterke attracties tussen deeltjes in een vaste stof zijn wat hen hun vaste vorm en volume geven. Ze weerstaan veranderingen in vorm en volume veel meer dan vloeistoffen of gassen.
 NASA-camera op afstand levert nieuwe aardebeelden op
NASA-camera op afstand levert nieuwe aardebeelden op Droogte, klimaatverandering bedreigen de toekomst van Amerikaanse waterkracht
Droogte, klimaatverandering bedreigen de toekomst van Amerikaanse waterkracht Nieuwe webtool zal militaire, samenwerking tussen windenergie-industrie
Nieuwe webtool zal militaire, samenwerking tussen windenergie-industrie Noordelijk halfrond wordt geconfronteerd met een 4-voudige stijging in perioden van extreme hitte:studie
Noordelijk halfrond wordt geconfronteerd met een 4-voudige stijging in perioden van extreme hitte:studie Everglades laten een verbetering van de waterkwaliteit zien
Everglades laten een verbetering van de waterkwaliteit zien
Hoofdlijnen
- Wat is het uitscheidingsproduct van Amoeba?
- Hoe ingewikkelde patronen ontstaan in zich ontwikkelende weefsels
- Waarom gedijt dit invasieve, niet-inheemse rietgras in de wetlands?
- Wanneer insuline commercieel werd geproduceerd in genetisch gemanipuleerde bacteriën en gist het verkregen uit de alvleesklier van wat?
- Is een pinda een angiosperm of gymnosperm?
- Wat is de methode waarmee tropische en niet-tropische hormonen een respons veroorzaken?
- Hoe assembleren wetenschappers met verschillende gezichtspunten het evolutionaire verhaal?
- Wiskundige modellen laten zien hoe organismen de som van hun genen overstijgen
- Wat zijn de fylogenetica?
- Monster X-ray laser biedt een kijkje in de nanowereld (update)

- Experts sceptisch over het gebruik van snot om een schutter te identificeren

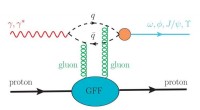
- Natuurkundigen halen de straal van de protonmassa uit experimentele gegevens
- Nieuwe klassen van topologische kristallijne isolatoren met anomalie van oppervlakterotatie

- Natuurkundigen ontdekken verborgen aspecten van elektrodynamica

 Wordt de zon uiteindelijk een neutronenster?
Wordt de zon uiteindelijk een neutronenster?  Nieuwe ontdekking van nanodeeltjes opent deur voor farmaceutica
Nieuwe ontdekking van nanodeeltjes opent deur voor farmaceutica Sla laat zien hoe je met olie doordrenkte grond kunt herstellen
Sla laat zien hoe je met olie doordrenkte grond kunt herstellen Fukushima-hotspots halen de krantenkoppen voor de Olympische Spelen, maar wat is het risico?
Fukushima-hotspots halen de krantenkoppen voor de Olympische Spelen, maar wat is het risico? Hoe vaak draait de maan elke dag rond de aarde?
Hoe vaak draait de maan elke dag rond de aarde?  IJsberg doemt op boven Groenlands dorp gezien vanuit de ruimte
IJsberg doemt op boven Groenlands dorp gezien vanuit de ruimte Hoe een eenvoudige psychologische interventie de schoolcijfers van studenten met een laag inkomen kan helpen verhogen
Hoe een eenvoudige psychologische interventie de schoolcijfers van studenten met een laag inkomen kan helpen verhogen Commentaar:COVID-19 verergerde de problemen van de Engelse pubindustrie
Commentaar:COVID-19 verergerde de problemen van de Engelse pubindustrie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

