
Wetenschap
Waar experimenteerde J. Thomson?
Het experiment:
* kathodestraalbuizen: Thomson gebruikte een gespecialiseerde glazen buis genaamd A Cathode Ray Tube (CRT). Deze buis werd geëvacueerd (bijna alle lucht werd verwijderd) en had er een hoge spanning over toegepast.
* kathodestralen: Wanneer de spanning werd toegepast, werd een stroom van onzichtbare deeltjes, bekend als kathodestralen, uitgezonden uit de negatieve elektrode (kathode).
* magnetische en elektrische velden: Thomson plaatste magnetische en elektrische velden rond de CRT. Hij merkte op dat de kathodestralen door beide velden werden afgebogen.
* Meet en analyse: Door de afbuiging van de stralen in de velden zorgvuldig te meten, kon Thomson de lading-massa-verhouding (E/M) van de deeltjes bepalen.
* Ontdekking van het elektron: De berekeningen van Thomson toonden aan dat de lading-massa-verhouding van de deeltjes in de kathodestralen veel hoger was dan enig bekende ion. Dit bracht hem ertoe te concluderen dat de kathodestralen waren samengesteld uit voorheen onbekende, negatief geladen deeltjes, die hij elektronen noemde .
Betekenis van het experiment:
* Atomische structuur: Thomson's experiment bracht een revolutie teweeg in ons begrip van het atoom. Het toonde aan dat atomen niet ondeelbaar zijn maar kleinere, fundamentele deeltjes bevatten.
* Elektronenontdekking: Zijn ontdekking van het elektron maakte de weg vrij voor verder onderzoek naar de structuur van materie en de ontwikkeling van de kwantummechanica.
Het "pruimpuddingmodel":
Op basis van zijn experiment stelde Thomson een model voor van het atoom genaamd het pruimpuddingmodel . Dit model beschouwde het atoom als een bol van positieve lading met negatief geladen elektronen ingebed daarin, zoals pruimen in een pudding. Hoewel dit model later onjuist was gebleken, was het een belangrijke stap om de atoomstructuur te begrijpen.
 Metaalvervuiling:als het in de lucht zit - en onze iPhones - komt het in onze botten terecht
Metaalvervuiling:als het in de lucht zit - en onze iPhones - komt het in onze botten terecht Opwarming van de aarde intensiveert extreme neerslag in China
Opwarming van de aarde intensiveert extreme neerslag in China Inleiding tot Febot
Inleiding tot Febot  Voorspelling van economische en demografische verschuivingen in de VS met een hogere resolutie
Voorspelling van economische en demografische verschuivingen in de VS met een hogere resolutie Milieuwetenschappers:tot 20% van de wereldwijde grondwaterbronnen dreigt op te drogen
Milieuwetenschappers:tot 20% van de wereldwijde grondwaterbronnen dreigt op te drogen
Hoofdlijnen
- Welk systeem maakt en brengt hormonen uit?
- Wat is het verschil tussen wetenschappelijke theorie en hypothese?
- Waarom moeten cellen een optimaal intern milieu behouden?
- Wat is exotomisch en endotomisch?
- Hoe celprocessen beschadigde eiwitten verzamelen en dumpen
- Hoe genetische achtergrond individuele verschillen binnen een soort vormt
- Wat zijn de monomeren van triglyceriden?
- De structuur en functie van spiercellen
- Hoe zijn gymnospermen en angiospermen verschillend?
- Over het ontstaan van vorm:er is geen magie in synchronisatie op afstand
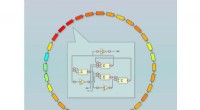
- Een kwantumspinvloeistof:honingraatrooster voldoet aan de ongrijpbare normen van het Kitaev-model
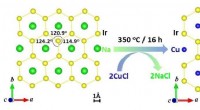
- Onderzoekers ontwikkelen nieuwe methode om superfluïde beweging te detecteren

- Herziene code kan de efficiëntie van fusie-experimenten helpen verbeteren

- Eerste stap naar fotonisch kwantumnetwerk

 In een opwarmende wereld, Cape Towns Day Zero droogte zal geen anomalie zijn
In een opwarmende wereld, Cape Towns Day Zero droogte zal geen anomalie zijn Asteroïde 16 Psyche is misschien niet wat wetenschappers hadden verwacht
Asteroïde 16 Psyche is misschien niet wat wetenschappers hadden verwacht  Voedselketen: definitie, soorten, belang en voorbeelden (met diagram)
Voedselketen: definitie, soorten, belang en voorbeelden (met diagram)  Historicus onthult verband tussen zelfmoord en politieke crisis
Historicus onthult verband tussen zelfmoord en politieke crisis Wat is een fysieke eigenschap die goud en koper gemeen hebben, maar niet ijzer?
Wat is een fysieke eigenschap die goud en koper gemeen hebben, maar niet ijzer?  Soorten aardrijkskundige kenmerken op een plaatgrens
Soorten aardrijkskundige kenmerken op een plaatgrens  Tesla CEO verheft aandeelhoudersgeesten, richt zich op de media
Tesla CEO verheft aandeelhoudersgeesten, richt zich op de media Verschil tussen licht magnesiumcarbonaat en zwaar carbonaat?
Verschil tussen licht magnesiumcarbonaat en zwaar carbonaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

