
Wetenschap
Wat is de relatie tussen twee element X en Y wiens atoomnummers 18 20 zijn, maar hun massagummer blijft hetzelfde als 40?
* Atomisch nummer (aantal protonen): X heeft een atoomnummer van 18, terwijl Y een atoomnummer van 20 heeft. Dit betekent dat X 18 protonen heeft en Y 20 protonen heeft.
* Massienummer (protonen + neutronen): Beide elementen hebben een massaal aantal van 40. Dit betekent dat zowel X als Y in totaal 40 protonen en neutronen hebben.
De relatie:
Elementen x en y zijn isotopen . Isotopen van een element hebben hetzelfde aantal protonen (atoomnummer) maar verschillen in het aantal neutronen.
Hier is hoe het werkt:
* element x: Met een atoomnummer van 18 (18 protonen) heeft het 22 neutronen nodig om een massa aantal van 40 te bereiken (18 protonen + 22 neutronen =40).
* element y: Met een atoomnummer van 20 (20 protonen) heeft het 20 neutronen nodig om een massa aantal van 40 te bereiken (20 protonen + 20 neutronen =40).
Conclusie:
Elementen X en Y zijn isotopen. X heeft 22 neutronen, terwijl Y 20 neutronen heeft. Het zijn verschillende vormen van hetzelfde element, maar hun verschillende neutronentellingen geven ze enigszins verschillende eigenschappen.
Opmerking: Element X is argon (AR) en element Y is calcium (Ca).
 Hoe steriliseer je flesjes?
Hoe steriliseer je flesjes?  Massaspectrometrische beeldvormingstechniek maakt diagnose eenvoudiger en slimmer
Massaspectrometrische beeldvormingstechniek maakt diagnose eenvoudiger en slimmer Wat is de enthalpie van een reactie?
Wat is de enthalpie van een reactie?  Autonome zelfgenezing gezien in piëzo-elektrische moleculaire kristallen
Autonome zelfgenezing gezien in piëzo-elektrische moleculaire kristallen Onderzoekers werpen licht op hoe één dodelijke ziekteverwekker zijn chemicaliën maakt
Onderzoekers werpen licht op hoe één dodelijke ziekteverwekker zijn chemicaliën maakt
 Stijgende zeespiegel creëert eerste inheemse Amerikaanse klimaatvluchtelingen
Stijgende zeespiegel creëert eerste inheemse Amerikaanse klimaatvluchtelingen Onderzoek naar plantenchemie onderzoekt trends in vergroening
Onderzoek naar plantenchemie onderzoekt trends in vergroening Een perfecte storm:beoordeling van de dodelijke impact van klimaatgerelateerde overstromingen en cyberaanvallen
Een perfecte storm:beoordeling van de dodelijke impact van klimaatgerelateerde overstromingen en cyberaanvallen  Het identificeren van de belangrijkste hotspots voor natuurbehoud in Canada wijst op een probleem
Het identificeren van de belangrijkste hotspots voor natuurbehoud in Canada wijst op een probleem Moet een geurtheorie zinvol zijn?
Moet een geurtheorie zinvol zijn?
Hoofdlijnen
- Hoe een beter begrip van het gedrag van hermelijnen de bestrijding van roofdieren in Aotearoa zal helpen
- De voordelen van het gebruik van Sticky End Enzymen
- Cellen bij elkaar houden:hoe ons lichaam mechanische stress weerstaat
- Wat leidt er af. Wetenschap?
- Hoe verzamelen wetenschappers bewijsmateriaal om vragen te beantwoorden?
- Waarom zijn Archaea en verschillende domein van bacteriën?
- Wanneer twee soorten zo nauw samenwerken dat ze aan elkaar zijn aangepast, wordt de interactie genoemd?
- Voetafdrukken gebruiken om reuzenpanda's in het wild te identificeren en te volgen
- Hoe transporteren dragereiwitten ADP en ATP de mitochondriën in?
- IonQ kondigt ontwikkeling van volgende generatie kwantumcomputer aan

- Algemene doorbraak op het gebied van atoomenergie maakt meer controle over fusie-energie mogelijk

- Thorium supergeleiding:wetenschappers ontdekken nieuwe hoge-temperatuur supergeleider
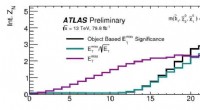
- ATLAS-experiment stelt sterke beperkingen aan supersymmetrische donkere materie
- Onderzoek wijst op natuurkundige principes die ten grondslag liggen aan het kwantumdarwinisme
 Epigenetische inzichten:hoe hybride populier scheuten regenereert
Epigenetische inzichten:hoe hybride populier scheuten regenereert  Hoeveel neutronen bevat een platina -atoom?
Hoeveel neutronen bevat een platina -atoom?  Een oceaan in de aarde? Er is vastgesteld dat er honderden kilometers beneden water ligt
Een oceaan in de aarde? Er is vastgesteld dat er honderden kilometers beneden water ligt Algoritme kan helpen de populariteit van posts op sociale media te vergroten
Algoritme kan helpen de populariteit van posts op sociale media te vergroten De oude inheemse Nieuw-Mexicaanse gemeenschap wist hoe ze duurzaam naast natuurbranden kon bestaan
De oude inheemse Nieuw-Mexicaanse gemeenschap wist hoe ze duurzaam naast natuurbranden kon bestaan  Mysteries of Earth:Onderzoekers voorspellen hoe snel de oude magma-oceaan stolde
Mysteries of Earth:Onderzoekers voorspellen hoe snel de oude magma-oceaan stolde  Hoe doodt streptomycine bacteriecellen?
Hoe doodt streptomycine bacteriecellen?  Kunsthuid creëert eerste prikkelbare apparaten
Kunsthuid creëert eerste prikkelbare apparaten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

