
Wetenschap
Hoe beïnvloedt de druk het volume?
p₁v₁ =p₂v₂
Waar:
* P₁ =Initiële druk
* V₁ =eerste volume
* P₂ =uiteindelijke druk
* V₂ =definitief volume
Hier is hoe het werkt:
* Stel je een container voor met een vaste hoeveelheid gas. De gasmoleculen bewegen en botsen constant met de wanden van de container, waardoor druk ontstaat.
* Als u het volume van de container vermindert (maak het kleiner), De gasmoleculen hebben minder ruimte om te bewegen.
* Dit betekent dat ze vaker met de muren botsen, het verhogen van de druk.
* Omgekeerd, als u het volume van de container verhoogt, De gasmoleculen hebben meer ruimte, botsen minder vaak met de wanden en de druk neemt af.
Voorbeelden:
* Een fietspomp: Terwijl u op de plunjer duwt, vermindert u het volume in de pomp. Dit verhoogt de druk, die lucht in de band dwingt.
* een ballon: Wanneer je in een ballon blaast, vergroot je het volume erin. De druk in de ballon neemt af, maar de ballon breidt zich uit om de toegevoegde lucht op te vangen.
Belangrijke overwegingen:
* de wet van Boyle is alleen van toepassing als de temperatuur en de hoeveelheid stof constant blijven. Als deze factoren veranderen, zal de relatie tussen druk en volume ook veranderen.
* Deze relatie is ook belangrijk in andere contexten, zoals in het menselijk lichaam (bijvoorbeeld ademhaling) , waarbij het drukverschil tussen de atmosfeer en de longen de lucht in en uit kan stromen.
 Nieuwe doelstelling voor ontwikkeling van innovatieve antibiotica
Nieuwe doelstelling voor ontwikkeling van innovatieve antibiotica Residuen in vingerafdrukken bevatten aanwijzingen voor hun leeftijd
Residuen in vingerafdrukken bevatten aanwijzingen voor hun leeftijd Elektrolytboost verbetert de prestaties van waterige dual-ion-batterijen
Elektrolytboost verbetert de prestaties van waterige dual-ion-batterijen Wetenschappers creëren een chemische methode voor het in kaart brengen van de ruimte en ontrafelen het mysterie van het getal van Mendelejev
Wetenschappers creëren een chemische methode voor het in kaart brengen van de ruimte en ontrafelen het mysterie van het getal van Mendelejev Warmteflux
Warmteflux
 Afbeelding:Copernicus Sentinel-2A-satelliet legt de wetlands van Botswana vast
Afbeelding:Copernicus Sentinel-2A-satelliet legt de wetlands van Botswana vast Ondanks hoge verwachtingen, de koolstof die wordt geabsorbeerd door het herstel van het Amazonewoud valt in het niet bij de uitstoot van ontbossing
Ondanks hoge verwachtingen, de koolstof die wordt geabsorbeerd door het herstel van het Amazonewoud valt in het niet bij de uitstoot van ontbossing NASA's ziet nachtelijke rek van tropische cycloon Carlos
NASA's ziet nachtelijke rek van tropische cycloon Carlos In Spanje, hoe voedingsstoffen een van Europa's grootste zoutwaterlagunes vergiftigden
In Spanje, hoe voedingsstoffen een van Europa's grootste zoutwaterlagunes vergiftigden De effecten van bioaccumulatie op het ecosysteem
De effecten van bioaccumulatie op het ecosysteem
Hoofdlijnen
- Hoe bereikt de buis van de pollenkorrels eierstok?
- Wat is hypotonisch en het voorbeeld ervan?
- Is een cypris hetero of auto?
- Onderzoekers ontdekken hoe muggen voorkomen dat ze bezwijken voor virussen die ze overbrengen
- Wat zijn lobben in een kern?
- Wat hebben variabelen en onafhankelijk gemeen?
- Kun je het 5 -koninkrijk van organisme met voorbeeld vermelden?
- Hoe ademen vogels beter? De ontdekking van onderzoekers zal je voor de gek houden
- Ribosome standby:hoe bacteriën eiwitten vertalen van structureel geblokkeerde mRNA's
- Meer dan de som der delen:het ATLAS-experiment kijkt in het proton

- Wat is kosmologische roodverschuiving?

- Hoe de beperkte bandbreedte efficiënter gebruiken? Denk als een grotbewonende vis
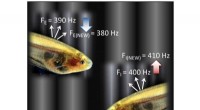
- DRUIVEN-3 duidt op een barst in het magnetische schild van de aarde

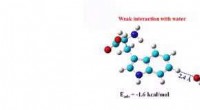
- Onderzoekers onderzoeken alomtegenwoordige interactie van biomoleculen met water
 Hoe wordt mechanisch koppel omgezet in elektrisch vermogen?
Hoe wordt mechanisch koppel omgezet in elektrisch vermogen?  Wordt Caustic Soda als veilig beschouwd voor het milieu?
Wordt Caustic Soda als veilig beschouwd voor het milieu?  Waarom groeien maggots op vlees?
Waarom groeien maggots op vlees?  Magnesiumdiboride in bulk supergeleidend houden bij hogere stroomdichtheden
Magnesiumdiboride in bulk supergeleidend houden bij hogere stroomdichtheden Wat zijn menselijke aanpassingen aan extreem klimaat in Coober Pedy?
Wat zijn menselijke aanpassingen aan extreem klimaat in Coober Pedy?  Nieuwe techniek om nanogestructureerde nanodraden te synthetiseren
Nieuwe techniek om nanogestructureerde nanodraden te synthetiseren Wat is de meest waarschijnlijke verklaring voor het feit dat Venus geen sterk magnetisch veld heeft?
Wat is de meest waarschijnlijke verklaring voor het feit dat Venus geen sterk magnetisch veld heeft?  Radiowaarnemingen wijzen op een waarschijnlijke verklaring voor het samensmelten van neutronensterren
Radiowaarnemingen wijzen op een waarschijnlijke verklaring voor het samensmelten van neutronensterren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

