Wetenschap
Kleiner door cellen zien:een natuurlijke eencellige biomagnifier voor beeldvorming onder de golflengte
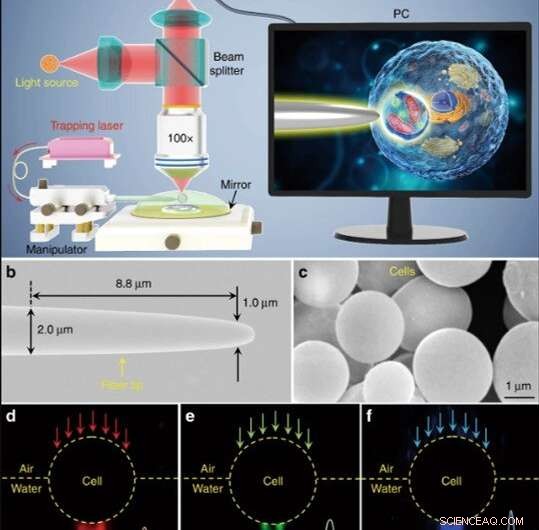
Schematische illustratie en materiaalkarakterisering. (a) Schematische weergave van de experimentele opstelling. Een conventionele microscoop met reflectiemodus uitgerust met een CCD-camera en × 100 objectieflens werd gebruikt om monsters te observeren en beelden op te nemen. De inzet op een pc-scherm toont schematisch hoe de biomagnifier wordt gebruikt om de subcellulaire structuren in een biomonster te vergroten en af te beelden. (b) SEM-beeld van de vezelpunt met een diameter van 1,0 m aan het taps toelopende uiteinde. (c) SEM-afbeelding met op gistcellen gebaseerde biomagnifiers met gladde oppervlakken en bolvormige vormen. d-f Donkerveldbeelden met 644-nm rood licht (d), 532 nm groen licht (e), en 473 nm blauw licht (f) dat door de biomagnifier straalt en wordt gefocusseerd in lichtvlekken onder de golflengte met een tailleradius van 370, 300, en 270 nm, respectievelijk. Credit:Licht:Wetenschap &Toepassingen, doi:10.1038/s41377-019-0168-4
Optische microscopen en pincetten kunnen objecten op microschaal in beeld brengen en manipuleren voor toepassingen in cellulaire en moleculaire biologie. De optische resolutie is echter, gehinderd door de diffractielimiet en daarom zijn zowel microscopen als pincetten niet in staat om nano-objecten rechtstreeks af te beelden en te manipuleren. Opkomende technieken in plasmonische/fotonische nanoscopen en nanopincet zijn gericht op het bereiken van resolutie op nanometerschaal, hoewel materiaalstructuren met een hoge index gemakkelijk mechanische en fotothermische schade aan de biospecimens op nanoschaal kunnen veroorzaken.
In een recente studie die nu is gepubliceerd op Licht:wetenschap en toepassingen , Yuchao Li en collega's van het Institute of Nanophotonics in China, ontwikkelde een optisch microscoopsysteem met levende cellen als kleine lenzen om objecten kleiner dan de golflengte van licht af te beelden en te manipuleren. Ze toonden sub-diffractie-limiet beeldvorming en manipulatie van nano-objecten met een niet-invasief apparaat, die ze construeerden door een cel op een vezelpunt te vangen. De gevangen cel vormde een biomagnifier die nanostructuren kon vergroten met een resolutie van 100 nm, onder witlichtmicroscopie. Met behulp van de biomagnifier, Li et al. vormden een nano-optische val om een individueel nanodeeltje met een straal van 50 nm nauwkeurig te manipuleren. De techniek biedt een uiterst nauwkeurig hulpmiddel voor optische beeldvorming, detectie en assemblage van bio-nanomaterialen zonder mechanische of fotothermische schade.
Optische beeldvorming om kleine objecten te manipuleren is cruciaal voor medische diagnose, biologische waarneming, cellulaire verkenning, moleculaire training en assemblage van materialen. Pincet en microscopen zijn standaardapparaten voor contactloze beeldvorming en manipulatie van minuscule monsters variërend van enkele nanometers tot enkele microns. Hoe dan ook, het is een uitdaging om de technologie te gebruiken om afbeeldingen op nanoschaal te maken, aangezien de optische resolutie beperkt is tot ongeveer de helft van de verlichtingsgolflengte.
Wetenschappers hebben de afgelopen decennia een dramatische vooruitgang geboekt met nanoscopen en nanopincet in het nabije veld om optische beeldvorming met nanometerresolutie te bereiken. Deze beeldvormingstechnieken werden tegengehouden door anorganische materialen met een hoge index, zoals edele metalen en halfgeleiders die werden gebruikt voor hun fabricage - die monsters van biologische cellen of weefsel mechanisch kunnen beschadigen tijdens beeldvorming en manipulatie in het nabije veld.
Wetenschappers onderzochten daarom eenvoudigere optische beeldvormingsschema's op basis van diëlektrische microsferen om de diffractielimiet te overwinnen die gebruikelijk is bij conventionele microscopen. Hoewel de techniek labelvrij en haalbaar is, dergelijke microbolletjes zijn gebaseerd op kunstmatige anorganische materialen zoals siliciumdioxide (SiO 2 ), titaandioxide (TiO 2 ) en bariumtitanaat (BaTiO 3 ). Onderzoekers zijn daarom geïnteresseerd in het ontwikkelen van een natuurlijk biomateriaal om een biocompatibel apparaat voor biobeeldvorming te bouwen, manipulatie en biomagnificatie bij ruimtelijke resolutie op nanoschaal.
(a) Schematische weergave van de experimentele opstelling. Een conventionele microscoop met reflectiemodus uitgerust met een CCD-camera en × 100 objectieflens werd gebruikt om monsters te observeren en beelden op te nemen. De inzet op een pc-scherm toont schematisch hoe de biomagnifier wordt gebruikt om de subcellulaire structuren in een biomonster te vergroten en af te beelden. Credit:Licht:Wetenschap &Toepassingen, doi:10.1038/s41377-019-0168-4 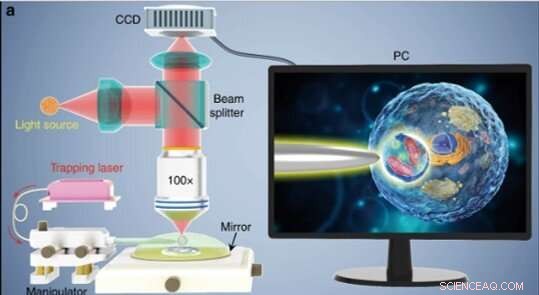
De wetenschappers voerden alle experimenten uit onder een optische microscoop met reflectiemodus, gekoppeld aan een CCD-camera (charge-coupled device) en objectieflens. Ze gebruikten lichtbronnen op 390 nm, 560 nm en 808 nm voor excitatie, respectievelijk verlichting en trapping. Met behulp van een optische vezel met een taps toelopende punt, Li et al. de biomagnifier opgesloten aan het einde van de vezel, die ze bestuurden door de tip te verplaatsen met behulp van een micromanipulator. Li et al. selecteerde gladde en bolvormige cellen om beeldafwijkingen te minimaliseren en merkte op dat de cellen betere focusprestaties vertoonden wanneer ze half ondergedompeld waren in oplossing om de levensvatbaarheid van de cellen te behouden.
Experimentele beeldvormingsprestaties van verschillende biomagnifiers. (a) Schematisch diagram dat laat zien dat de biomagnifier de nanostructuren in het nabije veld van een object verzamelt en een vrijwel vergroot beeld vormt dat kan worden vastgelegd met een conventionele optische microscoop. (b-e) Optische afbeeldingen van verschillende biomagnifiers opgebouwd uit bacteriële (b), gist (c), rood bloed (d), en stamcellen (e) die gedeeltelijk zijn ondergedompeld in celsuspensie. f SEM-beeld van een tweedimensionale zeshoekige, dicht opeengepakte silica-nanobolarray samengesteld door een fotoferesetechniek. (g-j) Optische beelden van de silica-nanosfeer-array vergroot door biomagnifiers op basis van bacteriële (g), gist (h), rood bloed (ik), en stamcellen (j). (k) SEM-beeld van het oppervlak van een Blu-ray-schijfrooster met een lijnbreedte van 200 nm en een afstand van 100 nm. l–o Optische beelden van de Blu-ray-roosterstructuur, vergroot door middel van biomagnifiers op basis van bacteriële (l), gist (m), rood bloed (n), en stamcellen (o). p Intensiteitsprofiel langs de stippellijn over de Blu-ray-roosterstructuur aangegeven in o. q Blauwe stippen die de vergrotingsfactor M weergeven van de door de biomagnifiers verkregen beelden als functie van de diameter van de biomagnifier. Credit:Licht:Wetenschap &Toepassingen, doi:10.1038/s41377-019-0168-4 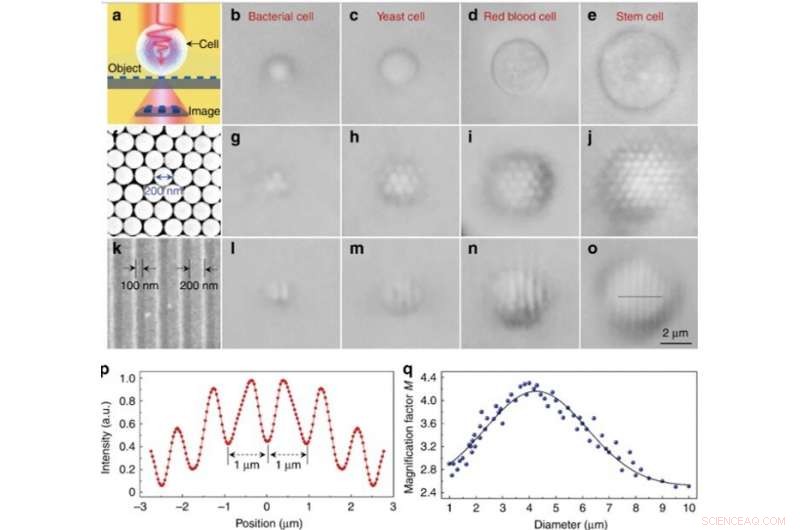
Alleen nanosferen met biomagnifiers erop konden worden opgelost tijdens beeldvorming, terwijl nanosferen zonder biomagnifiers niet konden worden opgelost met een conventionele microscoop. De vergrotingsfactor M van de op stamcellen gebaseerde biomagnifiers bleek 3,3 keer groter te zijn (x 3,3), en de wetenschappers toonden aan dat de experimentele M afhing van de diameter van de biomagnifier. Vervolgens, Li et al. voerden alle experimenten uit met biomagnifiers van deze diameter.
Nano-optische beeldvorming van subcellulaire structuren en letters met nanopatronen. (een, b) optische beelden van de subcellulaire structuren van een menselijke epitheelcel met behulp van een conventionele optische microscoop (a) en biomagnifiers (b). De posities van vier biomagnifiers zijn gemarkeerd als A–D. Ter vergelijking, de biomagnifiers kunnen het fibreuze cytoskelet (aangegeven als A-C) in de cel en tweelaagse structuren (aangegeven als D) op het celmembraan oplossen, die niet te onderscheiden zijn door de conventionele microscoop. c–e SEM (c), donkerveld (d), en optische afbeeldingen (e) van letters met nanopatroon JNU die het acroniem van Jinan University vertegenwoordigen. De lijnbreedte van de letters met nanopatroon is 100 nm, die kleiner is dan de diffractielimietresolutie van de conventionele optische microscoop. f–h Optische afbeeldingen die laten zien dat de biomagnifier die op de vezeltip is gevangen, de letters J (f) met nanopatroon kan scannen en afbeelden N (g), en U (h) door de vezel te verplaatsen. De lijnbreedte van de letters met nanopatroon werd vergroot van 100 tot 400 nm. Credit:Licht:Wetenschap &Toepassingen, doi:10.1038/s41377-019-0168-4 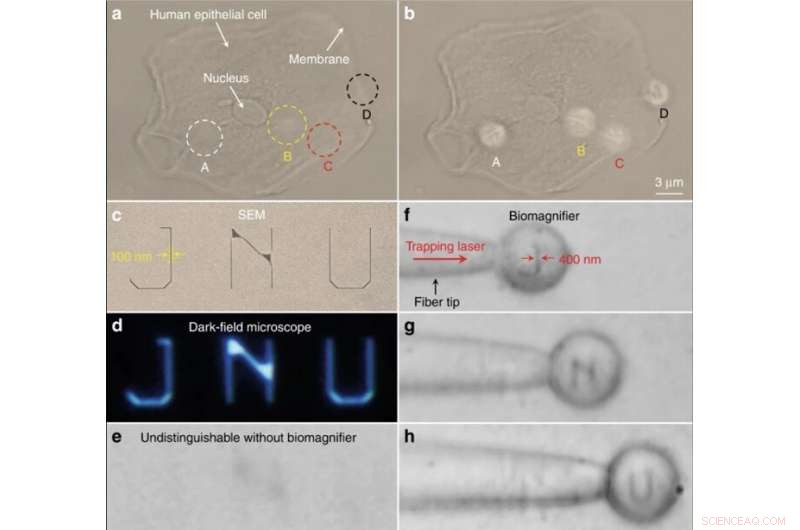
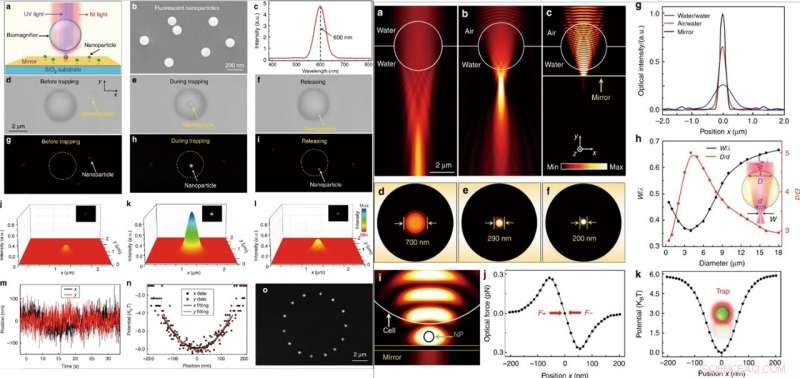
LINKS:optische manipulatie van een enkel fluorescerend nanodeeltje. (a) Schematisch diagram dat een fluorescerend nanodeeltje toont dat op het oppervlak van een spiegel is opgehangen en wordt opgevangen door de biomagnifier. (b) SEM-afbeelding met de PS-fluorescerende nanodeeltjes met een gemiddelde straal van 50 nm. (c) Emissiespectrum dat de centrale emissiegolflengte van de fluorescerende nanodeeltjes op 600 nm toont. (d-f) Optische afbeeldingen tonen het vangproces van een enkel PS-nanodeeltje met de biomagnifier. Het proces bestond uit drie opeenvolgende stappen:vóór het vangen (d), tijdens het vangen (e), en na loslaten (f). g–i Fluorescentiebeelden die de fluorescentievlek van het PS-nanodeeltje tonen voordat het wordt opgesloten (g), tijdens het vangen (h), en na loslaten (i). j–l Driedimensionale kleurtoewijzing van de fluorescentievlekken van het nanodeeltje zoals weergegeven in g–i. m Realtime tracering van de positie van het ingesloten nanodeeltje in de x- en y-richtingen. (n) Vangpotentiaal van het gevangen nanodeeltje in de x- en y-richtingen met paraboolfittingen. (o) Samengestelde fluorescentiebeelden tonen het bewegingsspoor van het gevangen nanodeeltje in het x-y-vlak door gecontroleerde beweging van de biomagnifier. RECHTS:Numerieke simulatie en berekening. (a-c) Optische intensiteitsverdelingen van lichtfocussering door een biomagnifier van 4 m volledig ondergedompeld in water (a), half ondergedompeld in water (b), en opgehangen aan het oppervlak van een spiegel (c). De verlichtingslichtbron was ingesteld als een Gauss-straal met een golflengte van 560 nm. (d-f) Optische intensiteitsverdelingen van de lichtvlekken van de biomagnifier die overeenkomt met (a-c) in het x-z-vlak. (g) Optische intensiteitsprofielen op de brandvlakken van het uitgangslicht van de biomagnifiers in de x-richting. (h) FEM-simulatieresultaten voor de genormaliseerde taille van de lichtvlek w/λ (w is de taillestraal van de lichtvlek en λ is de golflengte van het ingangslicht) en de verhouding D/d (de breedte van het lineaire gebied waar licht de biomagnifier aan de voorkant binnenkomt, wordt D genoemd, en de breedte van de uitgaande lichtbundel aan het achteroppervlak is (d) als een functie van de diameter van de biomagnifier. (i) Gesimuleerde intensiteitsverdeling van nabij-infrarood vanglicht waaruit blijkt dat een nanodeeltje (straal:50 nm) is opgesloten in de opening tussen de biomagnifier en de spiegel. Het optische ingangsvermogen van het vanglicht was ingesteld op 10 mW. (j) Gesimuleerde optische krachten van het nanodeeltje gevangen in de lichtvlek als een functie van de positie van het nanodeeltje langs de x-richting. (k) Berekend vangpotentieel van het ingesloten nanodeeltje als functie van de positie langs de x-richting. Credit:Licht:Wetenschap &Toepassingen, doi:10.1038/s41377-019-0168-4
Daarna, wanneer ze gelijktijdig nabij-infrarood (IR) en UV-laserstralen op de biomagnifier door een objectieflens bestraalden, ze zouden de nanodeeltjes kunnen vangen en opwekken. Voor deze experimenten is de wetenschappers gebruikten fluorescerende nanodeeltjes met een gemiddelde straal van 50 nm. Toen ze een enkel nanodeeltje opsloten in de focus van een biomagnifier, ze observeerden zowel optische als fluorescerende beelden van het betreffende monster. Li et al. berekende vervolgens de vangststijfheid van het deeltje in realtime met behulp van een standaard optisch pincet. De mogelijkheid om een enkel nanodeeltje contactloos en precies via optica te manipuleren, zal nuttig zijn om goed gereguleerde nanostructuren te assembleren. Wanneer Li et al. numeriek het beeldvormingsmechanisme en de vangststijfheid van biomagnifiers onderzocht met behulp van 3D-simulatie en COMSOL-software. Ze observeerden dat het subdiffractie-limietlichtfocusvermogen het gevolg was van een gecombineerd "fotonisch nanojet" -effect en coherente interferentieverbetering door de spiegel.
Beperkingen van de methode omvatten beeldvorming aberratie en vervorming als gevolg van de inhomogene intracellulaire structuren van de natuurlijke biomagnifier, vergeleken met diëlektrische microsferen met uniforme brekingsindices. Gelukkig, intracellulaire materialen waren optisch transparant voor zichtbaar en nabij-infrarood licht en de optische interacties waren relatief zwak in een enkele cel. Intracellulaire activiteiten kunnen ook de partiële brekingsindexverdeling in een cel veranderen om lichtvervorming te veroorzaken tijdens het vangen en beeldvorming, maar de meeste intracellulaire activiteiten waren ultrasnel en hadden geen invloed op het beeldvormingsschema.
Op deze manier, Yuchao Li en collega's ontwikkelden een nieuwe experimentele beeldvormingstechniek en verifieerden de experimentele mogelijkheden met FEM-simulaties. Li et al. geïntegreerde optische nanoscopen en nanopincet in een enkel apparaat om voor het eerst in dit werk nanostructuren tegelijkertijd af te beelden en te manipuleren. Ze bevorderden de resolutie van de techniek tot 100 nm en stelden een labelvrije beeldvormingsprocedure voor. De wetenschappers stellen zich de levende biomagnifier voor om nieuwe kansen te openen in beeldvorming met superresolutie, real-time detectie en nauwkeurige nano-assemblage van bionanomaterialen om interessante nanoarchitecturen te vormen.
© 2019 Wetenschap X Netwerk
 Verschillen tussen HDPE kunststof en polyethyleen kunststof
Verschillen tussen HDPE kunststof en polyethyleen kunststof  Zeewier:van superfood tot supergeleider
Zeewier:van superfood tot supergeleider Zelfbevloeiende grond kan de landbouw transformeren
Zelfbevloeiende grond kan de landbouw transformeren Gyroscoopmoleculen vormen kristal dat zowel solide als vol beweging is
Gyroscoopmoleculen vormen kristal dat zowel solide als vol beweging is Nieuwe elektroden kunnen de efficiëntie van elektrische voertuigen en vliegtuigen verhogen
Nieuwe elektroden kunnen de efficiëntie van elektrische voertuigen en vliegtuigen verhogen
Hoofdlijnen
- Een titerrapport lezen
- Hoe gedraag je je in een dierentuin - volgens de wetenschap
- Hoe de griezelige verkenningen van de zomer
- Microbiële ziekten en mutaties: wat is het ?, Lijsten & Oorzaken
- Grootte doet er niet toe - althans voor hamerhaaien en zwemprestaties
- Disruptieve bio-engineering - verandert de manier waarop cellen met elkaar omgaan
- Het belang van DNA in de menselijke cel
- Zijn er evolutionaire wortels voor menselijke obesitas?
- 10, 000 jaar oud DNA bewijst wanneer vissen meren koloniseerden
 Aide van de gouverneur van Iowa prijst Apple-deal, krijgt baan bij bedrijf
Aide van de gouverneur van Iowa prijst Apple-deal, krijgt baan bij bedrijf Droogte zet aan tot extreme maatregelen om Wests wilde paarden te beschermen
Droogte zet aan tot extreme maatregelen om Wests wilde paarden te beschermen NASA bevestigt herontdekte IMAGE-satelliet
NASA bevestigt herontdekte IMAGE-satelliet Wat staat er in de voorspelling en hoe weten we dat?
Wat staat er in de voorspelling en hoe weten we dat? Nanotechnologen vormen bijna wrijvingsloos diamantmateriaal
Nanotechnologen vormen bijna wrijvingsloos diamantmateriaal Tesla gaat $ 920 miljoen aan obligaties afbetalen met bedrijfscontanten
Tesla gaat $ 920 miljoen aan obligaties afbetalen met bedrijfscontanten Afbeelding:Kubik op ruimtestation
Afbeelding:Kubik op ruimtestation Klaar om ruimtepuin op te sporen
Klaar om ruimtepuin op te sporen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Dutch | Norway | Swedish | German | Danish |

-
Wetenschap © https://nl.scienceaq.com