
Wetenschap
Massa berekenen met het getal van Avogadro:een praktische gids
Door Kylene Arnold Bijgewerkt op 24 maart 2022
Het getal van Avogadro is ongeveer gelijk aan 6,022 x 10^23. Deze hoeveelheid vormt de basis voor een andere maateenheid die veel wordt gebruikt in de scheikunde:de mol. Eén mol is een hoeveelheid gelijk aan het getal van Avogadro. Wanneer wetenschappers daarom het getal van Avogadro gebruiken, meten ze meestal molaire grootheden. Eén van deze molaire grootheden is de molaire massa, die gelijk is aan het aantal gram per mol van die stof. De molaire massa van een element is gemakshalve gelijk aan het atomaire massagetal, dat u kunt vinden in het periodiek systeem. Als je het atoommassanummer van een element en de massa van je monster kent, kun je de massa van elk element in het monster vinden door de mol te gebruiken.
Stap 1
Vind de totale massa van de stof door deze op een massabalans te meten. Vergeet hierbij niet de massa van uw maatbeker af te trekken.
Als een watermonster bijvoorbeeld 13 gram in het bekerglas weegt en het bekerglas een massa van 3 gram heeft, heeft het water een massa van 10 gram.
Stap 2
Bepaal de chemische formule van de stof. Water heeft bijvoorbeeld de formule H2O.
Stap 3
Zoek het atomaire massagetal van elk element in de verbinding. Deze informatie staat in het periodiek systeem, meestal als decimaal getal boven of onder het chemische symbool. Het atomaire massagetal is ook gelijk aan de massa in grammen van één mol van dat element. Dit wordt de molaire massa genoemd. Het atomaire massagetal van waterstof is bijvoorbeeld 1,0079 en dat van zuurstof 15,999. Deze getallen zijn ook gelijk aan de molaire massa van elk element.
Stap 4
Voeg de molmassa's van elk element in de verbinding toe om de totale molmassa van de stof te vinden. Bijvoorbeeld 1,0079 + 1,0079 + 15,999 =18,0148. Elke mol water heeft een massa van 18,0148 gram.
Stap 5
Deel de massa van de verbinding door de molaire massa om het aantal mol in uw monster te bepalen. 10 gram water gedeeld door 18,0148 gram per mol is bijvoorbeeld gelijk aan 0,5551 mol water.
Stap 6
Onderzoek je chemische formule om de verhouding tussen het aantal mol van de verbinding en het aantal mol van elk element te bepalen. Water heeft bijvoorbeeld twee waterstofatomen en één zuurstofatoom in elk molecuul. Daarom zitten er in elke mol water twee mol waterstof en één mol zuurstof.
Stap 7
Vermenigvuldig het aantal mol van uw verbinding met elke verhouding tussen verbinding en element. Om bijvoorbeeld het aantal mol waterstof te vinden, vermenigvuldigt u 0,5551 mol water met 2 mol waterstof per mol water. 0,551 * 2 =1,102, dus er zijn 1,102 mol waterstof in uw monster aanwezig. Met dezelfde methode kun je vaststellen dat er ook 0,5551 mol zuurstof aanwezig is.
Stap 8
Vermenigvuldig het aantal mol van elk element met de molaire massa van dat element. Dit geeft u de totale massa van elk element in uw monster. Bijvoorbeeld 1,102 * 1,0079 =1,111 gram waterstof. Op dezelfde manier is 0,5551 * 15,999 =8,881 gram zuurstof.
Dingen die nodig zijn
- Massabalans
- Periodiek systeem der elementen
 Hoeveel bosbrandrook infiltreert onze huizen?
Hoeveel bosbrandrook infiltreert onze huizen? Eerste metingen van jodium in het noordpoolgebied onthullen vragen over luchtvervuiling
Eerste metingen van jodium in het noordpoolgebied onthullen vragen over luchtvervuiling Tornado treft Luxemburg, gewond 19, beschadigt 100 huizen
Tornado treft Luxemburg, gewond 19, beschadigt 100 huizen Indonesische bosbranden brengen 10 miljoen kinderen in gevaar:UN
Indonesische bosbranden brengen 10 miljoen kinderen in gevaar:UN Federale studie:nieuwe klimaatwet om koolstofvervuiling te verminderen met 40%
Federale studie:nieuwe klimaatwet om koolstofvervuiling te verminderen met 40%
Hoofdlijnen
- Hoe mensen hebben gedomineerd en verstoord met het enten van planten?
- De definitie van moleculaire celbiologie
- Wordt de lac operon gevonden in prokaryoten of eukaryoten?
- Hoe maak je van kelp-aquacultuur een betere koolstofput
- Onderzoek laat zien hoe bacteriële ziekteverwekkers zich aanpassen aan voedingsstress
- Hoe concurreren organismen om voedsel?
- Wat zijn enkele aanpassingen van de gevoelige plant?
- Cytoplasma:het essentiële onderdeel van menselijke cellen - Functie en rol
- Helicase:het enzym dat DNA openritst - Functie en belang
- Vloeibare metalen printen in driedimensionale structuren

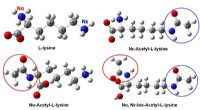
- Raman- en infraroodspectroscopie helpen bij het identificeren van verschillende geacetyleerde lysines
- Bacteriële enzymen gekaapt om complexe moleculen te maken die normaal door planten worden gemaakt
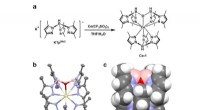
- Diepblauwe organische lichtemitterende diodes op basis van een doublet-emissie cerium(III)-complex
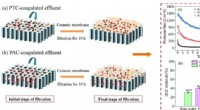
- Polytitaniumchloride pre-coagulatie voor vervuilingscontrole van keramisch membraan
 Wat is de stof gevormd als gevolg van chemische reactie die wordt genoemd?
Wat is de stof gevormd als gevolg van chemische reactie die wordt genoemd?  Waarom schaadt elektriciteit het milieu?
Waarom schaadt elektriciteit het milieu?  Veranderingen in brandactiviteit bedreigen meer dan 4, 400 soorten wereldwijd
Veranderingen in brandactiviteit bedreigen meer dan 4, 400 soorten wereldwijd Hoe de som en het verschil van kubussen te achterhalen
Hoe de som en het verschil van kubussen te achterhalen Tesla levert eerste in China gemaakte Model 3 aan klanten
Tesla levert eerste in China gemaakte Model 3 aan klanten Is wind een vorm van energie?
Is wind een vorm van energie?  Wat is een deel van DNA die code voor eigenschap?
Wat is een deel van DNA die code voor eigenschap?  Welke transcriptiefactor is hoogstwaarschijnlijk wanneer ze naar beneden gereguleerd worden om oligodendrocieten te veroorzaken die zich niet correct vormen?
Welke transcriptiefactor is hoogstwaarschijnlijk wanneer ze naar beneden gereguleerd worden om oligodendrocieten te veroorzaken die zich niet correct vormen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

