
Wetenschap
Atomen, ionen, moleculen en verbindingen:hun verschillen begrijpen
Door Kevin Lee | Bijgewerkt op 24 maart 2022
Afbeelding tegoed:Creativeye99/iStock/GettyImages
Eén zandkorrel bevat grofweg 2,3×10 19 siliciumdioxide (SiO₂) moleculen. Hoewel dat aantal enorm is, bevat het graan zelfs nog meer atomen, omdat elk SiO₂-molecuul uit drie atomen bestaat.
Atomen:de bouwstenen van materie
Atomen zijn de fundamentele eenheden van alle fysieke substanties. Binnenin een atoom vind je een kern – gemaakt van protonen en neutronen – omgeven door een wolk van elektronen. Protonen hebben een positieve lading, elektronen een negatieve lading en neutronen zijn neutraal. Wanneer een atoom een gelijk aantal protonen en elektronen heeft, is het elektrisch neutraal. Elk proton of neutron bestaat zelf uit drie nog kleinere deeltjes die quarks worden genoemd.
Wanneer atomen elektronen verkrijgen of verliezen:de geboorte van ionen
Wanneer een atoom een of meer elektronen verliest, wordt het positief geladen; wanneer het elektronen krijgt, wordt het negatief geladen. Deze geladen atomen worden ionen genoemd. Omdat ionen lading dragen, gedragen ze zich bij chemische reacties anders dan neutrale atomen. De ionenstaart van een komeet, zichtbaar wanneer zonlicht de gassen in zijn coma ioniseert, demonstreert bijvoorbeeld de dynamische aard van ionensoorten.
Moleculen en verbindingen:onderscheidende kenmerken
Een molecuul is een groep van twee of meer atomen die chemisch gebonden zijn. Elementen, zoals goud of waterstof, bestaan uit slechts één type atoom, terwijl verbindingen uit ten minste twee verschillende elementen bestaan. Chemische formules onthullen de exacte samenstelling van een molecuul:water (H₂O) bevat twee waterstofatomen en één zuurstofatoom. Het subscript na het symbool van een element geeft het aantal atomen van dat element aan; als er geen subscript aanwezig is, wordt slechts één atoom aangenomen.
Fascinerende atomaire feiten
Ondanks dat wetenschappers slechts 109 elementen catalogiseren (het aantal is onlangs gestegen tot 118 volgens IUPAC), zijn er meer dan 13 miljoen verschillende verbindingen geïdentificeerd, wat de enorme combinatorische mogelijkheden van atomaire binding illustreert.
Een isotoop is een variant van een element dat qua neutronenaantal verschilt. De meest voorkomende isotoop van waterstof (protium) heeft bijvoorbeeld één proton en geen neutronen, maar de zwaardere vormen ervan – deuterium (één proton, één neutron) en tritium (één proton, twee neutronen) – introduceren verschillende nucleaire eigenschappen. Wanneer een kern stabiliteit zoekt, kan deze ioniserende straling uitzenden, een fenomeen dat centraal staat in de nucleaire chemie en natuurkunde.
 Wat is de moleculaire formule van koperacetaat?
Wat is de moleculaire formule van koperacetaat?  Waarom natriumchloride en cesium hebben verschillende structuren?
Waarom natriumchloride en cesium hebben verschillende structuren?  Als voor 1,25 gram zuiver CaCO3 25,5 ml HCl-oplossing nodig is voor een volledige reactie, wat is dan de molariteitsoplossing?
Als voor 1,25 gram zuiver CaCO3 25,5 ml HCl-oplossing nodig is voor een volledige reactie, wat is dan de molariteitsoplossing?  Hiërarchisch 3D-printen van nanoporeus goud kan een revolutie teweegbrengen in het ontwerp van elektrochemische reactoren
Hiërarchisch 3D-printen van nanoporeus goud kan een revolutie teweegbrengen in het ontwerp van elektrochemische reactoren Onderzoek wijst op uniek medicijndoelwit in antibioticaresistente bacteriën
Onderzoek wijst op uniek medicijndoelwit in antibioticaresistente bacteriën
 Vraag en antwoord:La Nina kan meer Atlantische stormen brengen, westelijke droogte
Vraag en antwoord:La Nina kan meer Atlantische stormen brengen, westelijke droogte Aziatische karpers die in veel grotere gebieden van Lake Michigan kunnen overleven dan eerder werd gedacht
Aziatische karpers die in veel grotere gebieden van Lake Michigan kunnen overleven dan eerder werd gedacht Kunnen vleermuizen mensen begeleiden naar schoon drinkwater op plekken waar het schaars is?
Kunnen vleermuizen mensen begeleiden naar schoon drinkwater op plekken waar het schaars is? Wat gebeurt er tijdens fotosynthese in planten?
Wat gebeurt er tijdens fotosynthese in planten?  Hoe de politiek onze persoonlijke relaties drijft – en zelfs waar we wonen
Hoe de politiek onze persoonlijke relaties drijft – en zelfs waar we wonen
Hoofdlijnen
- Welke vorm van epidermale cellen tomaten vertonen?
- Wat is het moleculaire gedrag?
- Wat zijn 2 cellen alleen gevonden bij dieren?
- Kan één enkel medicijn de twee belangrijkste doodsoorzaken in de VS behandelen:kanker en hart- en vaatziekten?
- Wat is de betekenis van wetenschappelijke woordniche?
- Welke wetenschapper was de eerste om DNA te modelleren?
- Welke organellen zijn uniek voor prokaryotische cellen?
- Wat is de 3 belangrijke gebeurtenis die leidde tot het begrijpen van de structuur van DNA?
- Wat zijn de cellen die openingen op de onderkant van het blad regelen?
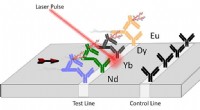
- Nieuwe technologie voor detectie van pathogenen aangedreven door lasers
- Interstellaire ionen nabootsen met lasers

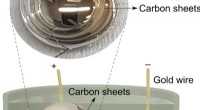
- Vloeibare metalen breken organische brandstoffen af tot ultradunne grafietplaten
- Onderzoekers identificeren enzym dat verantwoordelijk is voor de verspreiding van kankertumoren

- Gezamenlijk onderzoek brengt koers naar honderden nieuwe nitriden

 Tekorten en lege schappen:hoe de toeleveringsketen zo gebroken raakte
Tekorten en lege schappen:hoe de toeleveringsketen zo gebroken raakte  Wetenschap vermengen met traditie onder de migrerende herders van Burkina Fasos
Wetenschap vermengen met traditie onder de migrerende herders van Burkina Fasos Lithium kan nu worden gerecycled
Lithium kan nu worden gerecycled Heeft de dichtheid de hoeveelheid warmte die een lichaam kan opslaan?
Heeft de dichtheid de hoeveelheid warmte die een lichaam kan opslaan?  NASA ziet windschering van invloed zijn op tropische cycloon 11S
NASA ziet windschering van invloed zijn op tropische cycloon 11S Hoe kamp X werkte
Hoe kamp X werkte  Gebruiken kerncentrales uranium om energie te produceren?
Gebruiken kerncentrales uranium om energie te produceren?  De rotscyclus:van erosie tot magma en weer terug
De rotscyclus:van erosie tot magma en weer terug
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

