
Wetenschap
Toniciteit begrijpen:osmose en isotone oplossingen
Door John Brennan Bijgewerkt op 24 maart 2022
a_Taiga/iStock/GettyImages
Wanneer water aan de ene kant van een membraan meer opgeloste stoffen bevat dan water aan de andere kant, kunnen er twee dingen gebeuren. Als de opgeloste stof door het membraan kan diffunderen, zal dat ook gebeuren. Als het membraan echter ondoordringbaar is voor de opgeloste stof, zal water in plaats daarvan door het membraan diffunderen. Dit laatste fenomeen wordt osmose genoemd. Toniciteit is een maat voor de relatieve concentratie van niet-penetrerende opgeloste stof aan weerszijden van een membraan. Het gebruikt dezelfde eenheden als molariteit of osmolariteit, maar in tegenstelling tot deze andere metingen worden alleen niet-penetrerende opgeloste stoffen in de berekening meegenomen.
Stap 1
Bepaal het aantal mol opgeloste stof. Een mol is 6,02 x 10 tot de 23 deeltjes (atomen of moleculen, afhankelijk van de bestudeerde stof). Neem eerst de atoommassa voor elk element zoals aangegeven in het periodiek systeem, vermenigvuldig deze met het aantal atomen van dat element in de verbinding en tel de resultaten voor alle elementen in de verbinding bij elkaar op om de molaire massa te vinden:het aantal grammen in één mol van die stof. Deel vervolgens het aantal gram opgeloste stof door de molaire massa van de verbinding om het aantal mol te krijgen.
Stap 2
Bereken de molariteit van de oplossing. De molariteit is gelijk aan het aantal mol opgeloste stof gedeeld door het aantal liters oplosmiddel. Deel dus het aantal mol door het aantal liters oplossing om de molariteit te vinden.
Stap 3
Bepaal of de opgeloste stof dissocieert terwijl deze oplost. Een algemene vuistregel is dat ionische verbindingen zullen dissociëren, terwijl covalent gebonden verbindingen dat niet zullen doen. Vermenigvuldig de molariteit van de oplossing met het aantal ionen dat wordt gevormd wanneer een enkele formule-eenheid van de verbinding dissocieert om de osmolariteit te vinden. CaCl2 zou bijvoorbeeld in water dissociëren en drie ionen vormen, terwijl NaCl er twee zou vormen. Bijgevolg is een 1-molaire oplossing van CaCl2 een 3-osmolaire oplossing, terwijl een 1-molaire oplossing van NaCl een 2-osmolaire oplossing zou zijn.
Stap 4
Bepaal welke opgeloste stoffen door het membraan kunnen diffunderen en welke niet. Als algemene regel geldt dat ureum en opgeloste gassen zoals O2 en CO2 door celmembranen kunnen diffunderen, terwijl glucose of ionen in oplossing dat niet kunnen. De toniciteit is hetzelfde als de osmolariteit, behalve dat deze alleen opgeloste stoffen meet die niet door het membraan kunnen diffunderen. Als een oplossing bijvoorbeeld een concentratie natriumchloride van 300 ml en een concentratie ureum van 100 ml heeft, sluiten we het ureum uit, omdat dit door het celmembraan kan diffunderen. De oplossing zou dus 300 ml zijn met het oog op de toniciteit.
Stap 5
Bepaal of de oplossing isotoon, hypertoon of hypotoon is. Een isotone oplossing heeft aan beide zijden van het membraan dezelfde toniciteit. De cellen in uw lichaam hebben een concentratie van 300 milliosmolaire niet-penetrerende opgeloste stoffen, dus zijn ze isotoon ten opzichte van hun omgeving zolang de interstitiële vloeistof een vergelijkbare concentratie heeft. Een hypertone oplossing zou er een zijn waarbij de concentratie opgeloste stoffen buiten de cel groter is, terwijl een hypotone oplossing een kleinere concentratie opgeloste stoffen heeft in verhouding tot de binnenkant van de cel.
Dingen die nodig zijn
- Potlood
- Papier
- Rekenmachine
TL;DR (te lang; niet gelezen)
Als u zich ooit heeft afgevraagd waarom ziekenhuizen een zoutoplossing gebruiken om bloedverlies te compenseren in plaats van zuiver water, ligt het antwoord in de toniciteit van het bloedplasma ten opzichte van de binnenkant van uw cellen. Zuiver water bevat geen opgeloste stoffen, dus als het ziekenhuis zuiver water rechtstreeks aan uw bloedbaan zou toevoegen, zou het hypotoon zijn voor (minder geconcentreerd dan) uw rode bloedcellen. Water zou geleidelijk in uw rode bloedcellen diffunderen en ervoor zorgen dat ze opzwellen totdat ze barsten. Ziekenhuizen gebruiken in plaats daarvan een zoutoplossing omdat deze isotoon is ten opzichte van uw cellen.
Referenties
- "Chemische principes, de zoektocht naar inzicht, 4e editie"; Peter Atkins en Loretta Jones; 2008.
- "Biologie, een aangepaste editie"; Campbell, Reece, Urry, Kaïn, Wasserman, Minorsky, Jackson; 2008.
 Wat zijn drie methoden om een chemische reactie te versnellen?
Wat zijn drie methoden om een chemische reactie te versnellen?  Hoe is mogelijk dat de beweging van negatieve ladingen zoals elektronen zowel postief als negatief geladen materialen kan produceren?
Hoe is mogelijk dat de beweging van negatieve ladingen zoals elektronen zowel postief als negatief geladen materialen kan produceren?  Wat is chloor in ionenvorm?
Wat is chloor in ionenvorm?  Wat is melamine Formaldehyde?
Wat is melamine Formaldehyde?  Wat wordt apparaat gebruikt in meet de kracht van pekeloplossing?
Wat wordt apparaat gebruikt in meet de kracht van pekeloplossing?
 Nieuw inzicht in de oorsprong van water op aarde
Nieuw inzicht in de oorsprong van water op aarde Welke eigenschappen van water helpen de wortels een boom op te bewegen naar bladeren tegen krachtzwaartekracht?
Welke eigenschappen van water helpen de wortels een boom op te bewegen naar bladeren tegen krachtzwaartekracht?  Hoe helpt uw kennis van het ecosysteem u het proces van opvolging te begrijpen?
Hoe helpt uw kennis van het ecosysteem u het proces van opvolging te begrijpen?  NASA-kaart geeft het meest nauwkeurige in de ruimte gebaseerde beeld van L.A.s koolstofdioxide
NASA-kaart geeft het meest nauwkeurige in de ruimte gebaseerde beeld van L.A.s koolstofdioxide Geboorte van onderzeese vulkaan voor de oostkust van Afrika tot in detail vastgelegd
Geboorte van onderzeese vulkaan voor de oostkust van Afrika tot in detail vastgelegd
Hoofdlijnen
- Wat betreft het klonen van gewassen in weefselcultuur?
- Welke tak van wetenschapsiabetes hoort erbij?
- Wat is het algemene doel van wetenschappers die werken met biotechnologie?
- Welk relatief nieuw veld onderzoekt de invloed van genen en erfelijkheid op acties van een persoon?
- Combineer het mysterie van hoe eencellige levensvormen zich ontwikkelden tot meercellige organismen
- Enzym hebben specifieke vormen die hun functie bepalen?
- Kleine vogels beschikken over een scala aan vliegstijlen dankzij hun evolutionaire voorsprong
- Wat wordt bestudeerd in de wetenschap van somatologie?
- Wat zijn twee andere verschillen planten en dierencel naast muren?
- Op fragmenten gebaseerde benaderingen gebruiken om nieuwe antibiotica te ontdekken
- Ingenieurs vinden dat antioxidanten de visualisatie van polymeren op nanoschaal verbeteren

- Skies of blue:koolstofemissies recyclen tot nuttige chemicaliën en de opwarming van de aarde verminderen

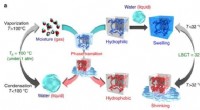
- Onderzoekers rapporteren een temperatuurgevoelige gel die vocht absorbeert en afgeeft
- LED's maken de weg vrij voor betere medicamenteuze therapieën

 In welke vorm treden er normaal gesproken elementen zoals waterstof voor?
In welke vorm treden er normaal gesproken elementen zoals waterstof voor?  Tientallen potentieel blootgesteld aan giftig kwik bij lekkage Houston
Tientallen potentieel blootgesteld aan giftig kwik bij lekkage Houston Universeel klemeiwit stabiliseert gevouwen eiwitten:nieuw inzicht in hoe de chaperonne Hsp70 werkt
Universeel klemeiwit stabiliseert gevouwen eiwitten:nieuw inzicht in hoe de chaperonne Hsp70 werkt  Chemie en informatica bundelen krachten om kunstmatige intelligentie toe te passen op chemische reacties
Chemie en informatica bundelen krachten om kunstmatige intelligentie toe te passen op chemische reacties Zelfassemblerende zoutkristallen origamiballen op nanoschaal omhullen vloeistoffen
Zelfassemblerende zoutkristallen origamiballen op nanoschaal omhullen vloeistoffen  Welke vormen tussen de verdeelde kern tijdens cytokenesis in plantencellen?
Welke vormen tussen de verdeelde kern tijdens cytokenesis in plantencellen?  Is het waar of onwaar, het reflecterende paneel gebruikt kinetische energie van bewegen en waarom?
Is het waar of onwaar, het reflecterende paneel gebruikt kinetische energie van bewegen en waarom?  Wearables zetten een logische stap richting controle aan boord
Wearables zetten een logische stap richting controle aan boord
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

