
Wetenschap
Why Water Is the Ideal Working Fluid for Calorimetry
Door Joe Turner – Bijgewerkt op 24 maart 2022
Wat is een calorimeter?
A calorimeter is a laboratory device that measures the heat exchanged during a chemical reaction or the heat capacity of a substance. The term derives from the Latin word “calor,” meaning heat.
De hoge soortelijke warmte van water
Water’s specific heat capacity is 4.18 J g⁻¹ °C⁻¹, the highest of any common liquid. Dit betekent dat er een grote hoeveelheid energie nodig is om de temperatuur te verhogen, waardoor temperatuurveranderingen in een calorimeter subtiel en gemakkelijk te meten zijn met standaardthermometers.
Praktische voordelen van het gebruik van water
Omdat water over een breed temperatuurbereik vloeibaar blijft, blijft het reactiemengsel in een stabiele fase, waardoor verdamping of koken wordt voorkomen, wat de resultaten zou kunnen vertekenen. Its high heat capacity also minimizes temperature fluctuations, ensuring accurate energy calculations.
Kosten en toegankelijkheid
Kraanwater is goedkoop, overal verkrijgbaar en vereist geen speciale behandelings- of verwijderingsprocedures, in tegenstelling tot veel organische oplosmiddelen die gevaarlijk of kostbaar kunnen zijn.
De calorieën begrijpen
By definition, a calorie is the energy needed to raise the temperature of 1 gram of water by 1 °C. Because water is the reference medium for this unit, its properties make it the cornerstone of calorimetric measurements.
For more detailed information, see the National Institute of Standards and Technology (NIST) data tables of de LibreTexts-chemiesectie over warmte en energie .
 Gigantische A-68 ijsberg drie jaar later
Gigantische A-68 ijsberg drie jaar later Wat is de groene kleur - materie in planten?
Wat is de groene kleur - materie in planten?  Slijmerige chemische aanwijzingen:veranderende algen kunnen ecosystemen veranderen
Slijmerige chemische aanwijzingen:veranderende algen kunnen ecosystemen veranderen Mangroveblauwe koolstof met een hoger risico op microplasticvervuiling
Mangroveblauwe koolstof met een hoger risico op microplasticvervuiling  Plaats dit in bestelling Ecosysteem en gemeenschap van het populatieorganisme?
Plaats dit in bestelling Ecosysteem en gemeenschap van het populatieorganisme?
Hoofdlijnen
- Waarom is een bioom een open systeem?
- Chemiosmose:ATP-productie bij cellulaire ademhaling versus fotosynthese
- Onderzoekers ontsluiten het waterbesparende potentieel van tarwe met TabHLH27 die stress en groei in evenwicht brengt
- Motivaties voor het jagen op dieren in het wild variëren in Afrika en Europa
- Hoe verschilt glucose van sucrose en cellulosezetmeel?
- Waar bevindt het cytoplasma zich op een dierencel?
- Wat is het verschil in celstructuren tussen grampositieve en gramnegatieve bacteriën?
- Wat is een kenmerken van iets in de domein archaea?
- Wat zijn nitraat-pH?
- Cetylpyridiniumchloride (CPC):veiligheid, voordelen en vaak voorkomende bijwerkingen

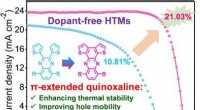
- Doteringsvrij, vochtstabiele organische lagen geven perovskiet-zonnecellen 21% efficiëntie
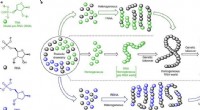
- Onderzoekers suggereren dat RNA en DNA hun oorsprong hebben gevonden in RNA-DNA-chimeren
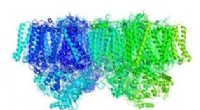
- Mechanisme achter de elektrische ladingen gegenereerd door fotosynthese
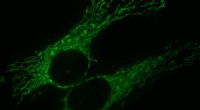
- Samen beter:Mitochondriale fusie ondersteunt celdeling
 Veel oude boeken bevatten giftige chemicaliën. Zo kun je ze herkennen
Veel oude boeken bevatten giftige chemicaliën. Zo kun je ze herkennen  Wetenschappers creëren flexibele biocompatibele trilhaartjes die kunnen worden bestuurd door een magneet
Wetenschappers creëren flexibele biocompatibele trilhaartjes die kunnen worden bestuurd door een magneet Onderzoek onthult nieuwe staat van materie:een Cooper-paar metaal
Onderzoek onthult nieuwe staat van materie:een Cooper-paar metaal Een hel vangen:orkaan Michael raast Florida binnen
Een hel vangen:orkaan Michael raast Florida binnen De missie van je leven:een drone op Titan in 2034 (update)
De missie van je leven:een drone op Titan in 2034 (update) Waarom hebben magnoliabomen was op hun bladeren?
Waarom hebben magnoliabomen was op hun bladeren?  Hoe levende cellen een naald-in-hooiberg-probleem oplossen om elektrische signalen te produceren
Hoe levende cellen een naald-in-hooiberg-probleem oplossen om elektrische signalen te produceren  Hoeveel energie produceert een hydro -elektrisch vermogen elk jaar?
Hoeveel energie produceert een hydro -elektrisch vermogen elk jaar?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

