
Wetenschap
Welke stof zal hoogstwaarschijnlijk niet kwantitatief volgen, de wet van Henry opgelost in water?
Dit is waarom:
* Henry's Law stelt dat de oplosbaarheid van een gas in een vloeistof recht evenredig is met de partiële druk van dat gas boven de vloeistof. Dit veronderstelt dat het opgeloste gas chemisch ongewijzigd blijft in de oplossing.
* chemische reacties Kan de concentratie van het opgeloste gas veranderen, waardoor de oplosbaarheid af zou afwijken van wat de wet van Henry voorspelt. Bijvoorbeeld:
* zure of basisgassen: Gassen zoals Co₂ of NH₃ kunnen reageren met water om respectievelijk koolzuurzuur (H₂co₃) of ammoniumhydroxide (NH₄OH) te vormen. Deze reacties verbruiken het opgeloste gas, wat leidt tot lagere oplosbaarheid dan verwacht door de wet van Henry.
* gassen die complexen vormen: Bepaalde gassen, zoals O₂ of CO, kunnen complexen vormen met watermoleculen of opgeloste ionen. Deze complexen kunnen de vrije gasconcentratie in de oplossing beïnvloeden, wat de oplosbaarheid ervan beïnvloedt.
* reacties met opgeloste soorten: Het opgeloste gas kan reageren met andere opgeloste stoffen in het water, waardoor de concentratie ervan wordt verminderd en afwijkt van de wet van Henry.
Voorbeelden van stoffen die de wet van Henry mogelijk niet volgen:
* koolstofdioxide (co₂): Reageert met water om koolzuur te vormen.
* ammoniak (NH₃): Reageert met water om ammoniumhydroxide te vormen.
* zwaveldioxide (So₂): Reageert met water om zwavelzuurzuur te vormen (h₂so₃).
* waterstofsulfide (H₂s): Kan reageren met water om hydrosulfurinezuur (H₂S) te vormen.
Opmerking: Hoewel veel stoffen tot op zekere hoogte kunnen afwijken van de wet van Henry, vertonen de stoffen die significante chemische reacties met water ondergaan waarschijnlijk de belangrijkste afwijkingen.
 In welke van de volgende verbindingen zijn dipool-dipoolattracties de belangrijkste intermoleculaire kracht ccl4 n2 ch3cl mgbr2 hcn of ch3co2h?
In welke van de volgende verbindingen zijn dipool-dipoolattracties de belangrijkste intermoleculaire kracht ccl4 n2 ch3cl mgbr2 hcn of ch3co2h?  Bestuderen chemici de samenstelling van materie?
Bestuderen chemici de samenstelling van materie?  Hoe worden de roodachtige gaslussen genoemd?
Hoe worden de roodachtige gaslussen genoemd?  Wat is een samengesteld object?
Wat is een samengesteld object?  Hoeveel meter in blokjes stikstofgas kan 1 liter vloeistof produceren?
Hoeveel meter in blokjes stikstofgas kan 1 liter vloeistof produceren?
 Versnelde uitspoeling van radiocesium uit strooisel op de bosbodem door hevige regenval
Versnelde uitspoeling van radiocesium uit strooisel op de bosbodem door hevige regenval Opinie:Maatregelen van armoede en welzijn negeren nog steeds het milieu – dit moet veranderen
Opinie:Maatregelen van armoede en welzijn negeren nog steeds het milieu – dit moet veranderen Waarom is er gras?
Waarom is er gras?  Bewijs gevonden van aardbevingen met lage slip die de voortgang van grote destructieve aardbevingen belemmeren
Bewijs gevonden van aardbevingen met lage slip die de voortgang van grote destructieve aardbevingen belemmeren Het vermijden van lock-in van fossiele brandstoffen kan de wereldwijde temperatuurstijging beperken
Het vermijden van lock-in van fossiele brandstoffen kan de wereldwijde temperatuurstijging beperken
Hoofdlijnen
- Kolonies in verval:wat veroorzaakt de massale sterfte van honingbijen?
- Hoe insecten bacteriën temmen:de oorsprong van symbiotische microben ontdekt nadat de mens zijn hand op een tak heeft gespietst
- Wat is diploïde eukaryotisch?
- Wat is de functie van een dierenspiercel in het organisme?
- Welke phylumgroep protozoa zijn vaak parasieten?
- Dugongs zullen waarschijnlijk functioneel uitgestorven zijn in China
- Waar komt cel vandaan?
- Wat doet het RESTPotory -systeem?
- Wat is een hyphotesis?
- Bouwpakket voor op maat ontworpen producten

- Goud delven met een computer

- Structurele en dynamische verschillen tussen selectieve en niet-selectieve ionkanalen
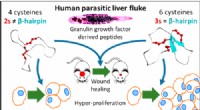
- Een molecuul geproduceerd door een Thaise leverparasiet zou de oplossing kunnen zijn voor die niet-genezende wonden
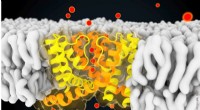
- Wetenschappers verbeteren een fotosynthetisch enzym door fluoroforen toe te voegen

 Is het waar dat stalactieten afzettingen zijn die aan grotdaken hangen die worden veroorzaakt door druipend grondwater?
Is het waar dat stalactieten afzettingen zijn die aan grotdaken hangen die worden veroorzaakt door druipend grondwater?  Wat is afvalwaterlandbouw?
Wat is afvalwaterlandbouw?  Wie heeft wie gekust? Prairiehond 'begroetkusjes' onthullen complexe sociale netwerken
Wie heeft wie gekust? Prairiehond 'begroetkusjes' onthullen complexe sociale netwerken  Onderzoekers bouwen een reeks lichtdetectoren op een fotonische chip die afzonderlijke fotonen kan opnemen
Onderzoekers bouwen een reeks lichtdetectoren op een fotonische chip die afzonderlijke fotonen kan opnemen Is 2 3-Butanedione oplosbaar in water?
Is 2 3-Butanedione oplosbaar in water?  Hydrogel baant weg voor biomedische doorbraak
Hydrogel baant weg voor biomedische doorbraak Nano-naalden kunnen medicijnen in cellen dwingen, zelfs als ze zich ertegen verzetten om het te nemen
Nano-naalden kunnen medicijnen in cellen dwingen, zelfs als ze zich ertegen verzetten om het te nemen Kunstmatige intelligentie bespaart water voor verenigingen van watergebruikers
Kunstmatige intelligentie bespaart water voor verenigingen van watergebruikers
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

