
Wetenschap
Wat is een representatief element? Een duidelijke definitie
Door Joshua Wade Bijgewerkt op 24 maart 2022
Het Periodiek Systeem der Elementen zoals het nu bekend is, werd ontwikkeld door de Russische scheikundige Dmitri Mendelejev en voor het eerst gepresenteerd in het Duitse chemiepriodical Zeitschrift f?r Chemie in 1869. Mendelejev had oorspronkelijk zijn 'Periodiek Systeem' gecreëerd door de eigenschappen van de elementen op stukjes kaart te schrijven en ze te rangschikken in volgorde van toenemend atoomgewicht. Mendelejev stelde ook vast dat de relatieve atoommassa van sommige elementen verkeerd was berekend. Door dit te corrigeren kon hij de elementen op de juiste plaats in de tafel plaatsen. Mendelejev liet ook ruimte voor elementen die nog niet ontdekt waren. Sinds juni 2010 bevat het periodiek systeem 118 bevestigde elementen.
In het periodiek systeem der elementen definiëren kolommen met elementen elementgroepen die veel gemeenschappelijke eigenschappen delen. Er zijn twee groepen groepen in het periodiek systeem. De eerste set bestaat uit Groep A-elementen en worden ook wel representatieve elementen genoemd. De tweede set bestaat uit Groep B-elementen en staan ook bekend als overgangsmetalen. Representatieve elementen zijn de meest voorkomende elementen op aarde.
Representatieve elementen en lay-out van het periodiek systeem
Representatieve elementen en lay-out van het periodiek systeem
In het Periodiek Systeem der Elementen zijn de elementen gerangschikt in kolommen die bekend staan als 'groepen' en rijen die bekend staan als 'perioden'. Groepen bevatten elementen met vergelijkbare eigenschappen die dezelfde elektronenrangschikking in hun buitenste schil hebben, bekend als 'valentie-elektronen', die de eigenschappen van het element en zijn chemische reactiviteit bepalen, en hoe het zal deelnemen aan chemische binding. De Romeinse cijfers boven elke groep bepalen het gebruikelijke aantal valentie-elektronen.
Groepen zijn verder onderverdeeld in representatieve elementen en transitiemetalen. Groepen 1A en 2A aan de linkerkant en 3A tot en met 8A aan de rechterkant worden geclassificeerd als representatieve elementen, terwijl de elementen daartussen geclassificeerd worden als overgangsmetalen. Representatieve elementen zijn ook bekend als \"Groep A,\" \"S- en P-blokelementen\" of \"Hoofdgroepelementen.\"
Betekenis van de lay-out
Betekenis van de lay-out
De lay-out van het periodiek systeem vertoont terugkerende chemische eigenschappen. Elementen worden gerangschikt in volgorde van oplopend atoomnummer (het aantal protonen in de atoomkern) en zo gerangschikt dat elementen met vergelijkbare eigenschappen in dezelfde kolommen vallen. Elementen worden vermeld met onder andere hun elementsymbool, atoomnummer en atoommassa.
Lijst met representatieve elementen in S-blok
Lijst met representatieve elementen in S-blok
De S-blokelementen of de elementen in de kolommen 1A en 2A aan de linkerkant van het periodiek systeem omvatten waterstof (H), lithium (Li), natrium (Na), kalium (K). Rubidium (Rb), Cesium (Cs), Francium (Fr), Beryllium (Be), Magnesium (Mg), Calcium (Ca), Strontium (Sr), Barium (Ba) en Radium (Ra).
Lijst met representatieve elementen in P-blok
Lijst met representatieve elementen in P-blok
De P-blokelementen of de elementen in de kolommen 3A tot en met 8A aan de rechterkant van het periodiek systeem zijn onder meer:
- Boor (B)
- Aluminium (Al)
- Gallium (Ga)
- Indium (In)
- Thallium (Tl)
- Koolstof (C)
- Silicium (Si)
- Germaan (Ge)
- Tin (Sn)
- Lood (Pb)
- Ununquadium (Uuq)
- Stikstof (N)
- Fosfor (P)
- Arseen (As)
- Antimoon (Sb)
- Bismuth (Bi)
- Zuurstof (O)
- Zwavel (S)
- Selenium (Se)
- Tellurium (Te)
- Polonium (Po)
- Fluoride (F)
- Chloor (Cl)
- Broom (Br)
- Jodium (I)
- Astatine (At)
- Helium (Hij)
- Neon (Ne)
- Argon (Ar)
- Krypton (Kr)
- Xenon (Xe)
- Radon (Rn)
Gebruik van het periodiek systeem
Gebruik van het periodiek systeem
Een van de belangrijkste toepassingen van het periodiek systeem is het voorspellen van de chemische eigenschappen van een element op basis van zijn locatie. Mendelejev gebruikte de trends in zijn tabel om de eigenschappen te voorspellen van vijf elementen die nog niet ontdekt waren op het moment dat hij zijn tabel construeerde. De atoomgrootte, het vermogen om een chemische binding te vormen en de energie die nodig is om een elektron te verwijderen, nemen allemaal af als je van links naar rechts beweegt over een bepaalde periode, en nemen toe als je een kolom verder gaat.
Hoofdlijnen
- Heeft de cel van het lichaam een identieke substantie in hun cytoplasma?
- Hoe zorgt heet water ervoor dat DNA vrijkomt in de celkernen?
- Zijn suikers gecreëerd tijdens aerobe ademhaling?
- Nerveus weefsel bestaat uit cellen die worden genoemd?
- Een epigenetisch effect dat het geslacht van een kind beïnvloedt, is de?
- Wat zijn de drie overeenkomsten tussen planten- en dierencel?
- Hoe zou je de wetenschap beschrijven?
- Welke structuur transporteert water en voedingsstoffen van de wortels naar de rest van de plant?
- Waarom leven bacteriën?
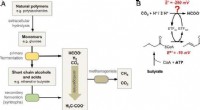
- Cruciale stap geïdentificeerd in de omzetting van biomassa naar methaan
- Peptide-vingerafdruk maakt eerdere diagnose van de ziekte van Alzheimer mogelijk

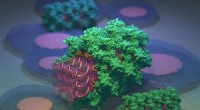
- DNA-nanostructuren worden gecamoufleerd door eiwitten
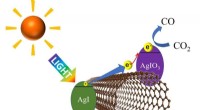
- Zichtbaar licht gebruiken om koolstofdioxide efficiënt af te breken
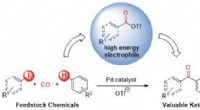
- Een groenere manier om ketonen te maken
 Bestaan er waterstofbruggen binnen een watermolecuul?
Bestaan er waterstofbruggen binnen een watermolecuul?  Kan een land kernenergie krijgen?
Kan een land kernenergie krijgen?  Wat is de waterdruk op 1500 meter diep in de golf?
Wat is de waterdruk op 1500 meter diep in de golf?  Hoe scheiden de batterij negatieve energie en positieve energie?
Hoe scheiden de batterij negatieve energie en positieve energie?  Berekening van de katalytische efficiëntie van enzymen:een praktische gids
Berekening van de katalytische efficiëntie van enzymen:een praktische gids  Wat zijn de 4 soorten snelheidswetten?
Wat zijn de 4 soorten snelheidswetten?  Meer natuurlijk voorkomende bomen en minder clustering kunnen stedelijke bossen ten goede komen
Meer natuurlijk voorkomende bomen en minder clustering kunnen stedelijke bossen ten goede komen Waarom er oceanen kunnen zijn in dwergplaneten voorbij Pluto – en wat dit betekent voor de waarschijnlijke overvloed aan leven
Waarom er oceanen kunnen zijn in dwergplaneten voorbij Pluto – en wat dit betekent voor de waarschijnlijke overvloed aan leven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


