
Wetenschap
De valentie van waterstof uitgelegd:waarom het één is en de impact ervan op de chemie
Door Kevin Carr – Bijgewerkt op 24 maart 2022
Afbeelding tegoed:luchschen/iStock/GettyImages
Atomen verbinden zich via chemische bindingen door elektronen te delen, een proces dat wordt bepaald door het buitenste elektronenaantal van elk element. Het aantal elektronen dat beschikbaar is om te delen in de buitenste schil is wat scheikundigen de valentie noemen.
TL;DR (te lang; niet gelezen)
Waterstof heeft, samen met alle elementen in de eerste groep van het periodiek systeem, een valentie van één.
Valentie-elektronen
Valentie-elektronen zijn de elektronen die zich op het hoogste energieniveau bevinden en die kunnen deelnemen aan chemische bindingen. In de covalente chemie worden deze elektronen gedeeld tussen atomen om te voldoen aan de octetregel, die stelt dat een stabiele configuratie gewoonlijk acht elektronen in de buitenste schil vereist. Wanneer een atoom al acht elektronen heeft, gedraagt het zich als een edelgas en blijft het inert. Atomen met minder dan acht elektronen zullen elektronen delen of overdragen om hun octet te voltooien.
Valentie van waterstof
Waterstof is een speciaal geval:de 1s-orbitaal kan slechts twee elektronen bevatten. Het enkele elektron in deze orbitaal is zijn valentie-elektron, dus het valentiegetal van waterstof is één. Het kan dit eenzame elektron delen met een ander atoom om zijn schil te vullen, of het kan het verliezen om een proton (H+) te vormen in zure oplossingen. Vanwege deze veelzijdigheid bindt waterstof zich met veel elementen. Vier waterstofatomen binden zich bijvoorbeeld met één koolstofatoom (valentie vier) om methaan (CH4) te vormen, en drie waterstofatomen combineren met één stikstofatoom (valentie vijf) om ammoniak (NH3) te produceren.
Andere waterstofverbindingen
Het vermogen van waterstof om zijn valentie-elektron te delen of te doneren, zorgt ervoor dat het zowel covalente als ionische bindingen kan vormen. Het kan zijn elektron doneren aan elektronegatieve atomen zoals fluor of chloor, waardoor ionische soorten zoals HCl+ ontstaan. Waterstof kan ook met zichzelf paren om H2-moleculen te produceren. In een waterige oplossing verliest waterstof vaak zijn elektron en wordt het de hydron (H+) die bijdraagt aan de zuurgraad van een oplossing.
Valentie van andere elementen
Groep 1-elementen, waaronder lithium, natrium en kalium, hebben ook een valentie van één. Groep 2-elementen (beryllium, magnesium, calcium, strontium, barium) hebben een valentie van twee. Overgangsmetalen (groepen 3-12) vertonen een bereik van valenties van één tot zeven, afhankelijk van hun elektronenconfiguratie en oxidatietoestand.
Groep 13-atomen (boor, aluminium) hebben een maximale valentie van drie. Groep 14-atomen (koolstof, silicium, germanium) kunnen een valentie van vier bereiken. Groep 15 atomen (stikstof, fosfor, arseen) zijn maximaal vijf. Groep 16-atomen (zuurstof, zwavel, selenium) bereiken maximaal zes. Groep 17-atomen (fluor, chloor, broom) kunnen er zeven bereiken. Edelgassen (groep 18) bezitten acht valentie-elektronen, maar omdat ze al stabiel zijn, wordt aangenomen dat ze een valentie nul hebben.
 Opsomming van verschillende soorten ecosysteem geven elk 2 voorbeelden?
Opsomming van verschillende soorten ecosysteem geven elk 2 voorbeelden?  Sprankelende stranden:Cyprus heeft schoonste wateren in de EU
Sprankelende stranden:Cyprus heeft schoonste wateren in de EU Onderzoekers ontdekken dat pompen jong grondwater naar nieuwe diepten trekt, mogelijk met verontreinigingen op sleeptouw
Onderzoekers ontdekken dat pompen jong grondwater naar nieuwe diepten trekt, mogelijk met verontreinigingen op sleeptouw Een onderzeese vulkaan ontdekt in de buurt van Christmas Island lijkt op het oog van Sauron
Een onderzeese vulkaan ontdekt in de buurt van Christmas Island lijkt op het oog van Sauron Deep learning kunstmatige intelligentie houdt vulkaanbewegingen in de gaten
Deep learning kunstmatige intelligentie houdt vulkaanbewegingen in de gaten
Hoofdlijnen
- Wat is de beschermende barrière die alle cellen omsluit?
- Terugkeer van de inheemse wilde kalkoen - duurzame oogstdoelen stellen wanneer de informatie beperkt is
- Wat is het embryo's orgaan van ademhalingsvoeding en uitscheiding?
- Hoeveel vellen papier kunnen uit één enkele boom worden geproduceerd?
- Biogene sedimenten zijn schelpen en skeletten van mariene dierenalgen welke twee voorbeelden dit?
- Welke klier speelt een belangrijke rol in zowel de immuun- als de cardiovasculaire systemen?
- Wat wordt door wetenschappers gebruikt om iets uit te leggen dat we niet kunnen zien of begrijpen?
- Welke andere organen die betrokken zijn bij het integumentaire systeem?
- Wat is het nucleïnezuur centraal in het metabolisme?
- Ingenieurs hergebruiken 19e-eeuwse fotografietechniek om rekbare, van kleur veranderende films te maken

- Wetenschappers ontdekken nieuwe scheikunde die de oorsprong van cellulair leven kan helpen verklaren
- AI-software helpt bij het ontwerpen van nieuw materiaal voor zonnecellen
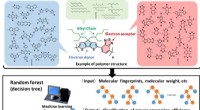
- Onderzoekers verwerven gelaagde metaalhalogenide-ferro-elektriciteit met hoge Curie-temperatuur via kooi-begrensde ethylaminerotators
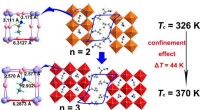
- Spannende tijden voor efficiënte, zware atoomvrije OLED's
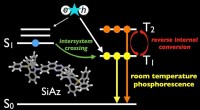
 Gaan materie en energie ooit op elkaar inwerken?
Gaan materie en energie ooit op elkaar inwerken?  Wat gebeurt er met de grootte van een deeltje in het monster wanneer vloeistof wordt verwarmd gesloten container totdat het van van gas verandert?
Wat gebeurt er met de grootte van een deeltje in het monster wanneer vloeistof wordt verwarmd gesloten container totdat het van van gas verandert?  Testen hoe soorten reageren op klimaatverandering
Testen hoe soorten reageren op klimaatverandering  Nicotine Hoe werkt
Nicotine Hoe werkt  Ontsteking van het synthetische transport van aminozuren in levende cellen
Ontsteking van het synthetische transport van aminozuren in levende cellen Wanneer een kracht wordt uitgeoefend op doos is een gelijke en tegengestelde reactie?
Wanneer een kracht wordt uitgeoefend op doos is een gelijke en tegengestelde reactie?  Voorbij de Uber-golf:hoe u zich kunt verplaatsen op oudejaarsavond
Voorbij de Uber-golf:hoe u zich kunt verplaatsen op oudejaarsavond  Netflix stimuleert productie Europese series
Netflix stimuleert productie Europese series
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

