
Wetenschap
Vloeistoffen met lagere kookpunten dan water:een wetenschappelijk overzicht
Door John Brennan
Bijgewerkt op 24 maart 2022
Kookpunten variëren afhankelijk van de moleculaire structuur. Het kookpunt van water bij atmosferische druk is 100°C (212°F). Veel gassen koken ver onder kamertemperatuur, en sommige vloeistoffen, zoals ethanol, hebben ook lagere kookpunten dan water.
Atmosferische gassen
Veel voorkomende atmosferische gassen, waaronder stikstof (N₂), zuurstof (O₂), kooldioxide, chloor (Cl₂) en waterstof, koken bij temperaturen ruim onder de 100 °C. Vloeibaar helium heeft bijvoorbeeld het laagste kookpunt van alle stoffen, namelijk ongeveer –268,9°C (-452°F), slechts 4,2°C boven het absolute nulpunt. Deze voorbeelden illustreren dat de classificatie van een stof als gas of vloeistof volledig afhankelijk is van temperatuur en druk.
Niet-polaire koolwaterstoffen
Water is een polair molecuul met een dipoolmoment; koolwaterstoffen zoals benzinecomponenten zijn niet-polair. Hun intermoleculaire krachten worden gedomineerd door Londense dispersiekrachten, die sterker worden naarmate de moleculaire omvang toeneemt. Bijgevolg koken kleine niet-polaire moleculen doorgaans bij lagere temperaturen dan water, omdat hun zwakkere interacties minder energie vereisen om te verdampen.
Alcoholen
Alcoholen zijn polair en kunnen waterstofbruggen vormen, maar meestal kunnen ze slechts één waterstofbrug per molecuul vormen, vergeleken met twee voor water. Als gevolg hiervan hebben alcoholen hogere kookpunten dan vergelijkbare koolwaterstoffen, maar lager dan water. Distillatie maakt gebruik van dit verschil om ethanol te concentreren in dranken zoals whisky.
Andere moleculen
Ethers – verbindingen waarbij een zuurstofatoom twee koolstofatomen overbrugt – zijn enigszins polair, maar hebben geen waterstofbindingsvermogen, waardoor ze lagere kookpunten hebben dan water. Ammoniak (NH₃) is een ander voorbeeld; het kookt bij –33°C en wordt bij kamertemperatuur als gas aangetroffen, dat gemakkelijk in water oplost. Deze en andere verbindingen laten verder zien hoe de moleculaire structuur het kookgedrag dicteert.
 Prototype ruimtesensoren maken testrit op NASA ER-2
Prototype ruimtesensoren maken testrit op NASA ER-2 Andalusische wetenschappers reconstrueren hoe de Gibraltar Arc er 9 miljoen jaar geleden uitzag
Andalusische wetenschappers reconstrueren hoe de Gibraltar Arc er 9 miljoen jaar geleden uitzag Wat zijn enkele positieve effecten van een orkaan?
Wat zijn enkele positieve effecten van een orkaan?  Noord-Atlantische Oceaan wordt minder zout, maar het is te vroeg om klimaatverandering de schuld te geven
Noord-Atlantische Oceaan wordt minder zout, maar het is te vroeg om klimaatverandering de schuld te geven Warme zomers kunnen de oceaancirculatie verzwakken
Warme zomers kunnen de oceaancirculatie verzwakken
Hoofdlijnen
- Welk cytoskeleteiwit helpt een cel zijn vorm te behouden?
- Ondergewaardeerde microben krijgen nu de eer voor het behouden van twee banen in de bodem
- CRISPR-octrooioorlogen benadrukken het probleem van het verlenen van brede intellectuele eigendomsrechten voor technologie die publieke voordelen biedt
- Wat is de naam van dikke lagere end spijsverteringskanaal waar vast afval verzameld en het lichaam verlaat?
- Welk proces ondergaan alle embryo's terwijl ze zich blijven ontwikkelen tot een volwassen organisme?
- Waar wordt genetische informatie gedragen in DNA?
- Wat zijn de eerste fagocytische cellen die op de plaats van een bacteriële infectie aankomen?
- Wat zijn de twee weefsellagen van diploblastische organismen?
- Hoe gebruiken wetenschappers de dichotome sleutel voor het classificeren van organismen?
- De verborgen risico's van popcorn met botersmaak:wat de wetenschap zegt

- Onderzoekers identificeren de bron van asymmetrie in RNA-DNA-hybriden
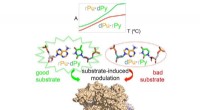
- Ultrasnelle compressie biedt nieuwe manier om macromoleculen in cellen te krijgen

- Beeldvorming van opeenvolgende potentiaalverdelingsveranderingen in elektroden tijdens laden/ontladen

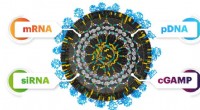
- Ontdekking van een universeel systeem voor het transporteren van nucleïnezuren in cellen
 China wil een ruimteschip bouwen dat kilometers lang is
China wil een ruimteschip bouwen dat kilometers lang is In welke groepen zijn organismen verdeeld?
In welke groepen zijn organismen verdeeld?  Wanneer de zomer begint op het oostelijk halfrond?
Wanneer de zomer begint op het oostelijk halfrond?  Gezichtsherkenning betrapt gebruiker van neppaspoort op Amerikaanse luchthaven
Gezichtsherkenning betrapt gebruiker van neppaspoort op Amerikaanse luchthaven Welke energie verandert er als je kaarsen op een taart aanstuurt?
Welke energie verandert er als je kaarsen op een taart aanstuurt?  BioAlchemy:afvalwater behandelen op het punt van productie
BioAlchemy:afvalwater behandelen op het punt van productie Hoe zandzakken werken
Hoe zandzakken werken  Kwantuminterferentie in de tijd
Kwantuminterferentie in de tijd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

