
Wetenschap
Stapsgewijze handleiding voor het berekenen van de alkaliteit op basis van een titratie
Door Timothy Banas • Bijgewerkt 24 maart 2022
In de analytische chemie is titratie een betrouwbare methode om de alkaliteit van een onbekende oplossing te kwantificeren. Alkaliteit vertegenwoordigt het vermogen van de oplossing om zuur te neutraliseren en is in wezen het tegenovergestelde van de zuurgraad. Door zorgvuldig een titrant met een bekende concentratie aan het monster toe te voegen totdat een kleurverandering gelijkwaardigheid aangeeft, kunnen we de pH van de oplossing berekenen met een eenvoudige reeks berekeningen.
Stap 1 – Noteer het aantal druppels
Noteer na voltooiing van de titratie het totale aantal druppels dat nodig is om het eindpunt te bereiken. Er kunnen bijvoorbeeld 40 druppels 1 M zoutzuur (HCl) nodig zijn geweest om 0,5 liter van de onbekende oplossing te neutraliseren.
Stap 2 – Converteer druppels naar milliliter
Omdat een oplossing op waterbasis ruwweg één milliliter per 20 druppels oplevert, deelt u het aantal druppels door 20 om het gebruikte zuurvolume te vinden.
Voorbeeld:40 ÷ 20 =2 ml
Stap 3 – Milliliters omrekenen naar liters
Deel de milliliterwaarde door 1.000 om het volume in liters uit te drukken.
Voorbeeld:2 ÷ 1.000 =0,002 L
Stap 4 – Bereken het aantal mol zuur
Vermenigvuldig het volume (in liters) met de molariteit van het zuur om te bepalen hoeveel mol H⁺ er is toegevoegd.
Voorbeeld:0,002 L × 1 M =0,002 mol
Stap 5 – Converteren naar equivalente mol H⁺
Pas de stoichiometrie van het zuur aan door te vermenigvuldigen met het aantal H⁺-ionen per molecuul. Voor HCl is deze factor 1; voor H₂SO₄ zou dit 2 zijn.
Voorbeeld:0,002 mol × 1 =0,002 equivalenten
Stap 6 – Bepaal [OH⁻] in het onbekende
Deel het equivalente aantal mol door het volume (in liters) van de oorspronkelijke oplossing om de concentratie hydroxide-ionen te vinden.
Voorbeeld:0,002 ÷ 0,5 L =0,004 M
Stap 7 – Bereken pOH
Neem de negatieve logaritme met grondtal 10 van de [OH⁻]-waarde om pOH te verkrijgen.
Voorbeeld:pOH =–log(0,004) ≈ 2,4
Stap 8 – Converteren naar pH
Trek de pOH af van 14 om de pH van de oplossing te verkrijgen.
Voorbeeld:pH =14 – 2,4 =11,6De onbekende oplossing heeft dus een pH van 11,6.
 Kan gebruikt koffiedik helpen bij het opruimen van milieutoxines?
Kan gebruikt koffiedik helpen bij het opruimen van milieutoxines?  Nucleatiekinetiek in kaart brengen met nanometerresolutie
Nucleatiekinetiek in kaart brengen met nanometerresolutie Watervrij calciumchloride:het ideale droogmiddel voor exsiccatoren
Watervrij calciumchloride:het ideale droogmiddel voor exsiccatoren  De poriën in membraanblaasjes onderzoeken
De poriën in membraanblaasjes onderzoeken Actieve methyleenverbindingen:eigenschappen, reactiviteit en voorbeelden
Actieve methyleenverbindingen:eigenschappen, reactiviteit en voorbeelden
 Gevallen herfstbladeren zijn een waardevolle hulpbron. Hier leest u hoe u er het beste van kunt maken
Gevallen herfstbladeren zijn een waardevolle hulpbron. Hier leest u hoe u er het beste van kunt maken  Waarom overstromt het waar er niet veel bomen in de buurt zijn?
Waarom overstromt het waar er niet veel bomen in de buurt zijn?  Het ondergronds opslaan van CO2 kan de CO2-uitstoot terugdringen, maar is het veilig?
Het ondergronds opslaan van CO2 kan de CO2-uitstoot terugdringen, maar is het veilig? Onderzoek kan controverses met betrekking tot grote magma-uitbarstingen verklaren
Onderzoek kan controverses met betrekking tot grote magma-uitbarstingen verklaren Cristobal herwint tropische stormkracht op weg naar Amerikaanse kust
Cristobal herwint tropische stormkracht op weg naar Amerikaanse kust
Hoofdlijnen
- Wat is de wetenschappelijke naam voor sporen?
- De belangrijkste rol bij het bepalen van de verdeling van biomen komt vandaan?
- Wat wordt voornamelijk gevormd uit dode cellen?
- Wat is de juiste uitspraak van woordwetenschap?
- Waarom zijn mutaties belangrijk voor evolutie?
- Het gen dat volledig tot expressie wordt gebracht wanneer twee verschillende allelen aanwezig zijn?
- Organismen kunnen worden onderverdeeld in domeinen op basis van kenmerken van hun cellen. Wat is deze domeinen?
- Welke cel transporteert zuurstof?
- Is schimmel een levend of niet -leven?
- De gevoeligheid van COVID-tests meten met nieuw materiaal van NIST
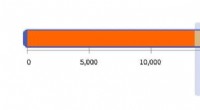
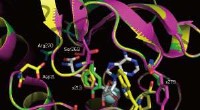
- Gerichte evolutie om enzymen te ontwerpen die beeldvormende middelen maken voor medische diagnose
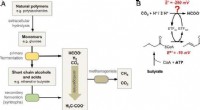
- Cruciale stap geïdentificeerd in de omzetting van biomassa naar methaan
- Enkele atomen verbreken de sterkste binding van koolstof

- Verbrandingsgedrag van aromaten kan de sleutel zijn tot het verbeteren van de extractie van zware olie

 Studie vindt geheim van diverse bossen super succes
Studie vindt geheim van diverse bossen super succes Hoe het kwadraat van binomiaal te vinden
Hoe het kwadraat van binomiaal te vinden  Wetenschappers ontwikkelen een nieuwe, zeer efficiënte fotokatalysator voor het verwijderen van kwik
Wetenschappers ontwikkelen een nieuwe, zeer efficiënte fotokatalysator voor het verwijderen van kwik  Let me flow:Bosniërs voeren oorlog tegen mini-waterkrachtcentrales
Let me flow:Bosniërs voeren oorlog tegen mini-waterkrachtcentrales Waarom wordt bier skunky?
Waarom wordt bier skunky?  Welke verbindingen bevatten de meest energie AMP ADP ATP PI?
Welke verbindingen bevatten de meest energie AMP ADP ATP PI?  Wat is het proces van het veranderen van energie?
Wat is het proces van het veranderen van energie?  Wie was de derde persoon die maan in Apollo 11 reisde?
Wie was de derde persoon die maan in Apollo 11 reisde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

