
Wetenschap
Belangrijke biologische buffers die de homeostase in stand houden
Door David Stewart | Bijgewerkt op 30 augustus 2022
Motortion/iStock/GettyImages
Een buffer is een chemische stof die de pH van een oplossing stabiliseert, zelfs als er zuren of basen worden toegevoegd. In levende systemen is buffering cruciaal voor het handhaven van een stabiele interne omgeving:homeostase. Kleine moleculen zoals bicarbonaat en fosfaat, maar ook macromoleculen zoals hemoglobine en eiwitten, zorgen allemaal voor dit buffervermogen.
Bicarbonaatbuffer
Het bicarbonaatbuffersysteem reguleert de pH van het bloed door een dynamisch evenwicht tussen koolzuur (H₂CO₃) en bicarbonaationen (HCO₃⁻). Wanneer het bloed te zuur wordt, zet de buffer overtollige waterstofionen om in kooldioxide, dat vervolgens door de longen wordt uitgestoten. Omgekeerd wordt bicarbonaat tijdens alkalose via de urine uitgescheiden, waardoor de neutrale pH wordt hersteld.
Fosfaatbuffer
Binnen cellen biedt de fosfaatbuffer, bestaande uit waterstoffosfaat (HPO₄²⁻) en diwaterstoffosfaat (H₂PO₄⁻), een sterkere buffercapaciteit dan het bicarbonaatsysteem. Het neutraliseert overtollige waterstofionen door de minder reactieve fosfaatsoort te vormen, en onder alkalische omstandigheden accepteert het hydroxide-ionen, waardoor de intracellulaire omgeving weer neutraal wordt.
Eiwitbuffer
Eiwitten, opgebouwd uit aminozuren verbonden door peptidebindingen, hebben zijketens die protonen kunnen doneren of accepteren. Bij fysiologische pH bestaan carboxylgroepen als negatief geladen carboxylaationen (COO⁻), terwijl aminogroepen geprotoneerd zijn als NH₃⁺. In zure omstandigheden vangen carboxylaten protonen op om COOH te vormen, en in alkalische omstandigheden laat NH₃⁺ protonen vrij, die NH₂ worden. Beide acties dempen pH-schommelingen.
Hemoglobinebuffer
Hemoglobine, het zuurstofdragende pigment in rode bloedcellen, buffert ook de pH van het weefsel. De globine-subeenheden kunnen protonen binden, terwijl het heemijzer zuurstof bindt. Tijdens het sporten worden overtollige protonen opgenomen door hemoglobine, waardoor tegelijkertijd zuurstof vrijkomt, waardoor de zuurophoping in de spieren wordt verminderd.
 Wat wordt blauw kobaltchloride roze en heeft een kookpunt van 100 graden?
Wat wordt blauw kobaltchloride roze en heeft een kookpunt van 100 graden?  Hoeveel chlooratomen zijn er in twee calciumchloride -formule -eenheden?
Hoeveel chlooratomen zijn er in twee calciumchloride -formule -eenheden?  Waarom reageren niet -metalen niet met water terwijl ze doen?
Waarom reageren niet -metalen niet met water terwijl ze doen?  Wat is de naam van Compound met Formula Nai?
Wat is de naam van Compound met Formula Nai?  Wat is een chemische reactie IT -product of polymeer?
Wat is een chemische reactie IT -product of polymeer?
Hoofdlijnen
- Hoe is het mogelijk dat minder dan 1 procent van de bacteriën ziekte veroorzaken?
- Wat is het bepalende kenmerk van eukaryoten?
- Wat is de wetenschappelijke naam voor stalagmieten?
- Wat gebruikt chemosynthese om voedsel te maken?
- Gebruikt cellulaire ademhaling NADPH als zijn elektronendrager?
- Hoe winkelt een plantensuikers van een plant?
- Cellulaire aanpassing:de rol van stress begrijpen
- Welk enzym is nodig om transcriptie te laten plaatsvinden?
- Is een cel van een prokaryotisch of eukaryotisch van een eikenblad?
- Systematische studie lost discussie over katalysatorontwerp voor uitlaatgassen van auto's op

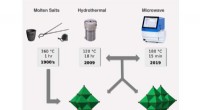
- Energieopslagmaterialen opgebouwd uit moleculaire blokken van nanoformaat
- Kunnen we plastic tassen recyclen tot stoffen van de toekomst?

- 4D-geprint thermiet kan lassen in de ruimte en gevechtszones gemakkelijker maken, veiliger

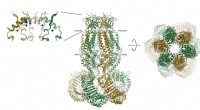
- Cellulaire klepstructuur opent potentiële nieuwe therapieën
 Wat gebeurt er als een zwart gat de zon doorslikt?
Wat gebeurt er als een zwart gat de zon doorslikt?  Een mijlpaal in ultrasnelle gelfabricage van onconventionele zelfherstellende edelmetaalgels
Een mijlpaal in ultrasnelle gelfabricage van onconventionele zelfherstellende edelmetaalgels Zuid-Afrikaanse jongeren zijn een generatie die verloren is gegaan onder de democratie:studie
Zuid-Afrikaanse jongeren zijn een generatie die verloren is gegaan onder de democratie:studie  Welk type energie opgeslagen vanwege zwaartekracht en hoogte boven de grond?
Welk type energie opgeslagen vanwege zwaartekracht en hoogte boven de grond?  Waar converteert energie zich om als een swing heen en weer beweegt?
Waar converteert energie zich om als een swing heen en weer beweegt?  Een kern van waarheid benaderen
Een kern van waarheid benaderen Waarom geeft de natuur de voorkeur aan kruisbestuiving?
Waarom geeft de natuur de voorkeur aan kruisbestuiving?  Wat zijn de 2 soorten natuurlijke hulpbronnen?
Wat zijn de 2 soorten natuurlijke hulpbronnen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

