
Wetenschap
Berekening van de pH-impact van verdunning:een praktische gids
Door Claire Gillespie
Bijgewerkt op 30 augustus 2022
Verdunning is een routinematige laboratoriumtechniek die bètastudenten gebruiken om nauwkeurige concentraties te bereiken. Het gebeurt ook in het dagelijks leven:water toevoegen aan koffie of wijn naar smaak. Belangrijk is dat verdunning de pH van een oplossing verandert, waardoor deze minder zuur of minder basisch wordt, afhankelijk van het uitgangsmateriaal.
TL;DR
Wanneer je een zure oplossing verdunt, beweegt de pH richting 7 (neutraler). Het verdunnen van een basische oplossing duwt de pH ervan naar 7 vanaf de alkalische kant. Bereken het effect door de oorspronkelijke pH om te zetten in waterstofionenconcentratie, die concentratie aan te passen voor het nieuwe volume en vervolgens weer om te rekenen naar pH.
Wat is verdunning?
Door oplosmiddel (meestal water) aan een oplossing toe te voegen, wordt de verhouding van het oplosmiddel ten opzichte van de opgeloste stof vergroot. De hoeveelheid opgeloste stof blijft hetzelfde, maar het volume groeit, dus elke molaire concentratie neemt af met de verhouding tussen het nieuwe volume en het oorspronkelijke volume.
De pH begrijpen
De pH-schaal, variërend van 0 tot 14, kwantificeert de zuurgraad of alkaliteit. Een pH-waarde van 7 is neutraal. Beneden de 7 is de oplossing zuur; boven de 7 is het eenvoudig. De schaal is logaritmisch:elke verandering van een geheel getal vertegenwoordigt een tienvoudig verschil in de waterstofionenconcentratie. pH 3 is bijvoorbeeld tien keer zuurder dan pH 4 en honderd keer zuurder dan pH 5.
pH wordt gedefinieerd als pH =–log[H⁺] , waarbij [H⁺] de molariteit van waterstofionen is. Herschikken geeft [H⁺] =10 –pH .
Een zuur verdunnen
Zuren (bijvoorbeeld citroensap, accuzuur, koffie) bevatten H⁺-ionen. Het toevoegen van water verlaagt [H⁺], waardoor de pH naar 7 stijgt. Omdat het toegevoegde water neutraal is, kan de pH van een zure oplossing nooit boven de 7 komen.
Een basis verdunnen
Basen (bijvoorbeeld ammoniak, bleekmiddel, zuiveringszout) bevatten OH⁻-ionen. Water verdunt OH⁻, waardoor de pH naar 7 daalt. De pH van een basische oplossing kan nooit onder de 7 komen als deze wordt verdund met neutraal water.
Stapsgewijze berekening
1. Zet de aanvankelijke pH om naar de waterstofionenconcentratie. Voor een pH6-oplossing is [H⁺] =10 –6 M.
2. Bepaal de verdunningsfactor. Als het eindvolume vier keer zo groot is als het origineel, wordt de concentratie door vier gedeeld.
3. Bereken de nieuwe [H⁺]. Met behulp van het bovenstaande voorbeeld:[H⁺]new =(10 –6 M) ÷ 4 =2,5 × 10 –7 M.
4. Omzetten naar pH. pHnieuw =–log(2,5 × 10 –7 ) ≈ 6,60.
Een viervoudige verdunning van een pH6-zuur verhoogt de pH dus tot ongeveer 6,6, waardoor deze dichter bij neutraliteit komt.
Praktische tips
- Gebruik altijd een gekalibreerde pH-meter voor nauwkeurige metingen.
- Houd bij sterke zuren of basen rekening met het effect van de ionsterkte op de pH.
- Houd er rekening mee dat de verdunning het neutrale punt (pH 7) niet kan overschrijden als je zuiver water gebruikt.
 Sedimenten in de Noordelijke IJszee onthullen het ontdooien van de permafrost tijdens de klimaatopwarming in het verleden
Sedimenten in de Noordelijke IJszee onthullen het ontdooien van de permafrost tijdens de klimaatopwarming in het verleden Wat is een soft bodem ecosysteem?
Wat is een soft bodem ecosysteem?  Onderzoek toont aan hoe het klimaat de voedselketens beïnvloedt en een sociaal-economische bedreiging vormt in Oost-Afrika
Onderzoek toont aan hoe het klimaat de voedselketens beïnvloedt en een sociaal-economische bedreiging vormt in Oost-Afrika  Vanuatu-eiland opnieuw geëvacueerd na uitbarsting vulkaan
Vanuatu-eiland opnieuw geëvacueerd na uitbarsting vulkaan Zelfs zonder El Nino vorig jaar, Aarde blijft opwarmen
Zelfs zonder El Nino vorig jaar, Aarde blijft opwarmen
Hoofdlijnen
- Hebben sommige eencellige organismen speciale structuren om overtollig water te pompen?
- Hoe een genmutatie leidt tot hogere intelligentie
- Wat zijn de namen en functies van 4 fasen celcyclus?
- Wat is de functie van een triglyceride in levende organismen?
- Hoe komen micro -organismen in het lichaam?
- Plasmiden zijn uniek voor wat?
- Wat is een voorbeeld van een kanaaleiwit?
- Hoe werkt een automatische DNA-sequencer?
- Wie wordt beschouwd als de oprichter van de moderne genetica?
- Licht op waarom plastic geel wordt
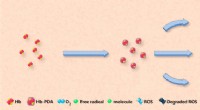
- Kunstbloed maken voor transfusies
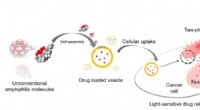
- Nieuwe technologie voor de levering van geneesmiddelen tegen kanker op aanvraag
- De kunst van het balanceren van chemische vergelijkingen beheersen:een praktische gids
- Neurale netwerken gebruiken om resultaten van organische chemie te voorspellen
 Welke twee redenen zouden de beste verklaring zijn voor het feit dat geothermische zonne- en windenergie niet méér worden gebruikt dan nu het geval is?
Welke twee redenen zouden de beste verklaring zijn voor het feit dat geothermische zonne- en windenergie niet méér worden gebruikt dan nu het geval is?  EPA-waakhond onderzoekt luchtkwaliteitsresultaten die zijn uitgegeven na Harvey
EPA-waakhond onderzoekt luchtkwaliteitsresultaten die zijn uitgegeven na Harvey Wat is de term voor wanneer de maan tussen de aarde gaat en de zon van het laatste blokkeert?
Wat is de term voor wanneer de maan tussen de aarde gaat en de zon van het laatste blokkeert?  Zal het mengen van Clorox en remvloeistof echt een explosie veroorzaken?
Zal het mengen van Clorox en remvloeistof echt een explosie veroorzaken?  Welke methode wordt gebruikt om een benaderingssnelheid te bepalen?
Welke methode wordt gebruikt om een benaderingssnelheid te bepalen?  Hoe kinesiotape werkt
Hoe kinesiotape werkt  Organismehabitat:begrijpen waar levende wezens gedijen
Organismehabitat:begrijpen waar levende wezens gedijen  Hoe slaagt u uit de 7e klas wetenschap?
Hoe slaagt u uit de 7e klas wetenschap?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

